▷ 더 보기
▷ 더 보기
▷ 더 보기
▷ 더 보기
▷ 더 보기
▷ 더 보기
▷ 더 보기

▷ 더 보기

▷ 더 보기
 Introduction
Introduction
Introduction
| Introduction |
|---|
| Introduction |
| Introduction |
Introduction
▷ Introduction
| Introduction | Introduction |
|---|---|
| Introduction | Introduction |
| Introduction | Introduction |
| Introduction | Introduction |
Introduction
- References
Introduction
Copyright © 광제당약국's All Rights Reserved.
 국소 칼시뉴린 억제제[Topical calcineurin inhibitors (TCI)]로서는 Tacrolimus 0.03%(프로토픽연고 등) 또는 0.1% 연고와 1.0% Pimecrolimus 크림(엘리델크림 등)이 대표적이다.
국소 칼시뉴린 억제제[Topical calcineurin inhibitors (TCI)]로서는 Tacrolimus 0.03%(프로토픽연고 등) 또는 0.1% 연고와 1.0% Pimecrolimus 크림(엘리델크림 등)이 대표적이다.이들 약물은 염증유발 사이토카인(proinflammatory cytokines)의 합성을 억제하여 활성을 나타내며 아토피성 피부염 치료에 사용된다. TCI는 코르티코스테로이드에 대한 대체 치료로서 사용될 수 있다
Tacrolimus는 보통 및 중증 아토피성 피부염 치료에 사용되며 Pimecrolimus는 경증 및 보통의 아토피성 피부염 치료에 사용된다.
Introduction
| Introduction |
|---|
| Introduction |
| Introduction |
Introduction
▷ Introduction
| Introduction | Introduction |
|---|---|
| Introduction | Introduction |
| Introduction | Introduction |
| Introduction | Introduction |
Introduction
- References
Gutfreund K, Bienias W, Szewczyk A, Kaszuba A. Topical calcineurin inhibitors in dermatology. Part I: Properties, method and effectiveness of drug use. Postepy Dermatol Alergol. 2013 Jun;30(3):165-9. doi: 10.5114/pdia.2013.35619. Epub 2013 Jun 20. PMID: 24278069; PMCID: PMC3834721.
Copyright © MediGloPark's All Rights Reserved.
 ▷ 이상지질혈증은 지단백 대사 이상으로 혈중 지질의 양이 비정상적으로 변화된 질환이다. 고콜레스테롤혈증, 고중성지방혈증, 낮은 고밀도지단백혈증 등으로 구분되며 동맥경화증 및 각종 심혈관질환의 위험인자이다.
▷ 이상지질혈증은 지단백 대사 이상으로 혈중 지질의 양이 비정상적으로 변화된 질환이다. 고콜레스테롤혈증, 고중성지방혈증, 낮은 고밀도지단백혈증 등으로 구분되며 동맥경화증 및 각종 심혈관질환의 위험인자이다.이상지질혈증은 지방대사와 운반에 관여하는 유전자의 결함에 의한 일차성 이상지질혈증과 당뇨병, 과음, 담즙 정체성 간질환, 갑상선 질환, 신부전, 비만, 식이, 임신, 성호르몬, 흡연, 약물 등 이차성 위험요소에 의한 이차성 이상지질혈증이 있다.
콜레스테롤은 인체내에서 세포를 보호하며, 성호르몬을 생성, 비타민D 생성 등에서 중요한 역할을 하지만 잉여의 콜레스테롤은 동맥경화를 유발하는 원인이다. 지질은 혈장에 불용성이므로 지단백(lipoprotein) 형태로 수송된다.
| 혈중 지방질 | 특징 |
|---|---|
| 저밀도지단백 콜레스테롤(LDL cholesterol) | 혈관벽에 쌓여 심혈관질환과 뇌혈관질환을 일으키는 동맥경화를 유발 |
| 고밀도지단백 콜레스테롤(HDL cholesterol) | 혈관벽에 쌓인 콜레스테롤을 간으로 운반하는역할을 하므로 동맥경화를 예방함 |
| 중성지방 | 음식으로 섭취된 과잉의 에너지를 저장하기 위해 생성. 평상시에는 지방세포에 저장되며 필요 시 방출되어 에너지원으로 사용 |
| 총콜레스테롤 | 저밀도지단백 콜레스테롤 + 고밀도지단백 콜레스테롤 |
▷한국인의 이상지질혈증 진단기준(2023년)
| 총콜레스테롤 | 기준수치 |
|---|---|
| 높음 | ≥240 |
| 경계 | 200-239 |
| 적정 | <200 |
| LDL콜레스테롤 | |
| 매우 높음 | ≥190 |
| 높음 | 160-189 |
| 경계 | 130-159 |
| 정상 | 100-129 |
| 적정 | <100 | HDL 콜레스테롤 |
| 낮음 | ≤40 |
| 높음 | ≥ 60 | 중성지방(Triglyceride, TG) |
| 매우 높음 | ≥500 |
| 높음 | 200-499 |
| 경계 | 150-199 |
| 적정 | <150 |
▷지단백 수치에 영향을 미치는 약물
| 약물 | 지단백 증감 |
|---|---|
| Estrogen | 총콜레스테롤↓ LDL↓ HDL↑ VLDL↑ TG↑ |
| Corticosteroids | 총콜레스테롤↑ LDL↑ HDL↑ VLDL↑ TG↑ |
| Cyclosporine | 총콜레스테롤↑ LDL↑ HDL(불변) VLDL(불변) TG(불변) |
| Phenothiazine | 총콜레스테롤↑ HDL↓ |
| 항경련제 | 총콜레스테롤(불변) LDL(불변) HDL↑ TG(불변) |
| Thiazide계 이뇨제 | LDL↑ HDL(불변) VLDL↑ TG↑ |
| 비선택적 β- 차단제 | 총콜레스테롤(불변) LDL(불변) HDL↓ VLDL↑ TG↑ |
| α1-차단제 | LDL↓ HDL↑ TG↓ |
▷당뇨병 치료제가 지질에 미치는 영향
| 약물 | 지단백 증감 |
|---|---|
| 설포닐우레아 (sulfonylurea) | TG↓ LDL(불변) HDL(불변) |
| 메트포르민 (metformin) | TG↓ LDL↓ HDL↑ |
| 치아졸리딘디온 (thiazolidinediones) | TG↓ LDL↑ HDL↑ |
| 알파-글루코시데이즈 (α-glucosidase) 억제제 | TG↓ LDL(불변) HDL(불변) |
| 메글리티나이드 (meglitinide) | TG(불변) LDL(불변) HDL(불변) |
| 인슐린 (insulin) | TG↓ LDL(불변) HDL↑ |
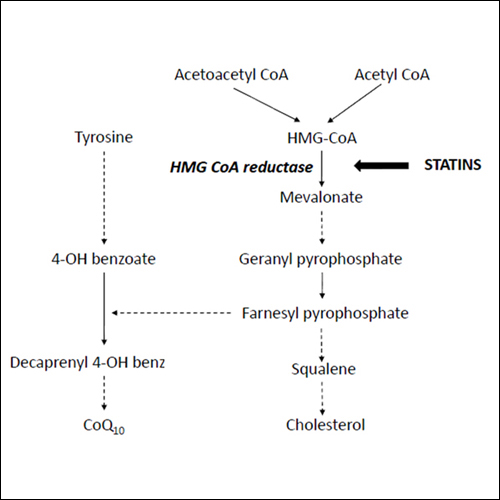
스타틴은 HMG-CoA Reductase 억제제로서 콜레스테롤 합성을 제한하여 간세포내 콜레스테롤 수준이 감소함에 따라 보상반응적으로 세포벽 표면 수용체가 세포의 콜레스테롤 수요를 맞추기 위해 증가하여 결과적으로 혈중 LDL 콜레스테롤 수준이 감소하게 된다. 스타틴은 중성지방을 10~20% 감소시킬 수 있으며 HDL은 약 5~10% 증가시킬 수 있는 것으로 알려져 있다.
Ezetimibe는 NPC1L1 단백을 억제하여 장관 내 콜레스테롤 흡수를 저해하므로 간으로 수송되는 지단백 콜레스테롤의 혈청 수준이 감소한다. 이로 인해 보상반응적 기전으로 간의 LDLR 수용체가 증가하여 순환 콜레스테롤의 제거가 촉진되며 이 과정에서 LDL 콜레스테롤 수준이 20% 감소하는 것으로 알려져 있다.
나이아신(Niacin, Nicotinic acid)은 수용성 비타민으로서 LDL-C(cholesterol) 감소작용이 Statins 만큼 효과적이지는 않지만 HDL-C 증가에는 가장 효과적인 것으로 알려져 있다. 나이아신은 지방조직의 지방산 유동성을 감소시켜 TG(Triglyceride)와 VLDL( very low-density lipoprotein)-C의 저하를 나타낸다. 그러나 안면홍조, 소양증, 구역, 소화불량 등의 부작용으로 사용이 제한적이다.
피브레이트(Fibrates)는 심혈관 사망률 이점을 보이지는 않지만 매우 높은 수준의 중성지방으로 인한 합병증(예: 췌장염) 감소에 이점이 있다. 피브레이트는 omega-3 지방산과 비교 시 50% 정도의 지방산 감소 효과가 있으며, 적지만 LDL-C 감소 및 HDL-C 증가 효과도 있다. 피브레이트는 peroxisomal B-oxidation에서 유전자 전사에 관여하는 PPAR(peroxisome proliferator-activated receptors)을 활성화한다. 즉, 아포지단백 C-III(지방분해 효소의 작용을 저해하는 단백질)의 기능을 저하시키는 PPAR-alpha 인자의 활성을 유도하여 지방분해 효과를 증가시켜 혈중 중성지방의 수치를 낮춘다(Fenofibrate). 피브레이트의 일반적인 부작용은 간효소 증가, creatine phosphokinase 증가, 근육병증, 담석증, 정맥혈전증 등이다.
한편, 피브레이트의 한 종류인 Gemfibrozil은 스타틴 대사를 억제하여 근육병증의 위험성이 증가하므로 스타틴과 병용투여하면 안된다.
Omega-3 지방산은 피브레이트와 유사하게 중성지방 수치를 25~30% 정도 감소시키며 고중성지방혈증(hypertriglyceridemia) 치료에 사용된다. 심혈관계 환자의 사망률 감소에 대한 이점은 확인되지 않았으며 위장관계 부작용 등에 주의하여야 한다.
고중성지방혈증과 죽상경화성 심혈관질환(Atherosclerotic cardiovascular disease, ASCVD)의 연관성에도 불구하고 Omega-3 지방산과 피브레이트는 ASCVD에 의한 질병률 또는 사망률 감소 효과에 대한 증거가 없으므로 췌장염 예방을 위한 심각한 고중성지방혈증(>500~1000)의 경우에 한하여 사용하는 것이 일반적이다.
PCSK9(proprotein convertase subtilisin/kexin type 9)은 간세포내 LDL-C 수용체의 분해를 촉진하고 그 작용 저하에 관여하는 효소로서 PCSK9에 의해 혈중의 LDL을 포획하는 LDL 수용체(LDL Receptor, LDL-R)의 감소가 촉진되어 혈중의 LDL-C의 농도가 증가한다. 이를 타겟으로 하는 합성 항체인 PCSK 억제제(Alirocumab, Evolocumab)는 이상지질혈증 치료에 혁신적이며 스타틴 치료와 무관하게 LDL-C 수준을 45~60% 정도 감소시키는 것으로 알려져 있다. 주된 부작용은 주사부위 이상반응이다.
Inclisiran은 siRNA(small interfering RNA)로서 작용하여 간세포내 PCSK9 효소 생성을 억제하며 고위험 ASCVD와 높은 LDL 수준을 나타내는 환자에 적용한다.
Bempedoic acid는 HMG-CoA reductase를 목표로 하는 기존의 스타틴과 달리 콜레스테롤 합성 상위 단계를 타겟으로 ATP citrate lyase를 억제하여 콜레스테롤 합성을 저해하며, 이에 따른 LDL-R 발현의 증가에 의한 혈장 LDL-C 감소를 나타낸다. Bempedoic acid는 전구약제로서 간에서 대사 된 후에 활성화되고 골격근과 같은 말초조직에서는 활성화되지 않으므로 스타틴의 근육병 부작용이 거의 없는 것으로 알려져 있다.
▷스타틴 제제들의 특징
| Statins | 특징 |
|---|---|
| Atorvastatin | ①배설 반감기(시간): 13~30 ②대사: CYP3A4 ③복용시간: 제한 없음 |
| Rosuvastatin | ①배설 반감기(시간): 19 ②대사: CYP2C9 ③복용시간: 제한 없음 |
| Fluvastatin | ①배설 반감기(시간): 0.5~3 ②대사: CYP2C9 ③복용시간: 취침전 |
| Lovastatin | ①배설 반감기(시간): 2~4 ②대사: CYP3A4 ③복용시간: 식사 시(조/석) *음식물에 의해 흡수 증가 |
| Pitavastatin | ①배설 반감기(시간): 12 ②대사: CYP2C9, 글루크론산화 ③복용시간: 저녁 |
| Pravastatin | ①배설 반감기(시간): 2~3 ②대사: 설폰화 ③복용시간: 취침전 *음식물에 의해 흡수 감소 |
| Simvastatin | ①배설 반감기(시간): 1~3 ②대사: CYP3A4 ③복용시간: 저녁 |
스타틴에 의한 주된 이상반응에는 근육통[CK(creatine kinase);정상], 근육염/근육병증(CK>정상 상한치), 횡문근 융해증. 스타틴에 의한 자가면역 근육병증, 신규 당뇨병, 아미노산전달효소 상승(정상 상한치x3), 간부전, 횡문근융해증에 의한 이차적 신손상, 중추신경계(기억/인지) 이상 등이 있다. 스타틴 치료 시 근육통은 1~10%, 심각한 부작용인 휭문근융해증은 0.1% 이하로 발생하는 것으로 알려져 있다.
근육독성 등의 이상반응으로 스타틴 요법을 중단한 경우 위험과 스타틴 요법에 다른 이익을 재고하여야 하며 증상 재발 시 ezetimibe로의 전환 등 다음 사항을 고려한다.
| 증상 재발 시 고려사항 |
|---|
| 1. Rosuvastatin: 일일 저용량(2.5~5mg/day) 또는 격일 또는 매주 |
| 2. Atorvastatin: 격일(5~10mg) 또는 10mg 1주 2회 |
| 3. Fluvastatin XL 80mg/day |
| 다양한 스타틴의 다양한 용량에서 증상 재발 시 |
| 1. Ezetimibe 단독요법 10mg/day 또는 Colesevelam 단독요법 |
| 2. Ezetimibe 10mg/day+Colesevelam |
| 비 스타틴 지질저하 약제에 내약하지 않는 경우 |
| 1. 식물 스타놀을 포함하여 생활요법 강화 |
| 2. 정량 가능한 모나콜린(Monacolin)-k 함유량(5~10mg)의 홍국(red yeast rice) 고려 |
▷ 이상지질혈증치료제들의 계열별 특징
| 계열 | 종류 및 특징 |
|---|---|
| Statins (HMG-CoA reductase 억제제) |
▷ 부작용 및 약물상호작용 - 간독성과 근육손상이 대표적인 부작용임 ◈ 두통, 구역, 수면장애, 간 효소와 ALP(Alkaline phosphatase) 증가. Fluconazole(강력한 CYP2C9 및 CYP2C19 억제제이며, 중등도 CYP3A4 억제제), 겜피브로질 또는 사이클로스포린과 병용 시 근염과 횡문근융해증 발생 위험. • 스타틴의 주된 대사 효소: CYP3A4[Atorvastatin, Lovastatin, Simvastatin(3A4, 3A5)] 또는 CYP2C9[Fluvastatin, Pitavastatin, Rosuvastatin(제한적)] ① CYP450 대사억제약물: Fluconazole, 사이클로스포린, 겜피브로질, -navir계 단백질분해효소 억제제 병용 시 근병증 및 흉문근 융해증 위험 증가 → 병용 주의 ② CYP450 대사와 p-당단백질(p-Glycoprotein)을 함께 억제: 베라파밀, 딜티아젬, 아졸계 항진균제, 마크로라이드계 항생제 → 병용 주의 ◈ 심각한 신장애(CLcr < 30 mL/min) 시에도 근염 발생 ◈ lovastatin, atorvastatin, rosuvastatin과 simvastatin은 warfarin의 작용을 증가시키며 rosuvastatin만 제외하고 모두 디곡신의 혈중농도를 증가시킴 - 위의 상호작용은 pravastatin 또는 fluvastatin에서는 관찰되지 않음 |
| 흡수 억제제 | ▷ 에제티미브(ezetimibe) • 간독성 • 스타틴과병용시 transaminase 증가 |
| PCSK9(Proprotein Convertase Subilisin/Kexin type 9) 억제제 | ▷ 알리로쿠맙(alirocumab) • 2주 1회피하주사 • 주사부위 이상반응 주의 ▷ 에볼로쿠맙(evolocumab) • 2주 1회 140 mg 또는 월 1회 420 mg • 주사부위 이상반응 주의 |
| PCSK9 억제 siRNA | ▷ Inclisiran |
| ATP citrate lyase 억제제 | ▷ Bempedoic acid |
| Fibric acid 유도체 (fibrates) | ▷ 페노피브레이트(fenofibrate) • 피부발진, 위장근육통(구역, 복부팽만, 경련) • 혈중 사이클로스포린 농도 감소;사이클로스포린 복용 환자에서 신독성 유발 가능 ▷ 겜피브로질(gemfibrozil) • 와파린작용 증가 • 담즙산 결합제에 의해 흡수 감소 • 겜피브로질의 스타틴제 대사 억제 → 근육증상과 횡문근융해증의 위험이 증가(병용주의 또는 금기) |
| 담즙산흡착제(resins) | ▷ 콜레스티라민(cholestyramine) • 식후 30분이내복용 ▷ 콜레스티폴(Colestipol) • 식후 30분이내복용 ▷ 콜레세벨람(Colesevelam) - 식사와함께 QD 또는BID로 복용 ◈ 답즙산 흡착제 이상반응: • 구역, 복부팽만, 경련과변비 • 간transaminase와 ALP 수치증가 • 지용성비타민, 디곡신, 와파린, 티아지드, β-억제제, 티록신과 페노바르비탈 흡수 저하 |
| 니코틴산(nicotinic acid) | • 음식과 함께 복용 ◈ 이상반응: 간독성, 프로스타글란딘에 의한 피부발적, 두통, 온감각, 소양증, 과다색소침착(특히 간찰영역), 흑색가시세포증, 피부건조, 구역, 구토, 설사, 근염 등 |
| 오메가-3-산에틸에스테르(omega-3-ethyl esters) | ◈ 이상반응: 드물게 트림, 미각도착, 소화불량 ◈ 약물상호작용 • P2Y12 억제제, NSAID, SSRI와 같은 항혈소판제제 작용 증가 • 항응고제 작용 증가 |
| 심바스타틴(simvastatin)/에제티미브(ezetimibe) | • 저녁에 복용 ◈ 약물상호작용 • CYP3A4효소를 강하게 억제하는 약제 병용 금기 |
| 아토르바스타틴(atorvastatin)/ 에제티미브(ezetimibe) | ◈ 약물상호작용 • CYP3A4 효소를 강하게 억제하는 약제를 병용하는 경우에 개시용량을 감량 |
| 로수바스타틴(rosuvastatin)/에제티미브(ezetimibe) | ◈ 약물상호작용 • 약물수송체 OATP1B1과 유출수송체 BCRP 저해제와 병용 시 혈중 농도 증가 |
신부전 환자에서 심혈관질환 발생률은 유의하게 증가한다. 단백질 섭취 제한과 채식 식이를 병행해야 하며 신배설 비율이 비교적 높은 로바스타틴, 피타바스타틴, 프라바스타틴, 로수바스타틴, 심바스타틴, 그리고 1차적으로 신배설되는 피브레이트 제제는 용량을 조절할 필요가 있다.
투석환자의 이상지질혈증 치료로 관상동맥질환 예방에는 아직 근거가 부족하여 권고사항이 없다. 신이식을 받은 환자는 코르티코스테로이드, 사이클로스포린 등의 약제로 인해 지질이상이 야기될 수 있고 이를 스타틴제제로 조절할 수 있으나 사이클로스포린이 CYP3A4를 억제하므로 주의해서 사용해야 한다.
- References
Taher ZA, Taher AA, Radi S. An Update on Dyslipidemia Management and Medications: A Review. Cureus. 2024 Mar 16;16(3):e56255. doi: 10.7759/cureus.56255. PMID: 38623110; PMCID: PMC11017140.
Zhang Y, Chen H, Hong L, Wang H, Li B, Zhang M, Li J, Yang L, Liu F. Inclisiran: a new generation of lipid-lowering siRNA therapeutic. Front Pharmacol. 2023 Oct 13;14:1260921. doi: 10.3389/fphar.2023.1260921. PMID: 37900173; PMCID: PMC10611522.
Masana Marín L, Plana Gil N. Bempedoic acid. Mechanism of action and pharmacokinetic and pharmacodynamic properties. Clin Investig Arterioscler. 2021 May;33 Suppl 1:53-57. English, Spanish. doi: 10.1016/j.arteri.2021.02.012. PMID: 33966814.
Ulrich Laufs et al. Efficacy and Safety of Bempedoic Acid in Patients With Hypercholesterolemia and Statin Intolerance. JOURNAL OF THE AMERICAN HEART ASSOCIATION.Volume 8, Number 7, 2 April 2019.
James McKenney, Niacin for dyslipidemia: Considerations in product selection, American Journal of Health-System Pharmacy, Volume 60, Issue 10, 15 May 2003, Pages 995–1005, https://doi.org/10.1093/ajhp/60.10.995
심미경. 이상지질혈증. 대한약사회 사이버연수원 학술자료(2023년).
Copyright © MediGloPark's All Rights Reserved.
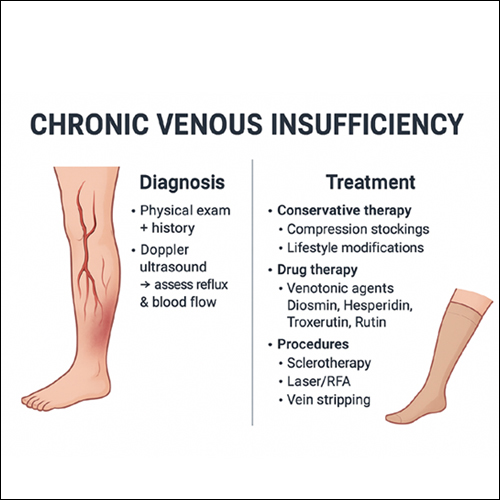
 ▷ 골반울혈증후군(Pelvic Congestion Syndrome, PCS)은 여성에서 만성골반통증의 일반적인 원인으로서 골반정맥의 확장 및 울혈로 인해 만성적인 골반통증과 회음부 통증 및 불편감을 호소한다.
▷ 골반울혈증후군(Pelvic Congestion Syndrome, PCS)은 여성에서 만성골반통증의 일반적인 원인으로서 골반정맥의 확장 및 울혈로 인해 만성적인 골반통증과 회음부 통증 및 불편감을 호소한다.PCS는 보통 출산을 경험한 여성들에서 많이 관찰되며 염증질환의 증거가 없이 6개월 이상 지속되는 만성골반통증이 특징이다.
다양한 강도의 통증이 나타날 수 있지만 주된 증상은 하복부동통과 요통, 성교통, 속발성 월경곤란증, 만성피로증, 과민성 장증후군, 비정상 자궁출혈, 월경불순이나 방광자극 증상으로 인한 절박뇨, 직장 불편감 등이며 월경 전이나 성교 후 또는 피로하거나 장시간 서 있을 때 증상이 심해진다.
비침윤성 영상진단(US, CT, MRI)이 필수적이다. 골반울혈증후군의 치료는 보통 비스테로이드성 항염증제, 메드록시프로게스테론 아세테이트(Medroxyprogesterone acetate) 또는 성선 자극 호르몬 분비 호르몬 작용제[gonadotropin-releasing hormone (GnRH) agonists], 필요 시 하지정맥류로 가는 혈류를 차단하는 절차 등이 있다.
이 약물들이 효과가 없고 통증이 지속적이고 중증인 경우, 하지정맥류로의 혈류를 차단하여 하지정맥류에 혈액이 축적되는 것을 막을 수 있다.
두 가지의 시술이 가능하다. 하나는 정맥 색전술로서 허벅지의 일부 부위를 마취제로 마취시킨 후 약간 절개한 후 얇고 잘 구부러지는 튜브(도관)를 절개 부위를 통해 정맥에 삽입한 후 하지정맥류까지 밀어 넣는다. 도관을 통해 작은 코일, 스폰지 또는 끈적끈적한 액체를 정맥에 넣어 정맥을 차단한다.
다른 방법으로 경화요법은 마찬가지로 도관을 삽입하고 이 도관을 통해 용액을 하지정맥류까지 주입한다. 이 용액이 정맥을 차단한다. 혈액이 골반 내 하지정맥류로 더 이상 흐르지 않으면 대개 통증이 줄어든다.
그밖에 불안과 우울증 관리를 위한 정신심리요법과 행동통증관리도 필요하다.
- References
Kashef, E., Evans, E., Patel, N. et al. Pelvic venous congestion syndrome: female venous congestive syndromes and endovascular treatment options. CVIR Endovasc 6, 25 (2023). https://doi.org/10.1186/s42155-023-00365-y
Ignacio EA, Dua R, Sarin S, Harper AS, Yim D, Mathur V, Venbrux AC. Pelvic congestion syndrome: diagnosis and treatment. Semin Intervent Radiol. 2008 Dec;25(4):361-8. doi: 10.1055/s-0028-1102998. PMID: 21326577; PMCID: PMC3036528.
JoAnn V. Pinkerton. Pelvic Congestion Syndrome. MSD Manual. 2023. https://www.msdmanuals.com
Copyright © MediGloPark's All Rights Reserved.
 PDRN(polydeoxyribonucleotide)은 분자량 50~1500kDa의 DNA 단편으로 이루어져 있다. 연어(Oncorhynchus mykiss: salmon trout 또는 Oncorhynchus keta: chum salmon)의 정자세포에서 주로 추출된다. 여러 전임상 및 임상연구에서 PDRN은 항염작용,
세포사멸억제작용, 항골다공증작용, 멜라닌생성억제작용, 이질통증(allodynia)억제작용, 골괴사억제작용, 골재생작용, 조직손상예방작용, 항궤양작용, 상처치유작용 등을 나타내는 것으로 보고되었으며, 이는 아데노신(Adenosine) A2A 수용체와 회수 경로(salvage pathway)의 활성화에 의한 것으로 알려져 있다.
PDRN(polydeoxyribonucleotide)은 분자량 50~1500kDa의 DNA 단편으로 이루어져 있다. 연어(Oncorhynchus mykiss: salmon trout 또는 Oncorhynchus keta: chum salmon)의 정자세포에서 주로 추출된다. 여러 전임상 및 임상연구에서 PDRN은 항염작용,
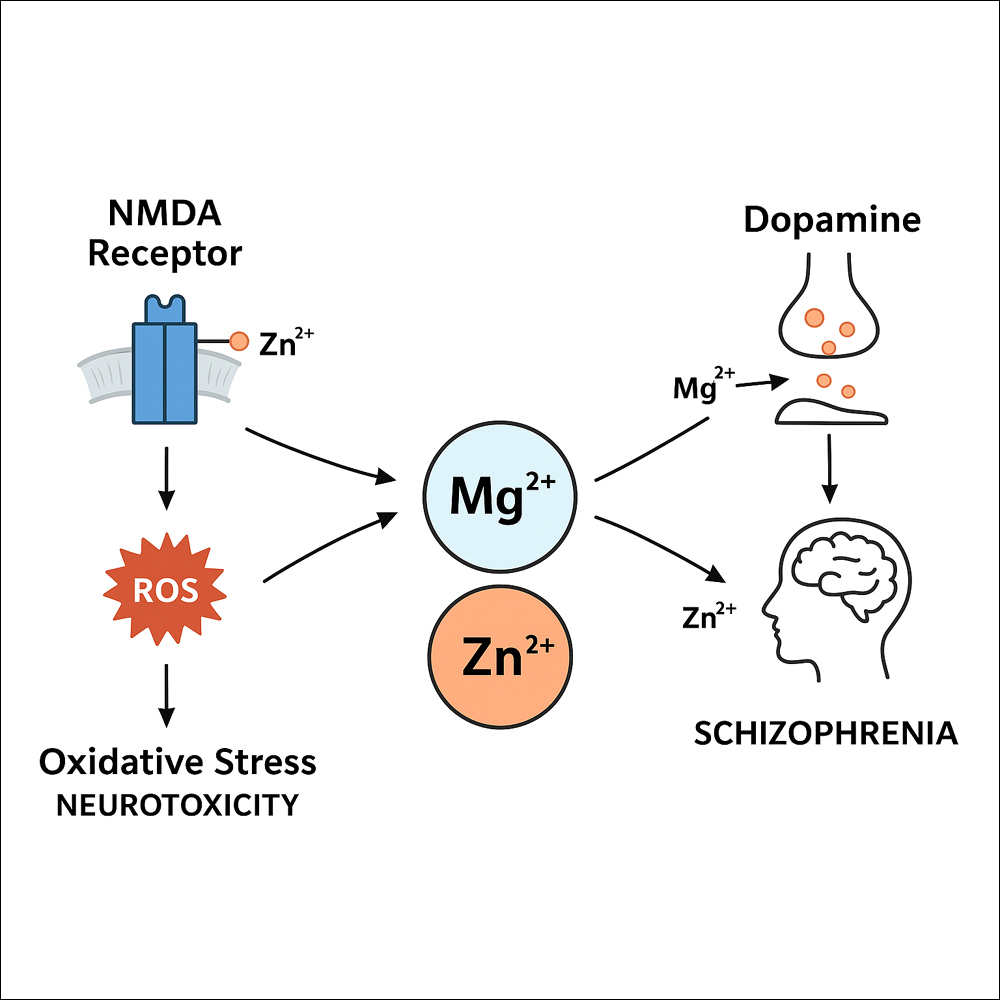
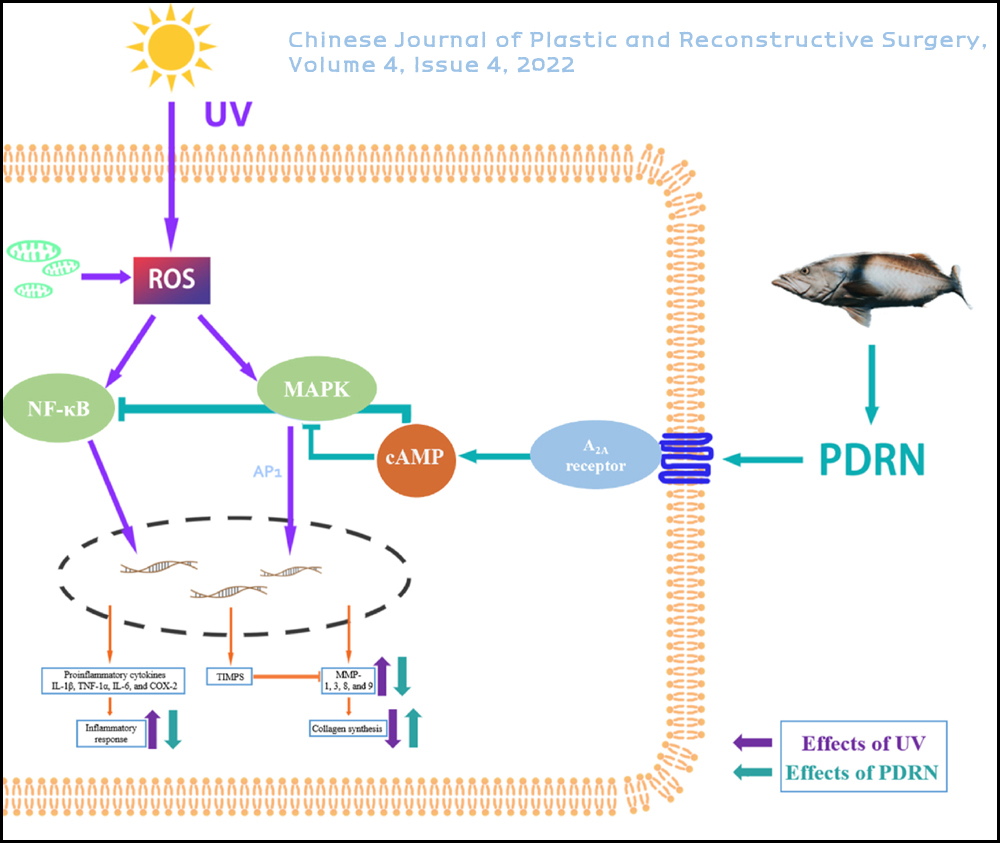
세포사멸억제작용, 항골다공증작용, 멜라닌생성억제작용, 이질통증(allodynia)억제작용, 골괴사억제작용, 골재생작용, 조직손상예방작용, 항궤양작용, 상처치유작용 등을 나타내는 것으로 보고되었으며, 이는 아데노신(Adenosine) A2A 수용체와 회수 경로(salvage pathway)의 활성화에 의한 것으로 알려져 있다. Adenosine 수용체는 활성산소(Reactive Oxygen Species, ROS) 관련 질환 관리의 확실한 타겟으로 알려져 있다. 특히 Adenosine A2A 수용체 활성화에 의해 염증반응조절, 세포자멸사 과정의 조절, 조직복구 및 치유 향상 등이 이루어지며, 활성산소에 의해 촉진되는 NF-kB와 MAPK(mitogen-activated protein kinases) 신호경로도 A2A 수용체에 의해 억제된다.
피부노화의 주된 내부적 요인은 활성산소로서 미토콘드리아의 호기성 대사 전자전달계의 부산물로서 만들어진다. 활성산소에 기인한 내부적 노화과정에는 진피의 섬유아세포 수의 감소, 세포외 기질 단백분해와 여러 생물활성분자들의 변화에 관여하는 MMPs(matrix metalloproteinases) 발현 증가, ECM(extracellular matrix)의 콜라겐과 엘라스틴 합성능 감소 등이 포함된다.
PDRN은 혈관신생(angiogenesis), 세포활성, 콜라겐 합성, 연조직 재생, 스킨 프라이밍(skin priming), 피부활성화 등을 촉진하며 과색소침착(hyperpigmentation) 치료에 사용될 수 있다.
| PDRN 특성 |
|---|
| ∙ 혈관신생 ∙ 세포활성 촉진 ∙ 콜라겐 합성 ∙ 과색소침착 치료 ∙ 연조직 재생 ∙ 스킨 프라이밍 ∙ 피부 활성화 ∙ 항염 ∙ 흉터 감소 ∙ 항노화 |
- References
Aawrish Khan, Guobao Wang, Feng Zhou, Lunli Gong, Jun Zhang, Lili Qi, Haiyan Cui, Polydeoxyribonucleotide: A promising skin anti-aging agent, Chinese Journal of Plastic and Reconstructive Surgery, Volume 4, Issue 4, 2022, Pages 187-193.
Squadrito F, Bitto A, Irrera N, Pizzino G, Pallio G, Minutoli L, Altavilla D. Pharmacological Activity and Clinical Use of PDRN. Front Pharmacol. 2017 Apr 26;8:224. doi: 10.3389/fphar.2017.00224. Erratum in: Front Pharmacol. 2022 Nov 21;13:1073510.
Copyright © MediGloPark's All Rights Reserved.
 목은 심리적으로 가장 위협을 느끼는 부분에 속하므로 목에 이물감이 있으면 신경이 많이 쓰인다. 내시경 검사 등 진료에서 역류성식도염과 같은 병변이 없는 데도 목에 이물감을 느낀다면 대부분 매핵기(인두신경증 Globus Pharyngeus)인 경우가 많다.
목은 심리적으로 가장 위협을 느끼는 부분에 속하므로 목에 이물감이 있으면 신경이 많이 쓰인다. 내시경 검사 등 진료에서 역류성식도염과 같은 병변이 없는 데도 목에 이물감을 느낀다면 대부분 매핵기(인두신경증 Globus Pharyngeus)인 경우가 많다.매핵기는 가래가 목에 걸려 있는 느낌이지만 실제로 가래가 나오는 경우는 드물고, 억지로 배출해보면 소량의 끈적한 흰색 점액인 경우가 일반적이다. 매핵기 증상자가 평상 시 목이 답답하여 '큭큭'거리며 가래를 뱉고자 하면 자극에 의해 오히려 없던 염증도 생길 수 있으므로 자제하고 소량의 물을 자주 섭취하여 증상을 감소시키는 것이 좋다.
동의보감 내경편에는 매핵기를 '治痰氣鬱結窒碍於咽喉之間咯之不出嚥之不下謂之梅核氣'(담의 기운이 울결되어 인후를 막아 뱉어도 나오지 않고 삼켜도 넘어가지 않는 것을 매핵기라고 한다)로 논하고 있다. 일반적으로 반하후박탕(半夏厚朴湯), 가미사칠탕(加味四七湯) 등이 많이 사용되나 매핵기가 기허증자의 신경과민이나 스트레스로 발생하는 경우가 많으므로 증상자의 체질에 따른 면밀한 처방구성을 하여야 빠른 치료를 기대할 수 있다. 특히 만성 매핵기 증상자의 경우 '큭큭'거리는 습관으로 염증이 발생한 경우 형개, 연교 등 소염작용이 있는 약제들과 울체된 기를 소통시키는 약제들을 함께 사용하여야 효과를 볼 수 있다.
| 매핵기의 병인(病因)과 치법(治法) |
|---|
| 병인(病因) | 치법(治法) |
|---|---|
| 지나친 喜 또는 怒로 熱이 몰리고 뭉쳐 痰盛鬱結[고금의감(古今醫鑑)] | 가미사칠탕(加味四七湯), 가미이진탕(加味二陳湯) |
| 병은 七氣에서 발생하며 氣가 몰리면 痰이 생기고, 痰이 盛하면 氣가 더욱 몰린다. | 痰을 없애야 氣가 고르게 됨: 칠기탕[七氣湯: 氣虛로 痰이 鬱結되어 가슴과 명치 밑이 단단하고 아픈 것을 主治(東醫寶鑑)] |
| 기울(氣鬱)로 생긴 경계증(驚悸症) | 加味四七湯 |
| 정충(炡沖)은 오래된 驚悸症에 의해 발생. | 氣鬱이 있으면: 加味四七湯+죽력(竹瀝), 생강즙(生薑汁) |
| 기담(氣痰): 七情鬱結로 목구멍에 痰이 막혀 梅核氣가 있으며 가슴이 더부룩하고 답답한것 | 加味四七湯, 加味二陳湯 |
| 계심통(悸心痛): 七情으로 炡沖驚悸症이 생겨서 가슴이 아픈 것 | 四七湯, 加味四七湯, 七氣湯 |
| 기수(氣嗽): 七氣에 상하여 생긴 기침. 담연(痰涎)이 뭉쳐 생긴 梅核氣 | 加味四七湯 |
| 처방과 약제 |
|---|
| 처방 | 약제 |
|---|---|
| 加味四七湯 | 동의보감(東醫寶鑑): 반하(半夏: 법제한 것) · 진피(陳皮) · 적복령(赤茯苓) 각 4g, 신국(神麴: 덖은 것) · 지실(枳實) · 천남성(天南星: 구운 것) 각 2.8g, 청피(靑皮) · 후박(厚朴) · 자소엽(紫蘇葉) · 빈랑(檳榔) · 사인(砂仁) 각 2g, 백두구(白豆蔲) · 익지인(益智仁) 각 1.2g, 생강(生薑) 5쪽. |
| 七氣湯 | 동의보감(東醫寶鑑): 반하[(半夏: 법제한 것):主藥] 12g, 인삼(人參) · 육계[(肉桂): 佐藥] · 자감초(炙甘草) 각 2.8g, 생강(生薑) 3쪽. |
| 四七湯 | 동의보감(東醫寶鑑): 반하(半夏: 법제한 것) 8g, 적복령(赤茯苓) 6.4g, 후박(厚朴: 법제한 것) 4.8g, 자소엽(紫蘇葉) 3.2g, 생강(生薑) 7쪽, 대조(大棗) 2개. |
| 半夏厚朴湯 | 반하, 후박, 소엽, 생강, 복령 |
| 加味二陳湯 | 반하(半夏: 법제한 것) · 진피(陳皮) · 적복령(赤茯苓) · 지각(枳殼) · 길경(桔梗) 각 4g, 황금(黃芩) · 치자(梔子: 덖은 것) 각 2.8g, 자소자(紫蘇子) · 백두구(白豆蔲) · 감초(甘草) 각 2g, 생강(生薑) 3쪽. |
- References
박성수, 염태환. 現代漢方講座(全四券). 행림출판, 1992.
한의학대사전 편찬위원회. 한의학대사전. 도서출판 정담, 2001.
정흥식, 이용태. 梅核氣의 形象醫學的 考察 Review on the Globus Hystericus in View of Hyungsang Medicine. 동의생리병리학회지 20권, 3호. 2006.
황은영, 서진우, 서현욱, 정선용, 김종우. 梅核氣로 인해 음식을 삼키지 못하는 전환장애 환자 치험 1례 A Case Report of Conversion Disorder Patient with Globus Hystericus and Swallowing difficulty. 동의신경정신과 학회지 J. of Oriental Neuropsychiatry Vol. 20. No. 2, 2009
Copyright © MediGloPark's All Rights Reserved.
 위염은 특정 원인에 의해 발생하는 경우가 많으며, 비스테로이드성 소염진통제(NSAIDs: nonsteroidal antiinflammatory drugs)나 음주로 야기된 급성 위염은 원인이 된 소염진통제 사용의 중지, 금주로 개선될 수도 있다.
위염은 특정 원인에 의해 발생하는 경우가 많으며, 비스테로이드성 소염진통제(NSAIDs: nonsteroidal antiinflammatory drugs)나 음주로 야기된 급성 위염은 원인이 된 소염진통제 사용의 중지, 금주로 개선될 수도 있다.위염 치료에 사용되는 약제들은 주로 헬리코박터균(Helicobacter pylori) 제균을 위한 항생제, 위산 생성 차단제, 제산제 등이다.
위염의 효과적인 치료를 위해서는 생활습관의 변화가 필요하다. 술은 위점막에 자극을 줄 수 있으므로 금주하여야 하며, 아스피린이나 이부프로펜과 같은 비스테로이드성 소염진통제는 위염의 위험성을 높이므로 환자는 아세트아미노펜 제제로 대체할 수 있는지 의사 또는 약사와 상의하여야 한다.
장기간 헬리코박터균 감염은 만성위염의 원인이 될 수 있으며, 드물지만 기생충 감염과 진균 감염에 의한 급성 또는 만성위염도 발생할 수 있다.
자가면역질환도 만성염증을 유발할 수 있다. 자가면역질환 환자에서 면역시스템이 염증이 있는 체내 세포를 잘못 공격하여 만성 자가면역성 위염이 발생할 수 있다. 또는 드물지만 다른 자가면역질환의 부작용으로서 위염이 발생하는 경우도 있다.
대수술, 외상 또는 심각한 질병에 의한 2차적 급성 위염이 발생할 수 있다. 심각한 생리학적 스트레스 상황에서는 뇌, 심장, 폐 등 생명유지와 더욱 밀접한 장기(vital organs)로 혈액을 보내기 위해 소화기계에 대한 혈액공급이 감소하게 되어 위벽의 방어력이 낮아져 위염이 발생할 위험성이 증가한다.
그 외 방사선치료, 화학요법, 담즙역류 등도 위염의 원인이 될 수 있다.
위염치료에 가장 빈번하게 사용되는 약제 가운데 하나인 양성자펌프억제제(PPIs: proton pump inhibitors)는 고관절 골절, 폐렴, 장내 세균감염(Clostridium difficile) 및 비타민B12 결핍증 등의 부작용을 발생시킬 수 있다. 또한 대부분의 PPI는 항혈소판제인 클로피도그렐(clopidogrel)의 활성화 효소를 억제하므로 약물상호작용에 주의하여야 한다. Clopidogrel은 간에서 CYP2C19과 CYP3A4에 의해 활성형으로 전환된다. 단, PPI 가운데 덱스란소프라졸(dexlansoprazole), 판토프라졸(pantoprazole) 등은 클로피도그렐의 활성화와 항혈소판 작용에 임상적으로 중요한 영향은 없는 것으로 알려져 있다.
PPI는 산에 의해 활성화되는 전구약물(prodrug)이다. 활성화된 PPI는 위벽세포내 H+/K+-ATPase에 이황화 결합(disulfide bond)을 통한 공유결합을 한다.
가장 먼저 시판된 PPI인 Omeprazole을 시작으로 Pantoprazole, Lansoprazole 및 Rabeprazole 등이 사용되고 있다. PPI 대사는 주로 CYP2C19과 CYP3A4에 의해 이루어진다. S-omeprazole은 CYP2C19에 비교적 영향을 덜 받으므로 위내 pH 조절효과가 더 우수하다. 유사하게 R-lansoprazole이 약물활성을 증가시킬 목적으로 개발되었다. 방출 지연성 제제(delayed release formulation)는 약물대사면에서도 유리하며 혈중 R-lansoprazole의 농도를 장시간 효과적으로 유지시킬 수 있다. Dexlansoprazole은 여러 PPI 가운데 가장 우수한 위내 pH 조절 효과를 나타내는 것 중의 하나이다.
▷ PPIs 종류와 특징(J Neurogastroenterol Motil. 2016)
| PPIs | 특징 |
|---|---|
| Dexlansoprazole | ∙ R-enantiomer of lansoprazole ∙ Dual delayed release formulation ∙ Dual-peaked pharmacokinetic profile ∙ 24-hour symptom control ∙ Administration without regard to food ∙ Hepatic metabolism: CYP2C19, CYP3A4 ∙ Weak inhibition of CYP2C19 ∙ No clinically important effect on exposure to the active metabolite of clopidogrel or clopidogrel-induced platelet inhibition |
| Esomeprazole | ∙ S-isomer of omeprazole ∙ Low initial oral bioavailability increasing over time ∙ Hepatic metabolism: CYP2C19, CYP3A4 ∙ Potent inhibition of CYP2C19 ∙ Possible interaction with clopidogrel via CYP2C19 ∙ Delayed absorption with food |
| Lansoprazole | ∙ Constant high bioavailability at therapeutic doses ∙ Rapid onset of maximal acid suppression ∙ Delayed absorption with food ∙ Concurrent antacid therapy reduces bioavailability ∙ Increased theophylline metabolism ∙ Hepatic metabolism: CYP2C19, CYP3A4 ∙ Weak inhibition of CYP2C19 ∙ No clinically important effect on exposure to the active metabolite of clopidogrel or clopidogrel-induced platelet inhibition |
| Omeprazole | ∙ Low initial oral bioavailability (35–40%) increasing to ~65% over time ∙ Dose-dependent kinetics ∙ Delayed absorption with food ∙ Hepatic metabolism: CYP2C19 ∙ Potent inhibition of CYP2C19 ∙ Interaction with clopidogrel via CYP2C19 |
| Pantoprazole | ∙ Constant bioavailability (~77%) ∙ Delayed absorption with food ∙ Hepatic metabolism: CYP2C19, CYP3A4 ∙ Weak inhibition of CYP2C19 ∙ No clinically important effect on exposure to the active metabolite of clopidogrel or clopidogrel-induced platelet inhibition |
Vonoprazan, Tegoprazan [(S)-4-((5,7-difluorochroman-4-yl)oxy)-N,N,2-trimethyl-1H-benzo[d]imidazole-6-carboxamide] 및 Fexuprazan은 위내 H+/K+-ATPase를 매우 선택적으로 억제하는 칼륨경쟁적위산분비억제제(P-CAB: Potassium-Competitive Acid Blocker)들이다.
Vonoprazan, Tegoprazan, 그리고 Fexuprazan은 아스피린과의 병용연구에서 약력학 및 약동학적으로 유의성 있는 약물상호작용이 나타나지 않아 아스피린에 의한 위장관 합병증 예방에 병용이 가능한 것으로 보고되었다.
Vonoprazan의 약물상호작용에 대한 연구에서 Vonoprazan이 CYP3A4, CYP2C9, CYP2D6 및 CYP2B6를 억제하는 것으로 나타나 cytochrome P450 기질 약제의 병용에 주의가 필요하다.
Tegoprazan은 주로 CYP3A4에 의해 대사되며, CYP1A2, CYP2C9 및 CYP2C19은 유의성 있게 억제하지 않는 것으로 알려져 있다. Tegoprazan과 일반적으로 많이 사용되는 진통제인 Naproxen, Aceclofenac, Celecoxib 등과의 약동학적 상호작용에 관한 연구에서 Tegoprazan과 병용 시 Aceclofenac 또는 Celecoxib Cmax의 변화가 관찰되었으며 이는 주로 Tegoprazan의 약력학적 작용에 의한 것으로 평가되었다. NSAIDs와의 병용 투여에 의한 Tegoprazan의 약동학적 영향은 관찰되지 않았다.
Aceclofenac은 전구약물(prodrug)으로서 위장관에서 신속하게 흡수되며 활성형인 Diclofenac이 COX 효소를 억제한다. Diclofenac은 대부분 CYP2C9에 의해 hydroxylation되어 대부분 소변으로 배설된다. Cerecoxib도 신속하게 흡수되는데, Al 및 Mg 함유 제산제와 병용 시 Cmax는 37%, AUC는 10% 감소하는 것으로 보고되었다. 그러나 음식에 의한 영향을 고려하여 투여하지는 않는다. Celecoxib는 주로 CYP2C9에 의해 대사되고 배설되며 일부는 CYP3A4에 의해 대사된다.
Fexuprazan은 PPI와 대조적으로 CYP2C19에 거의 영향을 받지 않아 장시간 효과를 나타내며, 비산성 조건에서도 활성화되며, 작용 개시가 빠르다. 반면에, Fexuprazan은 CYP3A4에 의해 주로 대사되므로 CYP3A4 매개성 약물상호작용에 주의하여야 한다. Fexuprazan과 아스피린과의 병용투여 시 약물상호작용에 관한 연구에서 아스피린의 혈소판 응집 억제작용은 Fexuprazan 병용투여에 의해 의미있는 영향을 받지 않는 것으로 나타났다. 또한 아스피린 병용투여에 의해 Fexuprazan의 전신적 노출은 20%까지 감소되는 것으로 나타났으나 임상적 유의성은 없는 것으로 평가되어 Fexuprazan이 아스피린 유도성 위장관 합병증 예방 잠재력이 있는 것으로 보고되었다.
H2 수용체 차단제[histamine-2 receptor antagonists (H2RAs)]는 GERD(gastroesophageal reflux disease), 위십이지장궤양, 위산과다 등에 사용되며, 오프라벨 사용으로서 스트레스성 위궤양 예방, 식도염, 위염, 위장관 출혈, 두드러기에 사용할 수 있다. H2RAs는 Helicobacter pylori 제균처방에 포함되기도 한다.
FDA 승인 H2RAs는 Famotidine, Cimetidinr, Nizatidine이다.
H2RAs는 위벽세포의 H2 수용체에 대한 경쟁적 길항제로서 H2 수용체에 가역적으로 결합하여 내생적 히스타민의 결합과 작용을 저해하는 기전으로 위산분비를 감소시킨다. 음식을 섭취하면 가스트린은 히스타민을 합성하고 분비하는 장크롬친화성유사세포(enterochromaffin-like cells)로 부터 히스타민 분비를 촉진하고 히스타민이 위벽세포의 히스타민 H2 수용체에 결합하여 위산분비를 야기한다.
H2RAs는 cytochrome P450 시스템에 의해 간에서 대사된다. 특이적으로 Cimetidine은 CYP1A2, CYP2C9, 그리고 CYP2D6를 저해하므로 심각한 약물상호작용을 발생시킬 수 있다. Theophylline, SSRI(selective serotonin reuptake inhibitors), 또는 Warfarin과 같이 CYP450 효소에 의해 대사되는 약제들과 Cimetidine을 병용하면 안된다.
H2RAs와 PPIs의 과도한 사용으로 철결핍성 빈혈이 발생할 수 있으며, PPIs와 H2RAs를 병용에 관한 사례대조군연구에서는 병용 시 골다공증성 골절 위험성이 증가하는 것으로 나타났다.
- References
Goh KL, Choi MG, Hsu PI, Chun HJ, Mahachai V, Kachintorn U, Leelakusolvong S, Kim N, Rani AA, Wong BC, Wu J, Chiu CT, Shetty V, Bocobo JC, Chan MM, Lin JT. Pharmacological and Safety Profile of Dexlansoprazole: A New Proton Pump Inhibitor - Implications for Treatment of Gastroesophageal Reflux Disease in the Asia Pacific Region. J Neurogastroenterol Motil. 2016 Jul 30;22(3):355-66. doi: 10.5056/jnm15150. PMID: 26932927; PMCID: PMC4930293.
Shin JM, Kim N. Pharmacokinetics and pharmacodynamics of the proton pump inhibitors. J Neurogastroenterol Motil. 2013 Jan;19(1):25-35. doi: 10.5056/jnm.2013.19.1.25. Epub 2013 Jan 8. PMID: 23350044; PMCID: PMC3548122.
Takahashi N, Take Y. Tegoprazan, a Novel Potassium-Competitive Acid Blocker to Control Gastric Acid Secretion and Motility. J Pharmacol Exp Ther. 2018 Feb;364(2):275-286. doi: 10.1124/jpet.117.244202. Epub 2017 Nov 27. PMID: 29180359.
Oh J, Yang E, Jang IJ, Lee H, Yoo H, Chung JY, Lee S, Oh J. Pharmacodynamic and Pharmacokinetic Drug Interactions between Fexuprazan, a Novel Potassium-Competitive Inhibitor, and Aspirin, in Healthy Subjects. Pharmaceutics. 2023 Feb 7;15(2):549. doi: 10.3390/pharmaceutics15020549. PMID: 36839870; PMCID: PMC9958674.
Wang Y, Wang C, Wang S, Zhou Q, Dai D, Shi J, Xu X, Luo Q. Cytochrome P450-Based Drug-Drug Interactions of Vonoprazan In Vitro and In Vivo. Front Pharmacol. 2020 Feb 14;11:53. doi: 10.3389/fphar.2020.00053. PMID: 32116727; PMCID: PMC7033572.
Seol Ju Moon, Naree Shin, MinJa Kang, Bongtae Kim, Min-Gul Kim, Pharmacokinetic Interactions Between Tegoprazan and Naproxen, Aceclofenac, and Celecoxib in Healthy Korean Male Subjects, Clinical Therapeutics, Volume 44, Issue 7, 2022, Pages 930-944.e1, ISSN 0149-2918, https://doi.org/10.1016/j.clinthera.2022.06.002.
Nugent CC, Falkson SR, Terrell JM. H2 Blockers. [Updated 2024 Aug 11]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK525994/
Copyright © MediGloPark's All Rights Reserved.
 목은 심리적으로 가장 위협을 느끼는 부분에 속하므로 목에 이물감이 있으면 신경이 많이 쓰인다. 내시경 검사 등 진료에서 역류성식도염과 같은 병변이 없는 데도 목에 이물감을 느낀다면 대부분 매핵기인 경우가 많다.
목은 심리적으로 가장 위협을 느끼는 부분에 속하므로 목에 이물감이 있으면 신경이 많이 쓰인다. 내시경 검사 등 진료에서 역류성식도염과 같은 병변이 없는 데도 목에 이물감을 느낀다면 대부분 매핵기인 경우가 많다.매핵기는 가래가 목에 걸려 있는 느낌이지만 실제로 가래가 나오는 경우는 드물고, 억지로 배출해보면 소량의 끈적한 흰색 점액인 경우가 일반적이다. 매핵기 증상자가 평상 시 목이 답답하여 '큭큭'거리며 가래를 뱉고자 하면 자극에 의해 오히려 없던 염증도 생길 수 있으므로 자제하고 소량의 물을 자주 섭취하여 증상을 감소시키는 것이 좋다.
동의보감 내경편에는 매핵기를 '治痰氣鬱結窒碍於咽喉之間咯之不出嚥之不下謂之梅核氣'로 논하고 있다. 일반적으로 반하후박탕(半夏厚朴湯: 반하, 후박, 소엽, 생강, 복령) 등이 많이 사용되나 매핵기가 기허증자의 신경과민이나 스트레스로 발생하는 경우가 많으므로 증상자의 체질에 따른 면밀한 처방구성을 하여야 빠른 치료를 기대할 수 있다. 특히 만성 매핵기 증상자의 경우 '큭큭'거리는 습관으로 염증이 발생한 경우 형개, 연교 등 소염작용이 있는 약제들과 울체된 기를 소통시키는 약제들을 함께 사용하여야 효과를 볼 수 있다.
| 증상 | 치법(治法) |
|---|---|
| 칠기(七氣) | 칠기탕[(七氣湯) 주약: 반하, 좌약: 육계] 담(痰)을 제거하여 기(氣)를 고르게 한다. |
| 기통(氣痛) | |
GlobusPharyngeus
▷ GlobusPharyngeus
| GlobusPharyngeus | GlobusPharyngeus |
|---|---|
| GlobusPharyngeus | GlobusPharyngeus |
| GlobusPharyngeus | GlobusPharyngeus |
| GlobusPharyngeus | GlobusPharyngeus |
EGlobusPharyngeus
- References
정흥식, 이용태. 梅核氣의 形象醫學的 考察 Review on the Globus Hystericus in View of Hyungsang Medicine. 동의생리병리학회지 20권, 3호. 2006.
황은영, 서진우, 서현욱, 정선용, 김종우. 梅核氣로 인해 음식을 삼키지 못하는 전환장애 환자 치험 1례 A Case Report of Conversion Disorder Patient with Globus Hystericus and Swallowing difficulty. 동의신경정신과 학회지 J. of Oriental Neuropsychiatry Vol. 20. No. 2, 2009
Copyright © MediGloPark's All Rights Reserved.
 GlobusPharyngeus
GlobusPharyngeus
GlobusPharyngeus
| GlobusPharyngeus |
|---|
| GlobusPharyngeus |
| GlobusPharyngeus |
GlobusPharyngeus
▷ GlobusPharyngeus
| GlobusPharyngeus | GlobusPharyngeus |
|---|---|
| GlobusPharyngeus | GlobusPharyngeus |
| GlobusPharyngeus | GlobusPharyngeus |
| GlobusPharyngeus | GlobusPharyngeus |
EGlobusPharyngeus
- References
GlobusPharyngeus
Copyright © MediGloPark's All Rights Reserved.
 만성적 면역성혈소판감소증(immune thrombocytopenia, ITP)은 특징적으로 혈소판 수치가 12개월 이상 낮게 나타나는 일종의 자가면역질환이다. 자반증 등의 증상은 없을 수도 있지만 중증 환자의 경우 사망의 위험성이 증가하므로
적극적인 치료가 필요하다.
만성적 면역성혈소판감소증(immune thrombocytopenia, ITP)은 특징적으로 혈소판 수치가 12개월 이상 낮게 나타나는 일종의 자가면역질환이다. 자반증 등의 증상은 없을 수도 있지만 중증 환자의 경우 사망의 위험성이 증가하므로
적극적인 치료가 필요하다.
엘트롬보팍(Eltrombopag: Revolade®, Promacta®)은 만성적 면역성혈소판감소증과 같은 혈액질환 환자에서 혈소판감소증(Thrombocytopenia) 치료를 목적으로 사용된다.
비장절제술(splenectomy) 후에 사용하기도 하며 스테로이드나 면역글로블린 등 다른 약의 효과가 충분하지 않을 때 사용된다. 엘트롬보팍은 인터페론 치료와 더불어 만성 C형 간염 환자의 혈소판감소증 치료를 위해 사용하기도 한다.
엘트롬보팍은 골수를 자극하여 더 많은 혈소판을 생성하도록 하는 작용을 한다.
일부 약들은 병용하지 않아야 하지만, 필요한 경우 약물상호작용의 위험성에도 불구하고 의사의 약용량 조정 및 모니터링 하에 함께 사용할 수도 있다.
엘트롬보팍 복용 시 칼슘이 많이 함유되어 있는 식품이나 유제품, 음주, 흡연 등은 피하는 것이 좋다. 그렇지 못할 경우는 의사와 상의하여 음식, 음주, 흡연 등에 대한 특별한 지시를 받아야 한다.
| 엘트롬보팍 복용 시 회피 |
|---|
| 칼슘이 풍부한 식품, 유제품: 엘트롬보팍의 효과 감소 |
| 술, 담배 |
ITP 환자의 경우 우선적으로 스테로이드와 면역글로불린주사 치료를 하며 치료가 충분하지 않을 경우 로미플로스팀(Romiprostim)과 엘트롬보팍(Eltrombopag)과 같은 혈소판 수용체 작용제(ThromboPOietin-Receptor Agonist, TPO-RA)가 사용된다.
▷ 엘트롬보팍 복용 시 주의하여야 할 약제
| 기준 | 약제 |
|---|---|
| Not recommended | Elagolix, Grazoprevir |
| Usually not recommended | Alpelisib, Aluminum, Atogepant, Atorvastatin, Axitinib, Bosentan, Calcium, Cerivastatin, Docetaxel, Eluxadoline, Exemestane, Fexofenadine, Fluvastatin, Glecaprevir, Glyburide, Irinotecan, Iron, Letermovir, Lovastatin, Magnesium, Methotrexate, Momelotinib, Nateglinide, Ozanimod, Paclitaxel, Paritaprevir, Pexidartinib, Pitavastatin, Pixantrone, Pravastatin, Repaglinide, Resmetirom, Revefenacin, Rosuvastatin, Selenium, Selexipag, Simvastatin, Sofosbuvir, Sulfasalazine, Sunitinib, Talazoparib, Tenofovir Alafenamide, Teriflunomide, Topotecan, Ubrogepant, Valsartan, Voxilaprevir, Zinc |
| May increase the risk of side effects but can be used | Lopinavir |
Eltrombopag 복용 시 칼슘이 풍부한 식품 또는 Al, Mg 등을 주성분으로 하는 제산제와 병용 시 Eltrombopag의 전신적 효과가 감소하므로 주의가 필요하다.
- References
Cheng G. Eltrombopag, a thrombopoietin- receptor agonist in the treatment of adult chronic immune thrombocytopenia: a review of the efficacy and safety profile. Ther Adv Hematol. 2012 Jun;3(3):155-64. doi: 10.1177/2040620712442525. PMID: 23556122; PMCID: PMC3573439.
Lozano ML, Segú-Vergés C, Coma M, Álvarez-Roman MT, González-Porras JR, Gutiérrez L, Valcárcel D, Butta N. Elucidating the Mechanism of Action of the Attributed Immunomodulatory Role of Eltrombopag in Primary Immune Thrombocytopenia: An In Silico Approach. Int J Mol Sci. 2021 Jun 27;22(13):6907. doi: 10.3390/ijms22136907. PMID: 34199099; PMCID: PMC8269123.
Williams DD, Peng B, Bailey CK, Wire MB, Deng Y, Park JW, Collins DA, Kapsi SG, Jenkins JM. Effects of food and antacids on the pharmacokinetics of eltrombopag in healthy adult subjects: two single-dose, open-label, randomized-sequence, crossover studies. Clin Ther. 2009 Apr;31(4):764-76. doi: 10.1016/j.clinthera.2009.04.010. PMID: 19446149.
Copyright © MediGloPark's All Rights Reserved.
 역류성 위식도질환(GERD, gastroesophageal reflux disease) 치료에는 생활습관의 변화, 약물치료, 그리고 드물지만 수술이 필요한 경우도 있다.
역류성 위식도질환(GERD, gastroesophageal reflux disease) 치료에는 생활습관의 변화, 약물치료, 그리고 드물지만 수술이 필요한 경우도 있다.생활습관의 수정만으로도 증상을 감소시킬 수 있으며 과체중이거나 비만인 사람은 체중감소가 필요하다.
약물치료로는 약국에서도 구입할 수 있는 제산제와 파모티딘과 같은 H2 차단제, 그리고 처방이 필요한 위산억제제(proton pump inhibitor 또는 potassium competitive acid blocker 등 )가 주로 사용되며 위장관운동조절제(Mosapride 등)도 도움이 된다.
그 외 알긴산나트륨(sodium alginate)액제 등이 증상 경감을 위해 사용되기도 한다.
| 역류성 식도질환 치료를 위한 습관 |
|---|
| 1. 음식은 소량씩 여러번으로 나누어 섭취한다. 위에 음식물이 가득하면 역류 위험성이 증가한다. |
| 2. 역류 유발 식품을 피한다. ▷ 역류 유발 식품: 박하, 지방질 음식, 매운 음식, 토마토, 양파, 마늘, 커피, 초콜릿, 술 등 |
| 3. 탄산음료 회피: 트림 시 위산 역류 |
| 4. 식후 서 있거나 앉아 있기: 식후 3시간 후에 취침 |
| 5. 식후 격렬한 운동을 피한다. |
| 6. 하체보다 상체를 15~20cm(머리 기준) 높게 하여 수면을 취한다. |
| 7. 체중 감량: 체중 증가에 의해 하부 식도 괄약근을 지지하는 근육이 약화되어 괄약근 닫힘 압력이 감소함 |
| 8. 금연: 니코틴에 의한 하부 식도 괄약근의 약화 |
| 9. 약물검토 ▷ 식도 괄약근 약화 약물: 에스트로겐, 삼환계 항우울제, 소염진통제 등 ▷ 식도 자극 약물: 골 흡수 억제제와 같은 일부 골다공증약(Bisphosphonates: alendronate, ibandronate, risedronate 등) |
- References
Richter JE, Peura D, Benjamin SB, Joelsson B, Whipple J. Efficacy of Omeprazole for the Treatment of Symptomatic Acid Reflux Disease Without Esophagitis. Arch Intern Med. 2000;160(12):1810–1816. doi:10.1001/archinte.160.12.1810
9 at-home treatments for acid reflux. https://www.health.harvard.edu/newsletter_article/9-ways-to-relieve-acid-reflux-without-medication
Copyright © MediGloPark's All Rights Reserved.
 양성의 성대 병변은 비암성(noncancerous) 성장으로 하나 또는 두 개의 성대에서 형성될 수 있으며 결절(작은 혹), 폴립 그리고 낭종(cyst)의 형태로 나타난다. 대부분 성대를 과도하게 사용하거나 잘못 사용하는 경우 발생한다.
양성의 성대 병변은 비암성(noncancerous) 성장으로 하나 또는 두 개의 성대에서 형성될 수 있으며 결절(작은 혹), 폴립 그리고 낭종(cyst)의 형태로 나타난다. 대부분 성대를 과도하게 사용하거나 잘못 사용하는 경우 발생한다.| 성대질환 치료 및 예방을 위한 주의사항 |
|---|
| 큰 소리, 과도한 노래나 대화를 하지 않는다(특히 상기도 감염증이 있는 경우). |
| 과음을 하지 않는다. |
| 지나친 카페인(커피 등)은 성대의 건조를 야기하므로 피한다. |
| 반드시 금연한다. |
| 충분한 수분섭취로 성대가 건조하지 않도록 한다. |
| 충분한 수면을 취한다. |
| 노래나 장시간 말을 해야 하는 경우에는 성대를 따뜻하게 해준다. |
| 목소리를 크게 드러내고자 하는 경우는 마이크를 사용한다. |
| 성대 보습을 위해 가습기를 사용한다. |
| 스트레스 관리를 하며 요가 등 근 긴장 감소를 위한 운동을 한다. |
치료에는 발성치료, 행동수정(금연 등), 약물치료(성대 염증, 위산역류질환, 알레르기, 부비동염 등 치료), 수술(보존적 치료법으로 개선되지 않은 경우) 등이 있다.
위식도역류질환( gastroesophageal reflux disease, GERD)에 의한 폴립으로 진단된 경우에는 위산억제제(proton pump inhibitor 또는 potassium competitive acid blocker 등 )를 사용할 수 있으며 원활한 객담 배출을 위해 아세틸시스테인과 같은 점액용해제(acetylcyteine 캡슐 또는 흡입제 등)를 같이 사용할 수 있다.
- References
Zou Y, Deng D, Li X, Yang Z. Association between gastroesophageal reflux disease and vocal fold polyps. Medicine (Baltimore). 2021 May 21;100(20):e25787. doi: 10.1097/MD.0000000000025787. PMID: 34011039; PMCID: PMC8137056.
Hassan WA. Laryngeal polyp associated with reflux disease: a case report. J Med Case Rep. 2020 Jan 4;14(1):2. doi: 10.1186/s13256-019-2324-0. PMID: 31900189; PMCID: PMC6942414.
Copyright © MediGloPark's All Rights Reserved.
지주막하 출혈, 니모디핀(Nimodipine)과 다제약물
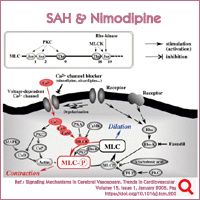 ▷ Nimodipine은 2세대 1,4-dihydropyridine CCB(calcium channel blocker)로 원래는 고혈압 치료제로 FDA 승인을 받았으나, 현재 FDA 승인 적응증은 지주막하 출혈(Subarachnoid hemorrhage, SAH)에 따른 뇌 혈관연축(vasospasm)의 예방과 치료이다.
Nimodipine은 졸중발작 후 신경학적 조건에 상관없이 허혈성 결손의 발생률과 심각도 저하 효과로 신경학적 결과를 개선한다.
Nimodipine은 친유성이고 BBB(blood-brain barrier)를 통과할 수 있으므로 우선적으로 뇌혈관에 작용하여 혈관 평활근 세포의 탈분극 시 칼슘 이온이 유입하는
voltage-gated L-type 칼슘 채널을 차단하므로 이 구조를 불활성화하여 혈관수축을 예방한다.
▷ Nimodipine은 2세대 1,4-dihydropyridine CCB(calcium channel blocker)로 원래는 고혈압 치료제로 FDA 승인을 받았으나, 현재 FDA 승인 적응증은 지주막하 출혈(Subarachnoid hemorrhage, SAH)에 따른 뇌 혈관연축(vasospasm)의 예방과 치료이다.
Nimodipine은 졸중발작 후 신경학적 조건에 상관없이 허혈성 결손의 발생률과 심각도 저하 효과로 신경학적 결과를 개선한다.
Nimodipine은 친유성이고 BBB(blood-brain barrier)를 통과할 수 있으므로 우선적으로 뇌혈관에 작용하여 혈관 평활근 세포의 탈분극 시 칼슘 이온이 유입하는
voltage-gated L-type 칼슘 채널을 차단하므로 이 구조를 불활성화하여 혈관수축을 예방한다.| Nimodipine의 작용 기전 |
|---|
| · 혈관조영적 혈관연축의 감소 |
| · 섬유소 용해 활성 증가 |
| · 신경보호 촉진 |
Nimodipine의 Off-Label 사용의 경우, 확산된 뇌손상에 고압산소치료(Hyperbaric Oxygen Therapy, HBOT)와 병용되며, 뇌신경(cranial nerve) 손상 후 회복 보조, 편두통 예방, 전신마취(general anesthesia, GA) 노인환자의 수술후 섬망 발생 감소, 말초성 어지럼증 및 메니에르질환(Ménière disease), 약물 내성 뇌전증, 오르가슴 및 목욕 관련 두통, 안과 처방 시 녹내장 관리 등에 사용되기도 한다.
SAH 환자에서 초기 출혈의 위험성 외에 초기 뇌손상과 그 후 뇌허혈에 의한 2차적 뇌손상이 심각한 문제가 되는데, 특히 Nimodipine이 장기적 뇌기능 개선에 효과가 있는 것으로 보고되었다. 또한 Nimodipine은 지연성 뇌허혈(delayed cerebral ischemia, DCI) 관련 사망 또는 식물인간 상태(vegetative state)의 위험성을 감소시키며, 뇌출혈 후 5~10일 동안에 Nimodipine 용량을 줄이는 것은 Nimodipone 사용의 유익성 상실로 이어질 수 있으므로 용량 감소 시 주의가 필요하다.
Nimodipine은 모든 동맥류성 지주막하 출혈(aneurysmal subarachnoid haemorrhage, aSAH) 환자에서 최대한 조기에 투여하여야 한다.
SAH 발생 후 신경학적 결손이 없는 환자에서 Nimodipine 투여는 혈관연축에 의한 새로운 신경학적 결손의 위험성을 낮출 수 있으며 매 4시간마다 Nimodipine 60mg을 경구 투여 시 SAH 후 뇌경색(cerebral infarction) 감소 및 결과 개선을 나타내는 것으로 보고되었다.
Nimodipine은 소혈관 피질하부 혈관성 치매(small vessel subcortical vascular dementia) 환자에 효과가 있는 것으로 보고 되었으며, SAH 후 혈관연축 예방에 경구투여와 정맥투여 효과는 동등한 것으로 보고되었다.
한편, Nimodipine은 두부 손상 환자, 급성 허혈성 반구 뇌졸중(acute ischemic hemispheric stroke), 초기 뇌졸중, 전조증상 없는 편두통 예방 등에는 효과가 없거나 거의 없는 것으로 나타났다.
| 구분 | Nimodipine 약동학(Pharmacokinetcs) |
|---|---|
| 흡수(Absorption) | · 음식과 복용 시 공복 대비 최고혈중농도 감소 및 생체이용률 저하(허가사항에는 식사 무관 복용) |
| 분포(Distribution) | · 혈장 단백(주로 α-acid glycoprotein)과 약 95% 결합하므로 α-acid glycoprotein 농도가 분포에 영향을 줌. |
| 대사(Metabolism) | · CYP3A4와 CYP3A5에 의해 대사 · CYP3A4 저해제에 의해 Nimodipine 혈장농도 증가 ※ CYP3A4 저해제 예: √ Macrolide antibiotics: erythromycin, clarithromycin, telithromycin √ Protease inhibitors: itonavir, indinavir, nelfinavir, saquinavir √ "-azole" Antimycotics: ketoconazole, voriconazole, itraconazole √ Antidepressants: nefazodone, fluoxetine √ quinupristin/dalfopristin, cimetidine, valproic acid √ grapefruit juice · CYP3A4 유도제 병용 시 Nimodipine 대사 촉진으로 혈청농도 감소, 치료 실패 가능성 증가 ※ CYP3A4 inducer의 예: carbamazepine, phenobarbital(phenobarbitone), phenytoin |
| 배설(Elimination) | · 최종 배설 반감기: 약 8~9시간 · 초기 배설 반감기: 1~2시간(4시간마다 투약 필요) · 신장 배설 |
노인환자는 심장, 간, 신장 기능 등이 저하된 경우가 많으므로 주의가 필요하며 CYP3A5 효소 발현이 저하된 환자에서 Nimodipine 투여 후 저혈압 및 방실차단(atrioventricular block) 부작용이 발생한 사례가 보고된 바 있다. Nimodipine은 항고혈압약과 병용 시 혈압저하 효과를 증가시킬 수 있으므로 이뇨제, β- 차단제, ACE 저해제, 칼슘길항제, α-차단제, PDE5 저해제, α-methyldopa 등과 동시에 투여 시 저혈압 예방을 위해 Nimodipine 용량 감소가 필요할 수 있다.
- References
Das JM, Zito PM. Nimodipine. [Updated 2024 May 7]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK534870/
Thilak, S., Brown, P., Whitehouse, T. et al. Diagnosis and management of subarachnoid haemorrhage. Nat Commun 15, 1850 (2024). https://doi.org/10.1038/s41467-024-46015-2
William S. Dodd, Dimitri Laurent, Aaron S. Dumont, Pascal M. Jabbour, Robert M. Starke, Brian L. Hoh, Nohra Chalouhi. Pathophysiology of Delayed Cerebral Ischemia After Subarachnoid Hemorrhage: A Review. Journal of the American Heart Association. Volume 10, Number 15, 2021. https://doi.org/10.1161/JAHA.121.021845
Copyright © MediGloPark's All Rights Reserved.
치매와 다제약물
 ▷ 대부분의 치매환자들은 노인이며 2가지 이상의 만성질환을 동반하는 경우가 많고 커뮤니케이션 장애와 인지기능 저하로 보통의 노인에 비해 다제약물의 위험에 노출될 가능성이 더 많다.
부적절 다제약물은 낙상, 노쇠 등의 증가와 관련이 있으며, 삶의 질 저하를 야기하고, 약물 유도성 인지기능 부전 위험성도 증가시킬 수 있다.
또한 이러한 부작용 이벤트들은 치매환자에서 비용과 돌봄 부담이 증가하는 결과를 나타내므로
다제약물에 대한 검토와 주의가 필요하다.
▷ 대부분의 치매환자들은 노인이며 2가지 이상의 만성질환을 동반하는 경우가 많고 커뮤니케이션 장애와 인지기능 저하로 보통의 노인에 비해 다제약물의 위험에 노출될 가능성이 더 많다.
부적절 다제약물은 낙상, 노쇠 등의 증가와 관련이 있으며, 삶의 질 저하를 야기하고, 약물 유도성 인지기능 부전 위험성도 증가시킬 수 있다.
또한 이러한 부작용 이벤트들은 치매환자에서 비용과 돌봄 부담이 증가하는 결과를 나타내므로
다제약물에 대한 검토와 주의가 필요하다.치매를 유발하는 위험인자에는 연령, 혈관성 위험인자, 두부 손상, 교육수준 등 다양한 요인들이 있다. 반면에 혈관 위험 인자들을 감소시키는 것으로 알려진 Statins, 항고혈압약, 항당뇨약 등은 인지 기능에 유익한 것으로 알려져 있다.
치매 치료 약물은 항콜린에스테라제(Anticholinesterase, Cholinesterase Inhibitor)와 NMDA(N-methyl-D-aspartate)-type glutamate 수용체 길항제로 대별된다. 항콜린에스테라제는 알츠하이머 치매에서 감소되는 acrtylcholine(Ach)의 분해를 억제하며 NMDA-type glutamate 수용체 길항제는 신경내 흥분독성을 야기하고 뇌가소성을 저해하는 Glutamate의 전달체계를 억제하여 치매의 진행을 늦추는 작용을 한다.
| 계열 | 치매 치료 약물 |
|---|---|
| Cholinesterase Inhibitors | Donepezyl, Galantamine, Rivastigmine |
| NMDA-type glutamate receptor antagonist | Memantine |
| Ach 합성 촉진제 | Acetyl-L-carnitine |
| Ach 전달 촉진제 | Choline alfoscerate, Nicergoline, Oxiracetam, Piracetam |
| 기타 | Cerebrolysin |
노인 에서 항우울제, 항정신병약, Benzodiazepines, Z-drugs와 같은 3종 이상의 중추신경계 작용약을 사용하는 것은 낙상과 골절의 위험성이 증가하므로 사용 자제를 권고하고 있다(Beers Criteria). 노인 치매환자에서는 특히 이러한 중추신경계 작용약과 치매 치료제를 병용 시 다제약물의 위험성에 주의하여야 한다. 다제약물과 인지기능 손상과의 관계에 대한 연구에서 다제약물에 노출된 노인의 경우 인지기능 손상의 위험성이 약 3배 증가하는 것으로 나타났다.
대부분의 치매환자들은 노인이므로 근육량과 체내 수분량이 비교적 저하되어 있는 반면에 체지방량은 증가하므로, 친유성 약물들의 분포용적은 감소하고 지용성 약물들의 분포용적은 증가하는 경향이 있다. 또한 노인의 경우 BBB(blood-brain barrier) 기능의 저하로 약물의 CNS 도달이 용이해지는 상황에 주의하여야 한다. 체내 흡수된 약물의 해독과 소실률도 노인에서는 감소하며, 간혈류, 간의 약물 청소율도 감소한다. 특히 노인에서 나타나는 신장 혈류 감소는 가장 심각한 약력학적 변화로서 약물의 신배설 저하를 야기한다.
Donepezyl과 Galantamine은 간에서 CYP3A4와 CYP2D6에 의해 대사된다. 약물대사와 관련된 상호작용 형태는 직접적인 비경쟁적 CYP3A4 효소저해(예: Ketoconazole)와 CYP3A4 효소 촉매자리에서의 경쟁적 저해로 대별된다. Donapezyl 대사에 대한 CYP2D6의 작용은 불분명하다.
Galantamine 대사는 CYP3A4와 CYP2D6 두 효소의 영향을 받는다. 강한 CYP3A4 저해제인 Ketoconazole과 강한 CYP2D6 저해제인 Paroxetine은 Galantamine과 병용 시 Galantamine의 AUC를 각각 30%와 40% 정도 증가시키는 것으로 나타났다. 또한 신기능 또는 간기능 부전 환자에서는 30~60% 정도의 Galantamine 혈중농도 증가가 발생하는 것으로 보고되었다. Donepezyl은 신손상이나 간손상 발생의 위험이 거의 없지만, 신손상 또는 간손상 환자에서는 Donepezyl 혈중농도가 상대적으로 증가한다. 특히 Galantamine의 경우 간기능 또는 신기능 손상 노인환자에서 Galantamine을 다른 약과 병용 시 생리학적 변화와 약물 상호작용에 의해서 혈중농도가 증가할 수 있으므로 매우 주의하여야 한다.
| 약물 | 약력학적(Pharmacokinetic) 상호작용 |
|---|---|
| Donepezyl Galantamine |
▷ CYP3A4 저해제에 의해 Donepezyl 대사 억제: 혈중농도 증가 · CYP3A4 저해제: Ketoconazole(direct non-competitive enzyme inhition), Itraconazole, Clarithromycin, Erythromycin, Ritonavir, Atazanavir, Verapamil 등 ▷ CYP3A4 저해제와 CYP2D6 저해제 모두에 의해 Galantamine 대사 억제 · CYP2D6 저해제: 항우울제(paroxetine, fluoxetine, bupropion, duloxetine, escitalopram, fluvoxamine, sertraline), Quinidine, Mirabegron(moderate) 등 ▷ CYP3A4 유도제에 의해 대사 촉진 · CYP3A4 유도제: Carbamazepine, Phenytoin, Rifampin 등 |
| Rivastigmine | · 혈액 esterase에 의해 대사(CYP 대사 없음: DDI 위험성 약함) |
| Memantine | ▷ 주로 비대사체로 뇨배설되므로 뇨pH에 영향을 받음 · Memantine은 약염기성 약물(pKa=10.27)로서 소변의 산성화로 인한 배설 증가(혈중농도 감소) 주의 : 뇨 pH 산성화로 인한 약효 저하 DDI 유발 · 현저한 뇨 알카리화로 배설 저하(혈중 농도 증가 → 독성 증가) 주의: 노인과 신기능 저하자는 특히 주의가 필요 · 뇨 알카리화 약물(Acetazolamide, Citric acid, Sodium bicarbonate 등)과 음식 주의 |
Rivastigmine은 혈중 esterase에 의해 빠르게 대사되며 cytochrome P450에 의해 대사되지 않으므로 cytochrome P450과 관련한 약물 상호작용 위험성은 없다. Memantine은 신배설되며 그 과정에서 뇨 pH에 영향을 받는다. 뇨가 산성화된 경우 신배설이 증가함에 따라 혈중농도가 감소하며, 뇨가 알카리화 되면 배설이 감소하여 혈중농도가 증가하게 되어 Memantine 노출 증대로 독성 위험성이 커진다.
한편, 약동학적 상호작용 관점에서 인지기능 개선 약물들은 일반적으로 시냅스 말단 Ach 농도를 증가시키는 작용을 하므로 반대의 작용을 하는 항콜린성 약물들과 병용 시 서로의 작용을 약화시킬 수 있다.
| 약물 | 약동학적(Pharmacodynamic) 상호작용 |
|---|---|
| Donepezyl Galantamine Rivastigmine |
▷ 항콜린성 약물의 항콜린 작용에 의한 치매약물의 효과 약화 : trihexyphenidyl, biperiden, butylscopolamine, atropine, amitriptyline, clomipramine 등 ▷ 콜린성 작용제에 의한 말초 콜린성 자극 촉진 : acetylcholine, betanechol, distigmine, neostigmine 등 |
| Memantine | ▷ NMDA-type glutamate 수용체 작용약과 병용 시 경쟁적 저해 : amantadine, ketamine, dextromethorphan |
퇴행성 치매 및 혈관성 치매의 위험성 증가와 인지기능 저하를 증가시키는 약물로는 Benzodiazepines와 같은 CNS 질환에 사용되는 약물, 일부 마약, 그리고 CNS에 작용하지는 않지만 PPIs(Proton pump inhibitors)도 포함되는 것으로 알려져 있다.
- References
Esumi S, Ushio S, Zamami Y. Polypharmacy in Older Adults with Alzheimer's Disease. Medicina (Kaunas). 2022 Oct 13;58(10):1445. doi: 10.3390/medicina58101445. PMID: 36295605; PMCID: PMC9608980.
Hea-Lim Kim, Hye-Jae Lee. Polypharmacy and associated factors in South Korean elderly patients with dementia: An analysis using National Health Insurance claims data. PLOS ONE. April 25, 2024. https://doi.org/10.1371/journal.pone.0302300
Barus R, Béné J, Deguil J, Gautier S, Bordet R. Drug interactions with dementia-related pathophysiological pathways worsen or prevent dementia. Br J Pharmacol. 2019 Sep;176(18):3413-3434. doi: 10.1111/bph.14607. Epub 2019 Mar 31. PMID: 30714122; PMCID: PMC6715604.
Kai Sin Chin. Pathophysiology of dementia. Australian Journal for General Practitioners. Volume 52, Issue 8, August 2023. doi: 10.31128/AJGP-02-23-6736.
Copyright © MediGloPark's All Rights Reserved.
마약성 진통제의 올바른 사용
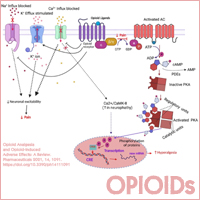 ▷ 마약성 진통제는 시냅스전 부위 및 시냅스후 부위 모두에 작용하여 진통효과를 나타낸다. 시냅스전 부위에 작용하여 구심성 통각신경의 칼슘 채널 차단으로 통각에 관여하는 substance P 및 glutamte와 같은 신경전달물질의 방출을 차단하며,
시냅스후 작용으로 포타슘 채널이 개방되고 세포막 과분극과 함께 통각 전달 발생에 요구되는 활동전위(action poential)가 증가한다. mu, kappa, 그리고 delta-opioid 수용체들이 통증에 관여한다.
▷ 마약성 진통제는 시냅스전 부위 및 시냅스후 부위 모두에 작용하여 진통효과를 나타낸다. 시냅스전 부위에 작용하여 구심성 통각신경의 칼슘 채널 차단으로 통각에 관여하는 substance P 및 glutamte와 같은 신경전달물질의 방출을 차단하며,
시냅스후 작용으로 포타슘 채널이 개방되고 세포막 과분극과 함께 통각 전달 발생에 요구되는 활동전위(action poential)가 증가한다. mu, kappa, 그리고 delta-opioid 수용체들이 통증에 관여한다. 또한, 일부 마약성 제제들은 약한 세로토닌 재흡수 억제작용과 세로토닌 뉴런에 대한 GABA성(gamma-aminobutyric acidergic) 시냅스전 억제 뉴런 저해를 통한 시냅스내 세로토닌 방출 증가 작용을 나타내므로 다른 세로토닌 작용제와 병용 시 세로토닌 동력학에 영향을 줄 수 있다. 이들 마약성 진통제들은 세로토닌 증후군을 야기할 수 있으므로 세로토닌 작용제와 병용 시 주의하여야 한다. Tramadol과 같은 Opioids의 세로토닌성 작용은 경련 역치를 저하시키므로 경련 기왕력 환자에서 경련증상을 야기하거나 악화시킬 수 있으므로 완전히 회피하거나 사용에 주의가 필요하다.
| 세로토닌 증후군 유발 가능 Opioids | 주의사항 및 특징 |
|---|---|
| Tramadol, Oxycodone, Fentanyl, Dextromethorphan, Meperidine, Codeine, Buprenorphine | · SSRI, SNRI 병용 시 세로토닌 증후군 위험성 증가 |
| Methadone | · SSRI, SNRI 병용 시 세로토닌 증후군 위험성 증가 · 부수적으로 NMDA(N-methyl-D-aspartate) 수용체에 결합하여 glutamate 작용에 길항하므로 신경병증성 통증에 다른 마약성 진통제들보다 효과적임 · QTc 간격 연장 또는 TdP(Torsades de Pointes) 위험성: QT연장증후군 환자에서 완전 회피 또는 사용 주의 |
마약성 진통제의 적응증은 주로 암성 통증, 급성 통증, 비암성 만성 통증(Chronic non-cancer pain, CNCP) 등이며, 비약물학적 치료 또는 다른 진통제로 통증 조절이 부적절한 경우에 사용된다. 마약성 진통제의 종류는 순수효능제, 부분 효능제, 혼합 효능-길항제 등이 있다.
마약성 진통제를 사용한다는 의미는 환자의 통증 조절이 매우 곤란함을 의미하므로 약료 시 주의하여야 한다.
일반적으로 통증 치료제는 비마약성 진통제+/- 보조제를 우선 사용하며(1단계), 통증이 지속될 경우 경증~보통 통증 치료용 마약성 진통제+/-비마약성 진통제+/-보조제(2단계), 그래도 통증이 지속될 경우 보통~심각 통증용 마약성 진통제+/-비마약성 진통제+/-보조제(3단계) 순으로 사용한다.
| 구분 | 마약성 진통제 |
|---|---|
| 순수 효능제 | Morphine, Oxycodone, Hydromorphone, Hydrocodone, Fentanyl, Codeine, Dihydrocodeine, Tramadol |
| 부분 효능제 | Buprenorphine |
| 혼합 효능-길항제 | Pentazocin, Butorphanol, Nalbuphine |
| Weak opioids | Codeine, Dihydrocodeine, Tramadol |
| Strong opioids | Morphine, Fentanyl, Hydromorphone, Oxycodone, Tapentadol |
마약성 진통제 중 부분 효능제 및 혼합 효능-길항제는 다른 마약성 진통제의 mu 수용체에서 작용을 경쟁할 수 있어 순수 효능제에 내약성이 있는 환자에게 사용 시 금단증상 및 재발성의 매우 급박한 (보통 관절부위)통증을 호소하는 통증위기(pain crisis)를 야기할 수 있다.
마약성 진통제는 급성 통증 초기 단계에서는 규칙적인 복용이 필요하지만, 통증이 경감되고 간혈적인 경우 필요 시 복용만으로도 조절이 가능하다. 지속적인 통증조절에 사용할 경우는 규칙적인 약물 복용이 필요하며 돌발성 통증 조절을 위해 속효성 제제를 병용하여야 한다. 한편, 환자의 신기능이 저하되어 있는 경우 대사체 축적에 의한 부작용의 위험성이 증가하므로 주의가 필요하다.
마약성 진통제의 주요 이상 사례는 다음과 같다.
| 마약성 진통제 사용 시 주의 사항 |
|---|
| 순수 효능제 내약성 환자에게 부분 효능제 및 혼합 효능-길항제 투여 시 μ-opioid receptor에서 경쟁적 길항으로 금단증상 및 pain crisis 발생 주의 |
| 지속적 통증 조절 시 규칙적 약물복용 필요. 돌발성 통증 조절을 위해 속효성 제제 병용 |
| 신기능 저하 시 대사체 축적에 의한 부작용 위험성 증가 |
| 마약성 진통제의 호흡관련 부작용 가능성으로 수면 무호흡 환자 주의 |
| ▷ 이상사례: 기분변화, 불쾌감, 황홀감, 진정, 집중력 저하, 오심 및 구토, 호흡저하, 호흡수 저하, 산소포화도 저하, 변비, 담도 경련, 뇨 저류, (마약성 진통제의 혈압 저하 효과로 인한)저혈압(: 저혈압 유발 약물 병용 주의), 가려움증 및 아주 드물게 기관지 수축에 의한 천식악화(: 히스타민 분비 관련), 약에 대한 내성, 금단 증상, 중독, 성선기능저하, gonadotropin-releasing hormone(GnRH) 분비 억제, (마약성 진통제의 세로토닌 작용에 기인한)세로토닌 증후군(: SSRI, SNRI 병용 시 위험성 증가) 등 |
마약성 진통제 사용 시 처방 오용(또는 남용) 위험성이 문제가 되며 다음과 같은 위험인자들에 주의하여야 한다.
| 구분 | 위험인자 |
|---|---|
| 남용 및 오용 가능성 | · 약물남용의 개인력 또는 가족력 · 고위험 대상 또는 환경과의 빈번한 접촉 |
| 연령 제한 | · 어린 연령 |
| 개인 또는 사회적 문제 | · 직장, 가족, 지인들과의 문제 야기 기왕력 · 아동학대의 기왕력 · 다양한 사회심리학적 스트레스 · 위험이나 스릴 지향적 행태의 기왕력 |
| 의존성 | · 흡연 등 규칙적 의존성 물질의 사용 · 약물 또는 알코올 중독 |
| 신경정신적 문제 | · 우울증 또는 불안증의 기왕력 |
마약성 진통제를 사용하는 성인에서 다제약물은 일반적인 현상이므로 의사, 약사를 포함한 임상전문가들은 치명적일 수 있는 마약 관련 DDIs(drug-drug intersctions)를 쉽게 파악하고 해결할 수 있어야 한다. 5가지 이상의 약물을 복용하는 입원 노인 환자들을 대상으로한 전향적 연구에서 cytochrome P450(CYP) 관련 DDIs가 80%로 나타났으며 복용약의 수가 증가할수록 심각한 DDIs 발생 가능성도 현저하게 증가한다.
일반적으로 DDIs는 약동학적(pharmacodynamic) DDIs와 약력학적(pharmacokinetic) DDIs로 대별된다. 전반적으로 마약성 진통제의 약동학적 DDIs는 benzodiazepines나 항우울제와 같은 CNS 억제제와 병용 시 많이 나타나며 호흡억제에 기인한 치명적 위험성과 낙상 등의 위험성이 심각하므로 주의가 필요하다.
마약성 진통제의 약력학적 DDIs는 CYP2D6와 CYP3As가 Opioid produg들의 활성화 또는 약물 모체(parent drug)의 배설에 관여한다. DDIs에 의해 진통효과가 감소하면 용량증가, 투여 횟수 증가로 내성, 의존성, 남용, 과용량 관련 사망 등의 위험성이 증가하므로 새로운 약물 개입 시 주의가 필요하다.
| CYP450 Isoforms | 약물대사 |
|---|---|
| CYP2D6 | ▷ Prodrug Opioids: CYP2D6 대사로 활성화(효소 친화성: 약함)되어 μ-opioid 수용체에 대한 친화성이 증가함 · Codeine → Morphine · Tramadol → O-desmethyltramadol · Oxycodone → Oxymorphone · Hydrocodone → Hydromorphone ▷ 유전적으로 CYP2D6 활성이 낮은 환자: 통증 조절 감소. 부작용 증가 ▷ 더 강한 친화성의 CYP2D6 기질(e.g., Propranolol)에 의해 경쟁적 대사(활성화) 저해 ▷ CYP2D6 inhibitor(e.g., Quinidine, Terbinafine, Amiodarone, Bupropion, Fluoxetin, Paroxetin, Mirabegron)에 의해 비경쟁적 대사(활성화) 저해 |
| CYP3A4/5 | ▷ Prodrug Opioids와 Non-prodrug opioids(e.g., Fentanyl)의 대사에 관여 ▷ CYP3A5 polymorphism에 따른 대사물 농도 변화: CYP3A5*1 발현자는 CYP3A5*3 발현자에 비해 Oxycodone 대사 증가로 대사물인 noroxycodone의 혈장 농도 증가 → 약용량 단계적 증가 위험 ▷ Prodrug Opioids는 CYP3As에 대한 효소 친화성이 약함 · CYP3A inhibitor(e.g., Ketoconazole, Voriconazole, Clarithromycin)에 의해 비경쟁적 대사 억제로 Opioid 관련 부작용 증가 · CYP3A inducer(e.g., Phenytoin, Rifampin)에 의해 Opioid 반응 감소 |
마약성 진통제의 노인주의 사항은 다음과 같다.
| 구분 | 마약성 진통제 노인 주의 사항 |
|---|---|
| Meferidine | 높은 신경계 독성(섬망 등) 위험성으로 사용 자제 권고. 특히 신부전 환자 위험(Beers) |
| 주의 질환 | 낙상 또는 골절 기왕력: 추가적인 낙상 유발 가능성으로 사용 자제(단, 마약성 진통제의 경우 최근 골절 및 관절 치환율로 인한 진통 목적인 경우는 제외) 권고(Beers). |
| 상호작용 | ▷ Opioid-Benzodiazepine: 호흡억제. Opioid 과량의 위험 증가. 수면 무호흡 또는 코골이 환자는 특히 주의 필요. ▷ Opioid-Gabapentinoid: 호흡곤란, 사망을 포함한 중증 진정 관련 부작용 위험 증가. 단, 마약성 진통제에서 Gabapentinoid로 전환되는 경우 Opioid 용량을 줄이기 위해서 병용하는 경우에는 주의하여 사용(Beers). |
| 만성 변비 환자 | 대체약이 있음에도 변비 유발 약제(마약류 포함)의 사용: 변비 악화 - 규칙적으로 마약성 진통제 사용 시 완하제 병용 필요(자극성 하제)(STOPP/START) |
| 경구 또는 경피형 강력 마약성 진통제를 경증 통증 일차선택약으로서 선택 | Morphine, Oxycodone, Fentanyl, Buprenorphine, Diamorphine, Methodone, Tramadol, Pethidine, Pentazocine(STOPP) |
| 돌발 통증을 위한 속효성 마약성 진통제 처방 없는 장시간 지속형 진통제 처방 | 중증 통증 지속 위험성(STOPP/START) |
마약성 진통제 사용의 적절성 평가는 약물의 필요성, 유효성, 복약 순응도, 안전성, 위험상병 등에 대한 검토 및 평가 등을 포함한다.
| 마약성 진통제의 적절성 평가 | 약물요법 최적화 계획 |
|---|---|
| ▷ 약물 필요성 및 유효성 평가 · 적응증 확인 · 통증 조절 확인: 속효성 진통제 복용 횟수 등 |
· 마약성 진통제의 적응증 확인(급성통증) · 현재 통증 조절 정도 확인: 속효성 진통제의 사용이 빈번할 경우 지속형 진통제의 용량 증량 필요(의료진에 고지) |
| ▷ 복약 순응도 평가 · 특수 제형: 패취제, 구강정, 설하정, 박칼정, 서방정 · 만성 통증 조절에 대한 환자 신념 및 약물치료법에 대한 이해도 평가 |
· 패취제, 구강정 등과 같은 특수제형 사용 시 주의가 필요한 약물에 대한 적절한 사용법에 대한 환자 교육 · 만성 통증 조절에 대한 환자 교육 시행 |
| ▷ 안전성 평가: 병용 약물 평가 · 벤조디아제핀, Gabapentin, Pregabalin: 과진정 평가 · 세로토닌 작용 약물: 특히 용량변경 또는 병용 초기 · 기타 중추신경계 억제 약물(술 포함) |
· 이상 사례가 의심될 경우: 병용약물 및 마약 요법 변경 고려 · 상호작용 위험 약물의 사용를 최소화 · 금주 권고 |
| ▷ 안전성 평가: · 실제 용량 및 용법, 의약품 보관 및 타인과의 공유 확인 |
· 의약품 보관법 및 타인과 공유 불가 교육 · 오남용이 의심될 경우: 환자 교육 및 의료진에 알림 · 임의의 용량 조정 불가를 교육 |
| ▷ 안전성 평가: 위험상병 확인 · 물질남용의 이력 및 정신과적 질환: 오남용 위험 증가 · 신기능의 저하: 과용량 위험 증가 · 심부전, 만성 폐질환, 수면 무호흡: 호흡저하 위험 증가 · 과거 낙상 및 골절의 이력: 낙상 위험 증가 · 저혈압 유발 가능 약물 병용: 저혈압 위험 증가 |
· 위험상병 동반의 경우: 환자 교육 시행 · 필요 시 의료진에 알림 시행 |
| ▷ 안전성 평가: · 변비 및 예방요법 확인 |
· 변비 예방에 대한 일반적인 교육 시행 및 예방요법에 대한 의료진 알림 시행 |
| ▷ 안전성 평가: · 진정 효과 확인: 졸림, 어눌한 언어구사 · 저혈압: 현기증, 권태감, 두통 등의 다양한 증상 · 호흡부전: 숨쉬기 어렵고 호흡이 느려지는 증상 · 소변저류 · 알러지 증상: 피부 발진, 가려움증, 쌕쌕거림, 흉부 압박감 등 · 세로토닌 증후군: 초조 환각, 혼동, 발한, 설사, 근육강직 등을 동반. 기분 변화나 환각 등을 경험 |
· 부작용이 의심되는 경우 의료진 알림 시행: 약물요법의 조정 및 적절한 치료를 진행할 수 있도록 함. |
| ▷ 기타, 일반적인 주의사항 | 잔여 마약 폐기 방법 교육: 펜타닐패취는 부착면끼리 접어서 폐기 |
마약성 진통제와 관련한 다제약물 중재는 적응증 복용행태 및 효과, 고위험 동반질환, 병용약, 상호작용, 부작용 등의 확인 및 검토를 포함한다.
| 70대 남성 | 만성 등 통증으로 hydrocodone/acetaminophen 7.5/325mg을 2정씩 1일 4~5회 복용. ibuprofen 600mg을 가끔 복용하는데 최근 복용횟수 증가(1일 3회)에도 무효하다고 함. 다른 약으로는 docusate, hydrochlorothiazide를 복용중. 고혈압 환자. 변비약을 복용중이나 개선 안됨. |
|---|---|
| 항목 | 중재 예시 |
| 적응증 확인 | 환자의 복용 이유 인지 여부를 질문하여 확인 |
| 복용 행태/효과 확인 | 복용시간, 복용 횟수, 복용량 인지 여부 확인, 통증 조절 상황, 처방용량대로 복용중인지 확인 |
| 고위험 동반질환 확인 | 낙상, 골절의 기왕력, 정신과 치료 경험, 심부전, 신부전, 간기능 저하 등 확인 |
| 병용약, 상호작용 확인 | 수면제, 신경통약, 우울증약, 기타 다른 약 복용중인지 질문하여 확인. 음주 여부 확인. |
| 부작용 확인 | 속이 울렁거리거나 미식거리지 않는지, 졸리움, 어눌한 말, 변비 여부, 알러지 여부 등 확인 |
| 기타 | 약의 보관, 약의 타인 공유 여부 확인 |
| 의원/병원 전달 사항 | · 현재 복용약으로 통증 조절이 되지 않음을 알림 · 고령의 고혈압 환자에게 ibuprofen의 사용은 혈압 조절 및 신기능에 영향을 줄 수 있어 그 사용이 적절하지 않을 수 있음을 알림 · 진통제 요법에 대한 변경 검토 및 지속적인 통증을 고려하여 장시간 작용 약물에 기반한 약물요법 검토 요망 알림 · docusate 복용에도 변비 호소 중이므로 약물요법 변경 검토 요망: 마약성 진통제를 지속적으로 사용 시 자극성 하제(Senna 등)의 사용이 권장됨. |
| 환자 주의사항 | · 복용 중인 진통제의 효과 부족으로 진통제의 변경이 필요하고 변비약도 변경이 요구됨을 설명하고 의료진과 상의를 권고(상담지 제공) · 변비 조절을 위해 평소 충분한 수분 및 야채의 섭취, 그리고 적절한 운동을 권고 · (마약성) 진통제를 변경하거나 증량 후 많이 졸립거나 말이 어눌한지 확인 후 해당되면 의료진 또는 조제약사와 반드시 상의할 것을 권고 · 진통제 용량을 늘리면 처음에는 약간 미식거릴 수 있으나 서서히 좋아질 수 있음을 고지(심한 경우 변경 및 용량조절을 의료진과 상담). 약의 용량 및 용법을 임의로 조정하지 마시고 반드시 의료진 또는 조제약사와 상의할 것을 권고 · 마약성 진통제의 타인 공유 금지를 고지 · 마약의 효과를 증가시킬 수 있는 약들도 있음을 고지하고 처방을 받을 때 현재 복용중인 약을 의료진 및 조제약사에게 미리 고지할 것을 주지시킴 · 금주의 필요성 · 만성통증의 경우 약물요법 이외에 도움이 되는 다른 방법을 주치의와 충분히 상담할 것을 권고 |
마약성 진통제의 일반적인 사용량은 다음과 같다.
| ▽ Opioid agonists in combination products for moderate pain | |
|---|---|
| Drug | Adult Dose |
| Codeine | · Oral: 30–60 mg every 4–6 hours as needed ※ Less potent than morphine |
| Hydrocodone | · Oral: 5–10 mg every 4–6 hours as needed ※ More potent than codeine |
| ▽ Opioid agonists for moderate-to-severe pain | |
| Drug | Adult Dose |
| Fentanyl | · Transdermal: 12 or 25 mcg/hour every 3 days · Transmucosal: 100–200 mcg every 2–4 hours · Intranasal: 100–200 mcg every 2–4 hours · Parenteral: 25–100 mcg every 30–60 minutes IV or as patient-controlled analgesia ◈ Pediatric Dose: Parenteral: 1–2 mcg/kg/dose IV; may be repeated in 2–4 hours as needed |
| Hydromorphone | · Oral immediate release: 2–4 mg every 4–6 hours · Oral extended-release: 8–32 mg every 24 hours · Oral liquid: 2.5–10 mg every 4–6 hours · Parenteral: 0.2–1 mg every 4–6 hours or as patient-controlled analgesia · Rectal: 3 mg every 6–8 hours(used at bedtime) ※ Short half-life |
| Levorphanol | · Oral: 2 mg every 6–8 hours · Parenteral: 1–2 mg IM or subcutaneously every 6–8 hours; 1 mg IV every 3–6 hours ※ Long half-life |
| Meperidine | · Oral: 50–300 mg every 4 hours · Parenteral: 50–150 mg IV or IM every 4 hours as needed ※ Not preferred: dysphoria, CNS excitation(eg, myoclonus, tremulousness, seizures caused by its active metabolite, normeperidine), accumulation(particularly in patients with renal failure) |
| Methadone | · Oral: 2.5–10 mg every 8–12 hours · Parenteral: 2.5–10 mg IM or IV every 8–12 hours ※ Risk of QT-interval prolongation; ECG monitoring recommended |
| Morphine | · Oral immediate-release: 5–30 mg every 4 hours · Oral controlled-release: 15 mg every 12 hours · Oral sustained-release: 30 mg every 24 hours · Parenteral: 2–5 mg IV or IM every 2–4 hours as neede ◈ Pediatric Dose: √ > 6 months old and < 50 kg: · Oral immediate-release tablet or oral solution: 0.2–0.5 mg/kg/dose every 3–4 hours as needed (usual initial maximum dose 15–20 mg/dose) · IV (preferred), subcutaneous, IM (IM not recommended): 0.05 mg/kg/dose every 2–4 hours as needed (initial maximum dose 1–2 mg/dose) √ > 6 months old and ≥ 50 kg: · Oral immediate-release tablets or oral solution: 15–20 mg every 3–4 hours as needed · Parenteral (IV, subcutaneous, or IM): 2–5 mg/dose every 2–4 hours as needed |
| Oxycodone | · Oral: 5–10 mg every 6 hours · Oral controlled-release: 10–20 mg every 12 hours ※ Also in combination products containing acetaminophen or aspirin |
| Oxymorphone | · Oral: 5 mg every 4 hours · Oral controlled-release: 5–10 mg every 12 hours · IM : 1–1.5 mg every 4 hours · IV: 0.5 mg every 4 hours · Rectal: 5 mg every 4–6 hours |
| ▽ Opioid agonist-antagonists | |
| Drug | Adult Dose |
| Buprenorphine | · IV or IM: 0.3 mg every 6 hours · Sublingual: 75 mcg once a day or, if tolerated, every 12 hours for ≥ 4 days, then increased to 150 mcg every 12 hours · Transdermal patch: initially 5mcg/hour applied once a week; may be titrated to 20 mcg/hour once a week |
| Butorphanol | · IV: Initially 1 mg, may be repeated every 3–4 hours as needed; usual range: 0.52 mg every 3–4 hours as needed · IM: Initially 2 mg, may be repeated every 3–4 hours as needed; usual range: 1–4 mg every 3–4 hours as needed · Nasal: Initially1 mg (1 spray in one nostril); if adequate relief is not achieved, may be repeated in 60–90 minutes; after the second dose, may be repeated every 3–4 hours as needed |
| Nalbuphine | · Parenteral: 10 mg IM, IV, subcutaneous every 3–6 hours |
| Pentazocine | · Oral: 50–100 mg every 3–4 hours · Parenteral: 30 mg IV, IM, every 3–4 hours (not to exceed 360 mg/day) |
| ▽ Mu-opioid agonists/norepinephrine reuptake inhibitors | |
| Drug | Adult Dose |
| Tapentadol | · Oral immediate-release: 50–100 mg every 4–6 hours, a second dose ≥ 1 hour later (≤ 700 mg total dose on 1st day); after 1st day, 50–100 mg every 4–6 hours (≤ 600 mg total daily dose) · Oral extended-release: 50 mg every 12 hours (usual therapeutic dose of 100–250 mg every 12 hours; maximum 500 mg/day) |
| Tramadol | · Oral immediate-release: 50–100 mg every 4–6 hours; maximum 400 mg/day · Oral extended-release: 100 mg once a day; increase by ≤ 100 mg/day every 5 days to a dose of ≤ 300 mg total daily dose ※ Less potential for abuse than with other opioids ※ Not as potent as other opioid analgesics |
- References
Matos A, Bankes DL, Bain KT, Ballinghoff T, Turgeon J. Opioids, Polypharmacy, and Drug Interactions: A Technological Paradigm Shift Is Needed to Ameliorate the Ongoing Opioid Epidemic. Pharmacy (Basel). 2020 Aug 25;8(3):154. doi: 10.3390/pharmacy8030154. PMID: 32854271; PMCID: PMC7559875.
Paul, A.K.; Smith, C.M.; Rahmatullah, M.; Nissapatorn, V.; Wilairatana, P.; Spetea, M.; Gueven, N.; Dietis, N. Opioid Analgesia and Opioid-Induced Adverse Effects: A Review. Pharmaceuticals 2021, 14, 1091. https://doi.org/10.3390/ph14111091
Cohen B, Ruth LJ, Preuss CV. Opioid Analgesics. [Updated 2023 Apr 29]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK459161/
MSD Manual professional version(2024). https://www.msdmanuals.com/professional/multimedia/table/opioid-analgesics
대한약사회 사이버연수원 학술자료(2024년).
Copyright © MediGloPark's All Rights Reserved.
비스테로이드성 소염진통제(NSAID)의 올바른 사용
 ▷ 모든 비스테로이드성 소염진통제(Nonsteroidal anti-inflammatory drugs, NSAIDs)는 COX(Cyclooxygenase) 효소를 억제한다. COX는 arachidonic acid를 prostaglandins(PGs)으로 전환하여
통증, 염증, 그리고 발열 등에 관여한다. 이 과정에서 PG H2가 thromboxane A2(혈소판에서 혈소판 응집과 혈전 형성 촉진), prostacyclin(=PGI2: 혈관 내피에서 혈소판 응집을 억제하는 혈관확장 작용)을
포함한 5종의 주된 PG로 전환된다. NSAIDs의 치료효과는 결과적으로 이들 에이코사노이드(eicosanoids) 결핍에 의한 것이다.
▷ 모든 비스테로이드성 소염진통제(Nonsteroidal anti-inflammatory drugs, NSAIDs)는 COX(Cyclooxygenase) 효소를 억제한다. COX는 arachidonic acid를 prostaglandins(PGs)으로 전환하여
통증, 염증, 그리고 발열 등에 관여한다. 이 과정에서 PG H2가 thromboxane A2(혈소판에서 혈소판 응집과 혈전 형성 촉진), prostacyclin(=PGI2: 혈관 내피에서 혈소판 응집을 억제하는 혈관확장 작용)을
포함한 5종의 주된 PG로 전환된다. NSAIDs의 치료효과는 결과적으로 이들 에이코사노이드(eicosanoids) 결핍에 의한 것이다.COX의 동종효소(isoenzyme)인 COX-1과 COX-2 중 COX-1은 본질적으로 체내에서 발현되어 위장관 점막 내벽 유지, 신기능, 혈소판 응집(혈소판에 의한 thromboxane 형성) 등에 관여한다. COX-2는 염증반응 과정에서 유도되어 발현된다. 대부분의 NSAIDs는 비선택적이어서 COX-1과 COX-2를 모두 억제한다. 그러나 Celecoxib와 같은 COX-2 선택적 NSAIDs는 COX-2를 목표로 하므로 상이한 부작용 양상을 나타낸다. COX-1은 위점막 보전에 매우 중요하고 COX-2 선택적 NSAIDs는 주로 염증반응에 관여하므로, COX-2 선택적 NSAIDs는 위점막 손상없이 항염작용을 나타낼 수 있다. 한편, COX-2는 본질적으로 발현되기도 하며 신장생리학적 기능, 생식기능, 골 재흡수 및 신경전달 등에 관여한다.
| COX의 기질(substrate) | COX에 의한 PGs 생성 | NSAIDs의 COX 저해 결과 |
|---|---|---|
| Arachidonic Acid → | ▷ GI mucosa:COX-1 → PGE2: gastric protection ① ↑mucus secretion ② ↑bicarbonate ③ ↑mucosal blood flow ▷ Kidney:COX-1&2 → PGE2 & PGI2: - afferent arteriolar vasodilation - ↑Na & water excretion ▷ Cardiovascular:COX1&2 → PGI2 & TXA2: - Vascular(COX-2:PGI2): ① vasodilation ② inhibit platelet aggregation - Platelet(COX-1:TXA2): ① platelet aggregation ② vasoconstriction |
▷ GI mucosa: COX-1 inhibition → - Peptic ulcers - GI bleeding ▷ Kidney: COX inhibition → - Na & water retention - Hypertension - Hemodynamic acute kidney injury ▷ Cardiovascular: COX-2 > COX-1 inhibition → - Stroke - Myocardial Infarction |
NSAIDs는 화학구조와 선택성을 근거로 구분한다.
| Chemical Structures or Selectivity | Drugs |
|---|---|
| Acetylated salicylates | Aspirin |
| Non-acetylated salicylates | Diflunisal, Salsalate |
| Propionic acids | Naproxen, Ibuprofen |
| Acetic acids | Diclofenac, Indomethacin |
| Enolic acids | Meloxicam, Piroxicam |
| Anthranilic acids | Meclofenamate, Mefenamic acid |
| Naphthylalanine | Nabumetone |
| Relatively selective COX-2 inhibitors | Etodolac, Meloxicam |
| Highly selective COX-2 inhibitors(-coxib) | Celecoxib, Etoricoxib, Polmacoxib |
선택적 COX-2 억제제는 위장관 궤양 위험성이 낮으며 혈소판 응집에 영향을 미치지 않아 출혈 위험성은 낮지만 혈전생성 위험성이 있고 고가인 특징이 있다.
노인 부적절 NSAIDs는 Ketolorac과 Indomethacin이 대표적이다.
| 대표적 노인 부적절 NSAIDs | 특징 및 주의사항 |
|---|---|
| ★ Ketolorac | · 매우강력한 NSAID. 마약성 진통제가 필요할 정도의 중등도에서 중증 급성 통증에 사용 · 소화성 궤양 유발률이 다른 NSAID 보다 높아서 단기간 사용으로 제한(주사: 2일, 경구: 5일) |
| ★ Indomethacin | · 중추신경계 부작용 위험이 높음. |
Beers, STOPP/START criteria의 NSAIDs의 노인주의 권고사항은 다음과 같다.
| NSAIDs | Beers, STOPP/START criteria 권고 |
|---|---|
| ★ NSAID(Aspirin > 325mg/d, Traditioal NSAID) | 다른 대체약이 없으며, PPI, misoprostol의 GI 예방약을 복용하는 경우가 아니면 만성적인 사용을 삼가 |
| ★ Ketorolac, Indomethacin | 노인에서 위장관 출혈, 소화성 궤양, 급성 신손상 위험 증가, Indomethacin은 다른 NSAID 보다 중추신경계 부작용 위험성이 높음 |
| Acetaminophen을 시도하지 않고, 골관절염 통증 경감을 위해서 장기간 NSAID 사용(3개월 초과) | STOPP |
| ▷ 질병에 따른 부적절 약물 · 심부전(Beers): 중증 고혈압 또는 심부전 환자에서 NSAID 사용 · 심장질환 환자에서 COX-2 억제제 사용(심근경색 및 뇌졸증 위험 증가) · 소화성 궤양(Beers): 소화성 궤양 또는 위장관 출혈의 기왕력이 있는 환자에서 COX-2 선택적 억제제 이외에 PPI 또는 H2 차단제 없이 NSAID 사용 · 만성신부전(Beers): GFR < 50ml/min 미만 환자에서 NSAID 사용 |
STOPP |
| ▷ 약물상호작용 · Corticosteroid - NSAIDs : 소화성 궤양 또는 출혈 위험성 증가 |
삼가거나 삼갈 수 없으면 위장관 보호제 사용(Beers) |
| ▷ 약물상호작용 · Warfarin, 항응고제(NOAC) - NSAIDs |
STOPP, Beers |
| ▷ 약물상호작용 · PPI 예방없이 NSAID와 항혈소판제 병용 |
STOPP |
NSAIDS는 위점막, 신장, 심혈관계, 간, 혈액계 등에 부작용을 나타내는 것으로 잘 알려져 있다. 위장관 장애는 COX-1 억제에 기인하지만 신독성과 심장독성은 COX-1억제제와 COX-2 억제제 모두에서 나타날 수 있다. 심혈관계 부작용(심근경색, 뇌졸중 등)은 특히 COX-2 선택성이 높을수록 심하다. 모든 비아스피린성 NSAIDs는 심혈관(Cardiovascular, CV) 혈전 위험성을 현저하게 증가실 수 있다.
COX-2 저해제는 thrombxane A2가 우세하게 균형을 변화시켜 혈전응집을 증가시킨다.
미국 FDA의 경고에 따르면 NSAID 복용 첫 주, 치료 초기에 심장마비나 뇌졸중 위험이 발생할 수 있으며 장기간 고용량 복용 시 부작용 위험은 더욱 증가한다. 또한 심장마비나 심장 우회술을 받은 환자는 NSAID로 인한 심혈관계 이상반응 위험이 가장 크다고 발표했다.
심근경색 후 최소 3~6개월간 NSAID를 사용하지 않는 것이 바람직하다. 고위험 심혈관계 환자에서는 Celecoxib보다 전통적인 NSAID(Naproxen)+PPI의 사용이 권장되며 NSAIDs의 사용을 가능하면 최저용량 및 최소기간으로 하여야 한다.
NSAIDs 장기 사용은 혈전생성 위험성 이외에 체액저류 효과로 인해 심부전 악화, 혈압조절 저하 효과가 발생한다.
| 구분 | NSAIDs 부작용 기전 및 주의사항 |
|---|---|
| 위점막 손상 | · COX-1억제(위점막 보호작용이 있는 PG 생성 저해) · 소화성 궤양 환자에서 더욱 심각: COX-2 선택적 NSAIDs 사용 권고(위험성 감소) |
| 신기능 손상 | · 신장에서 발현되는 COX-1 및 COX-2 억제 · 신 혈류역학(hemodynamics)과 사구체 여과(glomerular filtration)에 관여하는 PGs 생성 촉진 기능의 COX-1 저해 · 나트륨 및 수분배설에 관여하는 COX-2 저해 · 나트륨 저류, 말초부종, 혈압상승, 체중증가 · 신부전 환자 위험성 증가: 급성 신부전, 체액 및 전해질 장애(고칼륨혈증 등), 신장유두괴사(renal papillary necrosis), 신증후군(nephrotic syndrome), 간질성 신염(interstitial nephritis) |
| 심뇌혈관계 부작용 | · COX-1 및 COX-2 억제: 혈전 위험성 증가(아스피린계열 제외) · Coxibs: COX-2 저해제는 thromboxane A2가 우세하게 균형을 변화 → 혈전응집 증가 · Myocardial infarction(MI), 혈전색전증(thromboembolic events), 심방세동(atrial fibrillation), 울혈성 심부전(드묾) · Diclofenac: 심혈관 부작용이 가장 심한 NSAIDs에 속함 |
| 간독성 | · NSAIDs 관련 간독성은 드물지만, Diclofenac은 간독성 위험성이 높음 |
| 혈액학적 부작용 | 비선택적 NSAIDs의 항혈소판 작용: GI 궤양 기왕력 환자, 혈소판 활성 손상 관련 혈우병(hemophilia), 혈소판 감소증(thrombocytopenia), 폰 빌레브란트병(von Willebrand disease) 환자, 그리고 수술기주위(perioperative) 시 주의 |
NSAIDs에 의한 위장관 합병증 위험도는 위험인자에 따라 분류한다.
| 구분 | NSAIDs에 의한 위장관 합병증 위험인자 |
|---|---|
| 고위험 | · 위험인자: >2 · 합병증을 수반한 소화성 궤양의 기왕력 |
| 중간위험 | · 위험인자: 1~2 · 고령: 65세 이상(75세 이상?) · 합병증을 수반하지 않은 소화성 궤양의 기왕력 · 저용량 aspirin 병용(항혈소판제) · 항응고제 복용 · 스테로이드 복용 · 고용량 또는 중복 NSAIDs 치료 |
| 저위험 | 위험인자: 없음 |
| 독립적, 추가적 위험인자 | H. pylori 감염 |
NSIDs 유발 위장관 합병증 예방에는 non-NSAID , 선택적 COX-2 억제제 또는 NSAID + PPI 사용 등의 방법이 있다.
| NSIDs 유발 위장관 합병증 예방 방법 | 특징 |
|---|---|
| non-NSAID 진통제 투여 | |
| 가능한 저용량 NSAID 투여 | |
| 선택적 COX-2 억제제 투여 | |
| ★ NSAID + PPI | · 효과입증(표준치료) · 허가사항 기준으로 보험 인정(Omeprazole 20mg, Esomeprazole 20mg, Pantoprazole 20mg, Lansoprazole 15mg: 12주) |
| NSAID + H2 blockers | 논란 중 |
| NSAID + Misoprostol |
노인이나 만성병 환자에서 혈압과 만성 통증은 흔한 동반질환이므로 NSAIDs와 고혈압약을 병용해야 하는 경우가 많다. NSAIDs는 신장의 PGs를 억제하고 체액저류를 일으키므로 NSAIDs의 병용투여는 Furosemide와 같이 신장의 PG E2 합성 촉진 등 PGs에 작용하거나, 그외 이뇨제나 ACEI와 같이 신장의 PGs의 효과를 조절하는 약제의 효과를 감소시켜 혈압상승을 야기할 수 있다.
NSAIDs와 급성 신손상에 관한 대규모 연구에서 NSAIDs와 이뇨제, ACEI, 또는 ARB 병용 시 급성 신독성의 현저한 증가는 나타나지 않았으나, NSAIDs, 이뇨제, ACEIs 또는 ARBs를 함께 사용하는 삼중요법(triple therapy)의 경우 급성 신독성이 현저하게 증가하는 것으로 나타났다.
NSAIDs의 신장독성은 Coxib와 비선택적 NSAIDs 모두 발생 가능하다.
| NSAIDs의 신장독성 |
|---|
| ·신장 관류가 감소되는 상황에서는 신장에서의 PG 생성이 중요한 보상기전임 |
| · ★ 직접적인 독성, 신장 혈관 확장작용과 신혈류량을 보존하는 국소 PGs 억제작용에 의해서 급성 신독성 발생 가능 | · ★ Coxib와 비선택적 NSAIDs 모두 발생 가능 |
| · 치료 시작 초기 발생 | · 치료 중단 시 가역적임 | · 임상양상: 급성 신부전(BUN, Scr↑), Hyperkalemmia, BP↑, 말초부종, 체중증가 |
| · ★ GFR < 30(50)ml/min: 경구 NSAIDs 삼가 |
| · 위험인자: ① 연령 > 65세 ② 만성 신부전, 신증후군 ③ 울혈성 심부전 ④ 중증 간질환 ⑤ 이뇨제, ACEI, Cyclosporine, Aminoglycosides 병용환자 ⑥ 급성 탈수 환자에서 NSAID 과량 투여 ⑦ 단독 고용량 다회 또는 복합 또는 장기 투여 ⑧ 모니터링 필요 ⑨ 이뇨제 + ACEI + NSAIDs: 첫 30일 이내에 급성 신손상 발생 위험 82% 증가 |
spironolactone과 같은 aldosterone 길항제는 상부 GI 출혈 위험성 증가 위험성이 있으므로 환자에게 OTC NSAIDs의 장기간 병용을 삼가하도록 권고하여야 한다.
| NSAID - Drug | Interactions |
|---|---|
| · NSAID + Furosemide · NSAID + other Diuretic or ACEI, ARB |
NSAIDs의 PGs 억제로 효과 감소: 혈압상승 위험 |
| Ibuprofen + ACEI or ARB | BP(SBP) 상승 주의 |
| Triple Therapy: NSAID + Diuretic + ACEI or ARB |
급성 신독성 발생 위험성 증가 |
| Aldosterone antagonist(Spironolactone) + long term use of NSAID | 상부 GI 출혈 위험성 증가 |
NSAIDs 복용에 대한 적절성 평가는 고위험 동반질환 확인, 복용행태 및 효과확인, 중복 복용 확인, 병용약 및 상호작용 평가, 부작용 확인 등을 포함한다.
| NSAIDs 사용 적절성 평가 | 약물요법 최적화 계획 |
|---|---|
| ▷ 약물 필요성 및 유효성 평가 - 적응증 및 적응증 지속 확인 - 중복 여부 확인(처방약, OTC약) - Ketorolac, Indomethacin 포함 여부 - 통증조절 효과 평가 |
- 복용 이유, 적응증의 지속 여부 확인을 통해 과다한 NSAID 사용이 있는지 검토하고, 서로 다른 통증으로 인한 NSAID 중복 복용 확인 및 시정(처방약, OTC) - 통증 조절 효과 확인, 국소제제 등으로 변경 가능성 확인 |
| ▷ 복약 순응도 평가 - 복약행태 확인(필요시, 지속적 복용 등) |
- 필요시, 아플 때만 복용 또는 지속적 복용, 과다 복용 여부 확인 |
| ▷ 안전성 평가 - 병용약물 평가: · 항응고제, 항혈소판제: 출혈위험 증가 · Aspirin + Ibuprofen: aspirin 항혈전 효과 감소 · Aspirin + Methotrexate: Methotrexate 독성 증가 · 스테로이드: 위장관 위험증가 · RAS 억제제 + 이뇨제 + 탈수상황 |
- 출혈 위험 증가, 가능한 중단, 꼭 필요한 경우 PPI 병용 추천 - RAS 억제제 + 이뇨제 + 탈수상황(설사, 구토 등): 급성 신손상의 위험 회피를 위해 NSAID 일시 중단 권고 |
| ▷ 안전성 평가 - 위험상병 확인: · 위장관 궤양, 위장관 출혈 기왕력 · 만성신장병 · 심부전 · 조절되지 않는 고혈압 |
· 위험상병 동반의 경우 예방조치 확인 · 가능한 다른 진통제 사용 또는 최소한의 기간 사용 권고 · 필요 시 의료진 알림 시행 |
| ▷ 안전성 평가 - 부작용 확인: · 위장관 합병증 · 신기능 · 혈압조절 · 심부전 증상 악화 등 |
· 장기 사용 시 소화성 궤양, 신기능 저하 등의 가능성: 정기적 진료 및 검사를 권고 · 위험상병 악화 시 중단 가능성 판단 후 진료의와 상담을 권고 |
| ▷ 기타, 일반적인 주의사항: · NSIDs 중복 투여 가능성 예방 |
· OTC 제제(Ibuprofen, Naproxen 등) 복용으로 중복 사용 가능: 추가 진통제 필요 시 Acetaminophen 권고 · 통증 시 사용 진통제의 동일 계열 가능성 교육 |
환자 NSAIDs 약료 상담 시는 적응증, 중복 복용 여부, 복용행태 및 효과, 고위험 동반질환, 병용약 및 상호작용, 부작용 등을 확인하고 평가한다.
| ▷ 질환명(80대, F): 골관절염, 스텐트 시술 |
▷ 사용약물: NSAID(without PPI) 장기 복용(속쓰림으로 알마겔 병용 중), Aspirin, Clopidogrel |
약료 상담의 예 |
중재 예시 |
|---|---|
| ① 적응증 및 중복 복용 확인: 복용이유, 복용기간, 중복 진통제 복용 여부 ② 복용행태 및 효과 확인: 매일 또는 통증 시에만 복용 여부, 복용량, 효과 확인 ③ 고위험 동반질환 확인: 속쓰림, 내시경 검사 여부, 뇌졸중, 심장질환, 신장질환 동반 여부 ④ 병용약 및 상호작용 확인: 혈액순환제(Ginkgo biloba extract 등), 심장병 예방약(Aspirin, Clopidogrel 등) 복용 여부 ⑤ 부작용 확인: 속쓰림, 짜장색 변, 붉은 변, 자주 드는 멍 등 부작용 증상 확인 |
▷ 환자 주의 사항: · 현재 복용 중인 모든 약을 의사에게 고지 권고 · 스텐트 시술 후 항혈전제 복용의 중요성 강조 · 소염진통제 병용 시 위장 문제 발생의 위험성 고지(의사와 상담을 권고) · 구토, 설사 등이 있으면 진통제 일시 중단 후 의사와 상담 · 신장 기능이 점차 감소할 수 있으므로 정기적 신기능 검사 권고 ▷ 상담지 포함 사항(의사 통보): · 지속적인 소염진통제(NSAID) 복용 중인 환자로 최근에 스텐트 시술 후 이종 항혈소판제(아스피린+클로피도그렐)를 복용하기 시작함 · 위장관 출혈이나 다른 위장 문제가 없는지 검토 요망 · NSAID를 Acetaminophen 또는 Tramadol로 변경하거나 변경이 어려운 경우 PPI 병용 처방을 고려 |
- References
Davis A, Robson J. The dangers of NSAIDs: look both ways. Br J Gen Pract. 2016 Apr;66(645):172-3. doi: 10.3399/bjgp16X684433. PMID: 27033477; PMCID: PMC4809680.
Abdu N, Mosazghi A, Teweldemedhin S, Asfaha L, Teshale M, Kibreab M, Anand IS, Tesfamariam EH, Russom M. Non-Steroidal Anti-Inflammatory Drugs (NSAIDs): Usage and co-prescription with other potentially interacting drugs in elderly: A cross-sectional study. PLoS One. 2020 Oct 9;15(10):e0238868. doi: 10.1371/journal.pone.0238868. PMID: 33035226; PMCID: PMC7546451.
Moore N, Pollack C, Butkerait P. Adverse drug reactions and drug-drug interactions with over-the-counter NSAIDs. Ther Clin Risk Manag. 2015 Jul 15;11:1061-75. doi: 10.2147/TCRM.S79135. PMID: 26203254; PMCID: PMC4508078.
Sara L. Noble et al. Cyclooxygenase-2 Enzyme Inhibitors: Place in Therapy. Am Fam Physician. 2000;61(12):3669-3676.
Feldman M, McMahon AT. Do cyclooxygenase-2 inhibitors provide benefits similar to those of traditional nonsteroidal anti-inflammatory drugs, with less gastrointestinal toxicity? Annals of Internal Medicine 2000;132:134–43.
대한약사회 사이버연수원 학술자료(2024).
Copyright © MediGloPark's All Rights Reserved.
파킨슨병과 다제약물
 ▷ 파킨슨병(Parkinson's Disease, PD)의 확실한 치료방법은 없지만, 약물치료나 수술요법 등을 통하여 증상을 개선할 수 있다. Dopamine의 전구체인 Levodopa는
혈액뇌관문(blood-brain barrier, BBB)을 통과하여 들어간 후 Dopamine으로 전환된다.
▷ 파킨슨병(Parkinson's Disease, PD)의 확실한 치료방법은 없지만, 약물치료나 수술요법 등을 통하여 증상을 개선할 수 있다. Dopamine의 전구체인 Levodopa는
혈액뇌관문(blood-brain barrier, BBB)을 통과하여 들어간 후 Dopamine으로 전환된다.통상 Levodopa는 Carbidopa와 조합하여 사용하는데, Carbidopa는 Benserazide와 같이 말초 aromatic-L-amino-acid decarboxylase 억제제로서 Levodopa가 뇌 외부 혈류에서 Dopamine으로 조기 전환되지 않도록 보호 (aromatic-L-amino-acid decarboxylase 저해제가 없으면 대부분의 Levodopa가 분해되어 뇌로 진입하는 양은 약 1% 정도임)하여 뇌로 진입하도록 한다. 이는 Levodopa의 생체이용률을 높일 뿐만아니라 Levodopa 치료에서 나타나는 부작용(오심, 구토, 저혈압, 피로, 나른함, 두통, 졸음 등)을 예방하거나 경감시킨다.
BBB를 통과한 Levodopa가 뇌내 신경세포에 의해 흡수되어 Dopamine으로 전환되면 시냅스 후 도파민 수용체를 활성화하여 감소되어 있는 Dopamine을 보충하게 된다. 초기 투여 시 Levodopa는 PD 증상개선에 큰 효과를 나타내지만 PD 환자의 특성 상 뇌 내 신경세포가 더 많이 손실(약물 흡수를 할 수 있는 신경세포가 감소)되므로 그 효과는 수년 이상 오래 지속되지 못한다. Levodopa 사용을 갑자기 중단하면 운동불능, 호흡곤란 등과 같은 심각한 부작용이 발생할 수 있으므로 주의하여야 한다. 한편, Levodopa는 off-label 사용의 경우 하지불안증후군(Restless Leg Syndrome)과 주기성 사지운동장애(Periodic Limb Movement in Sleep, PLMS) 등에 쓰인다.
PD 증상을 치료하기 위한 약물은 Dopamine 작용제, MAO-B(Monoamine oxidase-B) 억제제, COMT(Catechol-O-methyltransferase) 억제제, 항콜린성 약물 등이 있다. Dopamine 작용제(Ergot-based dopamine agonists: Bromocriptine, Cabergoline / Non-ergot-based dopamine agonists: Amantadine, Apomorphine, Fenoldopam, Pramipexole, Ropinirole, Rotigotine) 중에서는 Pramipexole, Ropinirole, Rotigotine 및 Apomorphine(Subcutaneous route) 등이 많이 사용된다.
| PD 증상 치료제 | 특징 |
|---|---|
| Levodopa: Co-beneldopa(Madopar®) , Co-careldopa | Dopamine 보충. 대부분의 PD 환자에 처방. |
| ▷ Dopamine agonists: Bromocriptine, Cabergoline, Fenoldopam, Pramipexole, Ropinirole, Rotigotine, Amantadine, Apomorphine(Subcutaneous route) | · 뇌내 Dopamine 생성 촉진 · 불수의 운동(Involuntary movement, Dyskinesia) 감소 |
| ▷ Enzyme inhibitors · MAO-B inhibitors: Selegiline, Rasagiline, Safinamide · COMT inhibitors: Entacapone, Co-careldopa and entacapone, Opicapone |
· Dopamine 양의 증가(←뇌내 Dopamine 분해 효소를 저해) · MAO-B 억제제 효과: < Levodopa · MAO-B 억제제는 주로 초기 PD 환자에 사용. · COMT 억제제는 주로 말기 PD 환자에 사용. |
| Foslevodopa/Foscarbidopa | · 심한 PD에 사용 · 가용성 Levodopa/Carbidopa phosphate의 연속적 s.c. infusion(안정된 Levodopa 공급). |
| 항콜린성 약물: Procyclidine, Trihexyphenidyl or Benzhexol | 진전(Tremors) 및 근경직(Muscle rigidity) 감소 |
PD 치료 시 약물치료에 잘 반응하지 않는 경우 뇌심부 자극술(Deep Brain Stimulation, DBS)을 사용하면 뇌심부에 이식한 전극들과 연결된 흉부내 소형 장치가 뇌의 특정영역을 자극하여 진전, 거동지연(slow movement), 경직 등 움직임과 관련된 많은 PD의 증상을 개선하는데 도움이 된다. 또한 물리치료, 식이요법, 운동요법, 언어치료(speech therapy), 작업치료(occupational therapy), 마사지 치료, 요가 등이 PD 증상 관리에 도움이 될 수 있다.
| PD 의 비약물 치료 | 특징 |
|---|---|
| 뇌심부 자극술(DBS) | 진전, 거동지연, 근육경직 등의 개선 |
| 물리치료, 작업치료, 언어치료 | 보행장애(gait disturbance), 음성장애(voice disorder), 진전, 경직, 정신기능(mental function) 쇠퇴 등의 개선에 도움. |
| 건강한 식이요법 | 전반적 건강 유지 |
| 운동요법 | 근육강화. 균형감, 유연성, 신체 조정력 등의 향상 |
| 마사지 치료 | 근육 긴장 완화 |
| 요가 | 유연성 증가 |
동시에 같이 사용하면 안되는 약물들임에도 불구하고 약물-약물 상호작용 발생을 감수하고 서로 다른 두 약물을 사용하는 경우가 있는데, 이 경우에는 의사가 용량조절을 하거나 주의하여야 할 필요가 있다. Levodopa-Carbidopa 복용 시 MAO 억제제(isocarboxazid, linezolid, metaxalone, methylene blue, moclobemide, phenelzine, procarbazine, tranylcypromine)를 같이 복용하게 되면 심각한(혹은 치명적) 약물 상호작용이 발생할 수 있다. 대부분의 MAO 억제제는 Levodopa-Carbidopa 치료전 2주 동안 복용하지 않아야 하지만, rasagiline, safinamide, selegiline과 같은 일부 MAO억제제는 의사의 세심한 모니터링 하에 사용이 가능하다.
Levodopa-Carbidopa 사용 시 주의하여야 할 약물은 다음과 같다.
| 구분 | Levodopa-Carbidopa 사용 시 주의 약물 | 조치사항 |
|---|---|---|
| Not recommended | Bromopride, Clorgyline, Furazolidone, Iproniazid, Isocarboxazid, Linezolid, Methylene Blue, Moclobemide, Nialamide, Pargyline, Phenelzine, Procarbazine, Sulpiride, Toloxatone, Tranylcypromine | 중단 또는 다른 약물로 대체를 고려 |
| Usually not recommended | Amisulpride. Bupropion. Haloperidol. Isoniazid. Macimorelin. Metoclopramide. Olanzapine. Sapropterin | 용량 또는 사용 횟수 조절을 고려 |
| Increased risk of certain side effects | Droxidopa, Fosphenytoin, Indinavir, Iron, Kava, Phenylalanine, Phenytoin, Spiramycin, Tyrosine | 용량 또는 사용 횟수 조절을 고려 |
PD 환자는 치매를 동반하는 것으로 잘 알려져 있다. 연구에 따르면 새로 진단된 PD 환자의 15~20%에서 MCI(Minimal Cognitive Impairment)가 있으며, PD 이환(罹患) 후 20년 경과 시 PD 환자의 80%가 치매환자로 진단되는 것으로 나타났다. 따라서 PD 초기 단계에서 MCI에 대한 효과적인 조기 개입으로 치매 진행을 예방하는 것이 필요하다.
다제약물 회피를 위한 약제 감소 노력은 인지기능 개선을 위한 효과적인 개입이 될 수 있다. MMSE(Mini-Mental State Examination) 점수로 측정한 다제약물과 인지기능 관계 연구에서 새로 진단된 PD환자가 다제약물에 노출된 경우 다제약물 기준 이하의 환자에 비해 인지기능이 낮게 나타났는데, 이는 약제 감소 노력이 초기 PD 환자의 치매 전개를 예방할 수 있는 효과적인 개입이 될 수 있다는 것을 의미한다.
Levodopa는 음식물 섭취 시 효과가 저하될 수 있다. 특히 고단백 식품은 Levodopa의 효과를 저하시키므로 주의하여야 하며, 단백질 섭취 시는 적절한 양의 단백질을 Levodopa 복용시간과 충분한 간격을 유지하고 섭취하여야 한다. 고단백 식품 섭취 후 혈장 LNAA(Large Neutral Amino Acid: Tryptophan, Tyrosine, Phenylalanine, BCAA) 수준이 증가하는데 BBB 통과 시 Levodopa와 동일한 포화가능 수송계에서 경쟁적으로 Levodopa의 BBB 통과를 저해할 수 있다. 여러 연구에서 고단백 섭취 후 Levodopa 치료는 혈장 Levodopa 수준이 공복 시보다 상승함에도 효과가 없는 것으로 나타났다.
철분은 catechol 구조를 가진 Levodopa-Carbidopa와 같은 약물과 chelation을 하여 작용을 저해할 수 있으므로 동시에 복용하지 않아야 한다.
규칙적인 커피섭취가 파킨슨병의 악화 위험을 낮추고 그 진행률을 낮추는 것으로 알려져 있다. 이는 커피 중의 카페인과 Methylxanthine이 dopamine 생성 신경에 보호효과를 나타내기 때문인 것으로 알려져 있다. Methylxantine은 비선택적 adenosine 수용체 길항제이다. 뇌의 adenosine 수용체 subtype인 A1과 A2A는 운동기능, 시냅스 가소성(synaptic plasticity), 신경신호 등을 조절한다. Levodopa 치료에 미치는 커피의 영향에 대해서는 논란이 있는데, 1일 300~1400mg의 고카페인 섭취의 경우 LID(levodopa-induced dyskinesias) 지속시간이 증가하지만 보통의 규칙적 섭취(1~3잔/하루)는 초기 PD에서 LID의 장기간 위험성을 낮출 수 있는 것으로 보고되었다. 동물 모델에서 만성적 A2A 수용체 차단은 반복적 도파민성 자극(dopaminergic stimulation)으로 야기되는 부적응 가소성(maladaptive plasticity)을 예방할 수 있는 것으로 보고되었다. 또한 카페인은 위배출(gastric emptying)을 가속하여 Levodopa의 흡수가 촉진되는 것으로 알려져 있다.
PD환자의 50~80% 정도가 변비로 고생한다. 이는 위장관 통과 지연, 장 운동성 저하, 항콜린성약물(cholinolytics)의 사용 등에 기인한다. 위장관운동촉진제(prokinetics)는 그 효과에도 불구하고 부작용으로 인해 주기적 사용이 부적절하다. 따라서 섬유소가 좀 더 안전한 선택이 될 수 있으며, 섬유소(차전자피: Plantago ovata husk)와 Levodopa를 동시에 투여 시 Levodopa의 흡수가 균일하고 완만하게 나타나고 Cmax는 감소하며 생체이용률은 증가하는 것으로 보고되었다. 이러한 결과는 섬유소가 변비를 해소하고 Levodopa의 부작용을 감소시키며 생체이용률을 높이는데 도움이 될 수 있다는 것을 의미한다.
비타민 C는 항산화작용으로 신경보호작용이 있으며, Levodopa와 병용 시 Levodopa 흡수율이 낮은 환자에서 비타민 C의 산성과 위산 분비 촉진에 기인한 위내 pH 저하로 Levodopa의 용해율이 증가하고 비타민 C에 의한 장 운동 촉진(Levodopa의 작용 개시 시간 단축)으로 Levodopa의 생체이용률(AUC 증가, Cmax 증가, tmax 감소)이 현저하게 증가 한다.
비타민 B6(50~100mg/day. oral)는 decarboxylase에 의한 방향족 L-아미노산의 탈탄산반응을 활성화 하여 Levodopa의 대사를 촉진한다. 그러나 대부분 PD 치료에서 같이 사용하는 Carbidopa나 Benserazide와 같은 dercarboxylase 억제제와 같이 병용투여 시 비타민 B6의 영향이 소실된다. 따라서 비타민 B6를 Levodopa_Carbidopa(또는 Benserazide)와 동시 투여 시 치료효과에는 영향이 없다. 한편, 만성적으으로 Levodopa를 사용하는 PD 환자의 1/3이상이 말초신경병증을 나타내는데 비타민 B6 수준이 낮으면 더욱 심해지므로 고용량(1000mg 이상/day)이 아닌 적정량의 비타민 B6의 섭취가 도움이 된다.
노인 PD 환자에서 일반적인 질환인 당뇨를 동반하는 경우 인공감미료인 아스파탐(Aspartame)을 사용하는 경우가 많은데, 아스파탐은 장에서 LNAAs 중 하나인 phenylalanine으로 가수분해 되어 Levodopa의 유입 시 경쟁하고 Levodopa의 흡수저하를 초래할 것으로 생각된다. 그러나 고용량의 아스파탐을 투여한 연구에서 phenylanine 수준이 증가함에도 환자의 운동수행(Motor Performance)에는 영향이 없는 것으로 나타나 Levodopa 효과에 대한 부정적 영향은 관찰되지 않았다.
| Levodopa-Food(Nutrients) | 특징 및 주의사항 |
|---|---|
| Levodopa와 표준식 | 식후 Levodopa+Carbidopa/Benserazide 복용 시 Levodopa의 현저한 흡수억제: 공복 시 복용(위장장애 시는 소량의 저단백 식사 후 복용을 고려). |
| Levodopa와 고단백 식품 | Levodopa에 대한 LNAAs의 경쟁적 저해로 Levodopa의 효과 저하: Levodopa는 공복 시 복용하고, 적량의 단백질을 Levodopa 복용 시간과 충분한 간격를 두고 일정한 시간 간격으로 분할 섭취. |
| Levodopa와 철분 보조제 | · 철 의존적 페롭토시스(ferroptosis) 조절 세포사멸 경로를 통해 PD 병인(pathogenesis)에 관련됨. · Levodopa의 현저한 흡수억제(←Chelation): 철분과 Levodopa-Carbidopa 투여 시 2시간 이상 간격 유지(Levodopa 및 Carbidopa와의 Chelation 회피) |
| Levodopa와 Enteral Nutrition | 고단백 성분 함유로 Levodopa 효과가 현저하게 감소: 단백질 함량을 낮추고 Levodopa 투여 시간과 충분한 간격 유지 또는 Levodopa 투여량 증가 고려 |
| Levodopa와 커피 | · 적정량의 커피는 LID 위험성 저하 및 Levodopa의 흡수 증가(더 많은 연구가 필요함) · 고카페인 회피(LID 위험성 증가) |
| 섬유소(차전자피 등) | · PD 환자 변비에 도움 · Levodopa 생체 이용률 증가 및 Cmax 감소 |
| Levodopa와 비타민 C | 비타민 C에 의한 Levodopa의 생체이용률 증가: PD 치료효과 향상 |
| Levodopa+비타민 B6 | decarboxylation 촉진으로 Levodopa 효과 감소 |
| Levodopa/Carbidopa(또는 Benserazide)+비타민 B6 | Levodopa 효과 불변(←Carbidopa 또는 Benserazide의 decarboxylase 억제). |
| Levodopa와 Aspartame(600 또는 1200mg) | Aspartame의 가수분해로 인한 Phenylalanine 생성에도 운동수행능 불변 |
뇌내 dopamine 수용체를 활성화하는 dopamine 작용제(Ropinirole, Bromocriptine, Cabergoline 등)는 음식물과 같이 복용할 때 흡수시간은 지연되나 생체이용률에는 큰 차이가 없는 것으로 나타났으며, 특히 음식물 관련 연구에서 Cabergoline이 음식물과의 상호작용이 가장 적은 것으로 나타났다.
Bromocriptine은 CYP450 3A4로 대사되므로 이 효소를 억제하는 자몽주스를 지나치게 섭취하지 않도록 주의하여야 한다.
| Dopamine agonists-Food(Nutrients) | 특징 및 주의사항 |
|---|---|
| Dopamine agonists( ropinirole, bromocriptine, cabergoline)+Food | 흡수시간 지연은 있으나 생체이용률에는 큰 영향 없음(식사와 함께 복용하면 오심 부작용 감소). |
| Bromocriptine + 자몽주스 | Bromocriptine 대사 감소로 부작용 증가 위험(←자몽주스에 의한 CYP3A4 억제) |
Levodopa는 COMT에 의해 대사되어 불활성화 된다. COMT 억제제(Entacapone, Tolcapone, Opicapone 등)는 Levodopa와 병용하여 혈류에서 Levodopa가 거의 분해되지 않고 BBB를 통과하여 뇌에 진입할 수 있도록 하며, Levodopa의 투여량을 줄일 수 있고, Dopamine 치료를 받은 환자에서 약물반응이 일정하지 않고 약물치료 효과가 떨어지는 운동동요현상(motor fluctuation)의 빈도수와 심각성을 감소시킬 수 있다. 한편, Tolcapone은 간독성 및 급성심장성사망 등의 부작용으로 사용이 금지된 나라도 있다. Tolcapone은 음식물에 의해 흡수가 지연되고 생체이용률의 경미한 감소를 나타내지만 임상학적으로 큰 의미는 없으며 식사와 관계없이 투약할 수 있다. 대조적으로 Opicapone은 보통 또는 고지방 음식에 의해 흡수율과 흡수량이 감소하여 tmax의 지연, AUC 감소(약 31~51%) , Cmax 감소(약 62~68%) 등이 발생하므로 식전 1시간 또는 식후 1시간에 복용하여야 한다.
| COMT inhibitors - Food(Nutrients) | 특징 및 주의사항 |
|---|---|
| Opicapone + Fat meals | tmax지연, AUC 감소, Cmax 감소→식전 1시간 또는 식후 1시간에 복용 |
MAO-B 억제제(Selegiline, Rasagiline, Safinamide 등)는 Dopamine 대사 효소인 MAO-B를 선택적으로 차단하여 Levodopa의 작용시간을 연장한다. Selegiline은 고지방식과 함께 경구투여 시 생체이용률이 3배 이상 증가하는 것으로 나타났다. 이는 장관 혈류 증가와 식후 지연된 위배출에 기인한 것으로 추정된다. 따라서 Selegiline 정제는 식사와 함께 복용하여야 한다. 한편, Selegiline 구강붕해정(Orally Disintegrating Tablet, ODT)은 음식물 존재 시 AUC 와 Cmax가 40% 감소하므로 식전 5분 또는 식후 5분 후에 복용하여야 한다. Rasagiline과 Safinamide는 음식과 함께 투여 시 tmax 지연 및 Cmax의 감소가 있으나 AUC에 영향이 없으므로 음식과 무관하게 경구투여할 수 있다.
MAO-B와 다르게 MAO-A는 tyramine 대사에 관여한다. MAO-A 억제제를 tyramine이 풍부한 음식(숙성된 치즈, 훈연 또는 가공된 고기 및 생선, 절임식품 또는 발효식품, 와인, 생맥주 등)과 같이 복용하면 혈청 tyramine 수준이 증가하여 심한 두통, 한출, 빈맥, 호흡촉박 등을 동반한 고혈압성 위기를 초래할 수 있다(Cheese Effect). tyramine 경구투여와 MAO 억제제에 관한 연구에서 SBP(Systolic Blood Pressure)를 증가(예: 20, 25, 30mmHg)시키는데 필요한 tyramine 용량비율, 즉 TSF(Tyramine Sensitivity Factor)가 2 이상인 경우 임상적으로 관련이 있는 것으로 본다.
PD 치료에 사용되는 모든 MAO 억제제는 제시된 치료용량에서 MAO-B에 선택적이다(Selegiline 10mg: TSF=1.75~3.12, Rasagiline 1mg: TSF=2, Safinamide 100mg: TSF=2.15). 그러나 용량이 증가함에 따라 MAO-B의 선택성이 소실되어 MAO-A에도 결합하는 현상이 발생한다. 그 결과 TSF의 증가가 나타나고 현저한 혈압상승, 가슴 두근거림, 오심 등의 cheese effect 증상 발현의 위험성이 커진다. Selegiline과 Rasagiline에서 용량증가 시 cheese efect의 증상이 발현되었으며, 반면에 Safinamide는 MAO-B에 대한 선택성이 매우 우수하여 치료이상의 과용량(300~350mg)에서도 의미있는 TSF 변화가 나타나지 않았다.
따라서 모든 MAO-B 억제제 복약 환자에게 tyramine 함유 식품을 제한할 필요는 없지만, Selegiline의 경우 10mg/day, Rasagiline의 경우 2mg/day 이상의 용량이 (동반 우울증 치료등을 위해) 필요한 경우에는 tyramine이 풍부한 식품의 섭취를 제한하도록 권고하여야 한다. 그러나 진행된 PD 환자에서 식이요법이 불가한 경우에는 Selegiline 경피흡수제 등으로 약물 변경을 하는 것이 더 좋은 대안이 될 수 있다.
한편, MAO-B 억제제는 루이소체(Lewy Body)의 주성분인 Alpha-synuclein 응집의 핵생성 단계(nucleation phase) 지연으로 질병 진행률 감소효과가 있는 것으로 연구되었다.
| MAO-B inhibitors - Tyramine-rich foods | 특징 및 주의사항 |
|---|---|
| Selegiline: higher than 10mg/day | · cheese effect 위험성 증가: tyramine 풍부 식품 섭취 제한 필요 · Selegiline 경피흡수제로 약물변경을 고려 |
| Rasagiline: higher than 2mg/day | cheese effect 위험성 증가: tyramine 풍부 식품 섭취 제한 필요 |
| Safinamide: supratherapeutic doses (300-350mg) | no significant changes in TSF |
PD 환자에서 항콜린성 약물(Biperiden, Benztropine, Pridinol, Trihexyphenidyl 등)은 진전(tremor), 근육긴장이상(Dystonia), 타액분비 과다(Excessive Salivation) 등의 증상 개선을 위해 도움이 되지만, 노인환자에서 인지장애, 혼란, 시야혼탁, 변비 등의 부작용 발현으로 부적절하다.
한편, 항콜린성 약물과 KCL 장용 또는 서방성 제제를 병용하는 경우 KLC의 식도나 위점막에 대한 자극이 더욱 심화되며 심한 경우 위장관 출혈 위험성이 현저하게 증가하는 것으로 나타났다.
| Cholinolytics | 특징 및 주의사항 |
|---|---|
| Cholinolytics: Biperiden, Benztropine, Pridinol, Trihexyphenidyl | 노인환자에서 인지장애, 혼란, 시야혼탁, 변비 등의 부작용 발현으로 부적절: 주의 및 모니터링 필요 |
| Cholinolytics + 장용 KCI 또는 서방성 KCl 제제 | 위장관 출혈 위험성 증가: 주의 및 모니터링 필요 |
Amantadine은 IR(Immediate-Release)정, 캡슐, 시럽, ER(Extended-Release)정 등 다양한 제형으로 사용되는데, IR과 ER 제제를 Levodopa와 조합하여 이상운동증(Dyskinesia)과 약효소실현상(Wearing Off)을 감소지킬 복적으로 사용할 수 있다. Amatadine IR 제제는 초기 PD환자의 운동증상의 가벼운 개선을 위해 단독으로도 사용될 수 있다. 모든 Amantadine 제제의 생체이용률 지표는 음식과 무관한 것으로 알려져 있다.
Pimavanserin은 2세대 항정신병약(antipsychotic)으로서 PD환자에서 PD 관련 정신증(psychosis)을 치료하기 위해 사용되기도 한다. Pimavanserin정은 고지방 음식물에 의해 tmax는 현저하게 감소하지만 AUC와 Cmax는 영향을 받지 않으므로 식사와 무관하게 투약할 수 있다.
진행된 PD 노인환자들은 투약과 관련된 부작용, 약물-약물 상호작용, 약물-음식 상호작용의 고위험군이므로 주의가 필요하다. 이는 다제약물, 자가 OTC 제제 및 보조식품, 복약법 준수 부족, 노화에 따른 약물동태학적(Pharmacokinetic) 및 약력학적(Pharmacodynamic) 변화 등에 기인한다.
| 노인 PD 환자의 약동학 및 약력학적 특징 |
|---|
| Pharmacokinetic Changes: 위내 pH 증가, 위 배출 감소, BBB의 투과성 증가, 간 대사 감소, 배설과정 저하 등 |
| Pharmacodynamic Changes: Deficiency of Dopamine Transporters and Uptake Sites. Increased Sensitivity to Dopamine |
- References
Nobuyuki Ishii, Hitoshi Mochizuki, Katsuya Sakai, Go Ogawa, Kazutaka Shiomi, Masamitsu Nakazato; Polypharmacy Associated with Cognitive Decline in Newly Diagnosed Parkinson’s Disease: A Cross-Sectional Study. Dement Geriatr Cogn Disord Extra 25 June 2020; 9 (3): 338–343. https://doi.org/10.1159/000502351.
Rosebraugh M, Voight EA, Moussa EM, Jameel F, Lou X, Zhang GGZ, Mayer PT, Stolarik D, Carr RA, Enright BP, Liu W, Facheris MF, Kym PR. Foslevodopa/Foscarbidopa: A New Subcutaneous Treatment for Parkinson's Disease. Ann Neurol. 2021 Jul;90(1):52-61. doi: 10.1002/ana.26073. Epub 2021 May 4. PMID: 33772855; PMCID: PMC8251848.
Agnieszka W, Paweł P, Małgorzata K. How to Optimize the Effectiveness and Safety of Parkinson's Disease Therapy? - A Systematic Review of Drugs Interactions with Food and Dietary Supplements. Curr Neuropharmacol. 2022;20(7):1427-1447. doi: 10.2174/1570159X19666211116142806. PMID: 34784871; PMCID: PMC9881082.
Wills AM, Eberly S, Tennis M, Lang AE, Messing S, Togasaki D, Tanner CM, Kamp C, Chen JF, Oakes D, McDermott MP, Schwarzschild MA; Parkinson Study Group. Caffeine consumption and risk of dyskinesia in CALM-PD. Mov Disord. 2013 Mar;28(3):380-3. doi: 10.1002/mds.25319. Epub 2013 Jan 21. PMID: 23339054; PMCID: PMC3608707.
Tan YY, Jenner P, Chen SD. Monoamine Oxidase-B Inhibitors for the Treatment of Parkinson's Disease: Past, Present, and Future. J Parkinsons Dis. 2022;12(2):477-493. doi: 10.3233/JPD-212976. PMID: 34957948; PMCID: PMC8925102.
Copyright © MediGloPark's All Rights Reserved.
노인 당뇨병과 다제약물
 제2형 당뇨병 환자에서 다제약물은 동반질환으로 인해 발생하는 경우가 많다. 특히 노인환자의 경우 신기능 및 간기능의 저하, 불규칙한 식사,
여러 약물의 상호작용에 의한 저혈당 위험, 저혈당 인지기능 저하 및 느린 회복 등으로 인해 주의가 필요하며, BMI≥25kg/㎡인 경우도 위험 인자가 된다.
제2형 당뇨병 환자에서 다제약물은 동반질환으로 인해 발생하는 경우가 많다. 특히 노인환자의 경우 신기능 및 간기능의 저하, 불규칙한 식사,
여러 약물의 상호작용에 의한 저혈당 위험, 저혈당 인지기능 저하 및 느린 회복 등으로 인해 주의가 필요하며, BMI≥25kg/㎡인 경우도 위험 인자가 된다.고혈당 관리 뿐만아니라 미세혈관 합병증(Microvascular complication: Diabetic nephropathy, Neuropathy, Retinopathy 등), 대혈관 합병증(Macrovascular complication: Coronary artery disease, Peripheral arterial disease, Stroke 등), 당뇨병 관련 노인병(인지기능 손상, 낙상, 요실금 등), 그리고 약물 부작용 등을 포함한 관리과정에서 당뇨환자가 복용해야 하는 약물의 수가 증가한다. 또한 제2형 당뇨병 환자에서 당뇨 이외에 고혈압, 이상지질혈증과 같은 질병의 치료제가 같이 사용되어야 하는 경우가 빈번하며, 처방약 외에 환자가 스스로 구입하여 복용하는 OTC 약물 및 건강보조식품들도 다양하게 상호작용을 나타내므로 이로 인한 다제약물의 위험성이 더욱 증가한다.
한편, 항당뇨약 사용 과정에서 저혈당은 낙상(항고혈압약 병용 시 위험성 증가), 부정맥, 사망 등 심각한 위험성 증가의 원인이므로 저혈당 증상과 대처방법에 대한 교육이 환자 및 보호자 모두에게 필요하다, 노인 당뇨병환자에서 심혈관질환 위험인자들의 치료 여부는 이를 통해 얻을 수 있는 이익과 환자의 건강 상태 등을 고려해서 결정하는데 금연, 혈압조절(<140/85mmHg), 이상지질혈증 치료 등이 중요하다.
| 노인 당뇨병 환자의 건강관리 | |
|---|---|
| 심혈관질환 위험인자 관리 | · 금연, 혈압조절(<140/85mmHg), 이상지질혈증 치료 |
| 운동과 임상영양요법 | · 혈당, 혈압, 지질 및 체중관리에 도움 · 특별한 문제가 없다면 일주일에 최소 150분의 유산소 운동 + 적절한 저항운동(근력운동) · 잘못된 식생활 습관, 치아문제, 미각감소, 소화기능장애, 경제적 또는 환경적 문제 등으로 식생활 조절곤란 발생 가능 |
| 당뇨병성 합병증의 선별검사 | · 개별화하여 시행하며, 특히 기능장애와 관련된 검사에 주안점을 둔다. |
| 인지기능장애 및 치매 | · 선별검사를 고려 |
노인 당뇨병 환자의 혈당조절 목표는 신체 및 인지기능, 기대여명 등을 평가하여 개별화하는데, 적극적인 치료로 인한 저혈당의 위험 등 부작용의 위험이 더 클 수 있으므로 혈당조절 목표치를 덜 엄격하게 유지한다.
| AGS 제시 HbA1c 수치 | |
|---|---|
| 건강한 노인 | 7.0~7.5% 또는 그 이하 |
| 일반적인 목표치 | 7.5~8.0% |
| 여러 동반질환+짧은 기대여명 | 8.0~9.0% |
반감기가 긴 Sulfonylurea 및 Insulin 사용 시 저혈당 발생에 주의하여야 하며 Metformin은 신부전 환자에서 금기이다. 또한 Metformin은 식욕부진을 유발하므로 저용량으로 시작하고 증상이 있을 경우에는 감량 또는 중단을 고려하여야 한다. 저혈당을 거의 유발하지 않는 경구 혈당강하제(Oral Hypoglycemic Agent, OHA)는 Metformin (Glucophage), Thiazolidinediones (TZDs), Dipeptidyl peptidase-4(DPP-4) 억제제, Alpha-glucosidase inhibitor 등이다.
특히 노인 당뇨병 환자는 입원이 필요할 정도의 낙상 위험이 크므로 인슐린 사용, 낙상의 경험, 선 자세 균형 점수 부진(poor standing balance score), A1c≥8% 등 위험인자들에 노출된 경우 더욱 주의하여야 한다. 노인 당뇨병 환자의 낙상에 의한 골절 위험성은 골밀도 감소 부작용이 있는 TZDs 복용 시 더욱 증가하며 65세 이상의 여성 당뇨환자에서 더욱 위험성이 증가한다.
당뇨환자의 낙상 위험성을 줄이기 위한 방법은 다음과 같다.
| 당뇨병 환자의 낙상 위험 감소 원칙 |
|---|
| · 모든 처방약과 OTC 약제를 검토하여 낙상 고위험 약제를 확인 |
| · 약제의 수와 용량을 제한 |
| · 저혈당 및 고혈당 회피 |
| · 환자 및 보호자에게 저혈당의 신호와 증상, 그리고 대처 방법에 대해 교육 및 상담 |
혈당강하제는 크게 OHA와 주사형 혈당강하제로 나눌 수 있다.
| 혈당강하제 | 특징 및 주의사항 |
|---|---|
| ▷Biguanide: · Metformin |
▷ 기전: ① 간 Glucose 생성 감소 ② Glucose 이용 증가 ③ Insulin 저항성 감소 ▷ A1c(%): 1~2 ▷ 장점: ① 체중감소(비만환자) ② Cardiovascular Protection ③ No hypoglycemia ④ 저가(Low cost) ▷ 단점: ① 신부전 환자 금기(GFR<30ml/min/1.73㎡) ② 식욕부진 유발 ③ 젖산산증(Lactic acdosis)(rarely) ④ 위장관계 부작용(설사, 구기) ⑤ Metformin 유도 비타민 B12 결핍성 신경병(간접적 낙상위험) 및 인지기능 손상 주의 |
| ▷ DPP-4 Inhibitors: · Sitagliptin · Vildagliptin · Saxagliptin · Linagliptin · Gemigliptin · Teneligliptin · Alogliptin · Evogliptin · Anagliptin |
▷ 기전: ① Incretin 작용 증가 ② Insulin 분비 증가 ③ Glucagon 분비 감소 ▷ A1c(%): 0.5~0.8 ▷ 장점: ① No Hypoglycemia ② Well tolerated ③ Weight neutrality ▷ 단점: ① Angioedema/urticarial ② Acute pancreatitis: 췌장염 위험환자 부적절 ③ Renal dosing: 신장기능에 따라 용량 조절 필요 |
| ▷ Sodium-glucose co-transporter 2(SGLT2) Inbitors: · Dapagliflozin · Empagliflozin · Ertugliflozin · Ipragliflozin |
▷ 기전: Glucose 배출 증가 ▷ 장점: ① No Hypoglycemia ② 체중감소(비만환자) ③ 혈압저하 ④ CVD 환자에서 CVD 이벤트 비율 및 CVD 환자 사망률 감소 ▷ 단점: ① Genitourinary infections(Glucose 뇨배설 관련) ② 다뇨증(Polyuria) ③ Volume depletion(포도당 배설 관련 다뇨로 인함) ④ 저혈압(volume 저하로 인함) ⑤ 어지럼증 ⑥ Diabetic ketoacidosis ⑦ Renal dosing: 신장기능에 따라 용량 조절 필요 ▷ 주의: 적절한 수분섭취 필요 |
| ▷ Sulfonylureas: · Glibenclamide · Glimepiride · Glipizide |
▷ 기전: Insulin 분비 증가 ▷ A1c(%):1~2 ▷ 장점: 저가(low cost) ▷ 단점: ① 저혈당(Hypoglycemia) 위험성(특히↑↑) 증가(←긴 반감기+Insulin 분비 증가 기전) → 노인 주의(BEERS criteria, STOPP/START) ② 체중증가(Weight gain) |
| ▷ Meglitinides: · Repaglinide · Mitiglinide · Nateglinide |
▷ 기전: Insulin 분비 증가 ▷ A1c(%): 1~2 ▷ 장점: ① Short onset of action ② Short duration ③ Lower Postprandial glucose(PPG): 식후 고혈당 치료에 사용 ▷ 단점: ① Hypoglycemia(sulfonylurea보다 덜함←Short duration) ② 체중증가 ③ 고가(Expensiveness) |
| ▷ Glitazones (Thiazolidinediones, TZD): · Pioglitazone · Lobeglitazone · Rosiglitazone |
▷ 기전: Insulin 저항성 감소 ▷ A1c(%): 0.5~1.4 ▷ 장점: ① No hypoglycemia ▷ 단점: ① 울혈성 심부전(CHF) 악화(수분저류 등으로 인한) → 노인 주의(BEERS criteria, STOPP/START): 중증 심부전 환자 금기 ② 골절(Fracture) 위험 증가 → 노인 주의 ③ 체중증가(수분저류 등으로 인한) ④ 수분저류 ⑤ 고가(Expensiveness) ⑥ Rosiglitazone-MI |
| ▷ Alpha Glucosidase Inhibitors: · Acarbose · Voglibose |
▷ 기전: Glucose 흡수 감소 ▷ A1c(%): 0.5~0.8 ▷ 장점: ① Weight neutrality ② Lower PPG ③ No hypoglycemia ▷ 단점: ① 위장관계 부작용(고창, GI flatulence): 만성 장질환자 등 부적절 ② 간기능 검사 필요 |
| ▷ Insulin: short acting(inj.): |
▷ 주의; 장시간 지속형 인슐린 없이 속효성 인슐린을 이용한 sliding scale: 고혈당 관리 개선없이 저혈당 위험 증가 → 노인 주의(BEERS criteria) |
| ▷ Insulin: long acting(inj.): · Insulin glargine(Lantus) · Insulin detemir(Levemir) |
|
| ▷ Glucagon-like peptide-1(GLP-1) Agonist(inj.): |
처음 제2형 당뇨로 진단되는 경우 Metformin과 같은 OHA 단독요법으로 시작하며, 혈당강하 효과가 목표치에 도달하지 못하면 2제 또는 3제 병합요법을 시행한다.
| 당뇨 치료 기준 | 2형 당뇨 치료 가이드라인 | 비고 |
|---|---|---|
| 첫 진단시 당화혈색소 < 7.5% | 생활습관 조절 + Metformin 단독요법 | |
| 초기 당화혈색소 ≥ 7.5% 또는 단독요법으로 3개월 이내 목표치에 도달하지 못한 경우 | 2제 요법 | |
| 2제 병합요법으로도 3개월 이내 목표에 도달하지 못한 경우 | 3제 요법 | 환자의 혈당조절이 매우 곤란한 상태 |
OHA 3제 요법으로 HbA1c가 목표치에 도달하지 못하거나 첫 진단 시 증상 발현과 함께 당화혈색소가 9.0% 이상일 때는 Basal Insulin에 OHA를 병용할 수 있으며, 그럼에도 HbA1c 목표치 달성이 안되면 Prandial Insulin, GLP-1 RA(Glucagon-Like Peptide 1 Receptor Agonist) 등을 추가할 수 있고, Premixed Insulin으로 전환할 수 있다.
OHA 치료 실패의 경우에 GLP-1 RA +/- OHA를 사용할 수 있고, 또는 Basal Insulin +/- OHA 후 HbA1c 목표치 달성이 안되면 GLP-1 RA 또는 Prandial Insulin을 x1 또는 x2(→ HbA1c 목표치 달성이 안되면 x2 또는 x3)을 사용할 수 있으며, Premixed Insulin x1 또는 x2 +/- OHA(→ HbA1c 목표치 달성이 안되면 Premixed Insulin x2 또는 x3 +/- OHA)를 사용할 수 있다.
| Insulin 사용 기준 | 1단계 | 2단계 |
|---|---|---|
| 첫 진단 시 증상발현 + HbA1c > 9.0% | Basal Insulin +/- OHAs | ▷ Intensification: · Add Prandial Insulin · Add GLP-1 RA · Switch to Premixed Insulin |
| OHA Failure | GLP-1 RA +/- OHA | |
| OHA Failure | Basal Insulin +/- OHA | GLP-1 RA |
| OHA Failure | Basal Insulin +/- OHA | Prandial Insulin x1 or x2 ⇒ Prandial Insulin x2 or x3 (3단계) |
| OHA Failure | Premixed Insulin x1 or x2 +/- OHA | Premixed Insulin x2 or x3 +/- OHA |
인슐린 주사제 사용의 경우 특히 저혈당에 주의하여야 한다. 저혈당은 혈장 포도당 농도가 낮으면서(70mg/dL 미만), 자율신경 항진 또는 신경당 결핍 증상이 있고, 포도당 섭취 혹은 투여로 혈당이 정상으로 회복되면 이러한 증상이 소실되는 경우이다.
인슐린에 의한 저혈당 발생과 관련하여 인슐린, 인슐린 유사체, 인슐린 분비 촉진제(Insulin secretagogues : Meglitinides, Sulfonylureas) 등이 저혈당 발생 위험성이 있으나, 인슐린 유사체들의 경우는 저혈당 발생 위험성이 상대적으로 덜하다.
| 인슐린 저혈당 위험성 비교 |
|---|
| Long-acting Insulins: Insulin glargine(Lantus), Insulin detemir(Levemir) < NPH(Humulin N; Novolin N) |
| Rapid-acting insulin analogs: Lispro(Humalog), Aspart(Novolog), Glulisine(Apidra) < Regular insulin(Humulin R; Novolin R) |
저혈당의 증상은 떨림, 불안, 혼란, 두근거림, 공복감 등이며 저혈당 무감지증이나 자율신경병증을 동반한 환자의 경우에는 증상이 없을 수 있으므로 주의가 필요하다. 또한 베타차단제을 복용중인 경우 저혈당의 증상이 가려질 수 있으므로 주의가 필요하다. 심한 경우 의식소실, 발작, 혼수상태가 발생한다.
특히 노인에서 인지기능 장애는 저혈당 발생의 강력한 위험인자 중 하나이며, 발생된 저혈당은 다시 인지기능 손상에 영향을 준다.
| 저혈당 단계 | 혈당수준 | 특징 |
|---|---|---|
| 1단계: 주의 필요 저혈당(Hypoglycemia Alert Value) | <70mg/dL ≥54mg/dL |
탄수화물을 즉시 섭취하거나 약제 종류 및 용량조절을 시행해야 할 정도의 저혈당 |
| 2단계: 임상적으로 명백한 저혈당(Cinically Signifiant Hypoglycemia) | <54mg/dL | 저혈당 방어체계의 장애를 유발할 정도의 저혈당 중증 저혈당, 치명적인 부정맥, 사망의 위험이 유의미하게 증가함 |
| 3단계: 중증 저혈당(Severe Hypoglycemia) | 특정 포도당 역치 수준이 없음 | ▷ 저혈당 해결을 위한 외부의 도움이 필요한 수준 ▷ 제2형 당뇨병환자에서 중증 저혈당 발생의 위험인자: 이전 중증 저혈당의 과거력, 저혈당 무감지증, 자율신경병증 동반자, 만성질환 또는 중증질환 이환자, 고령 또는 청소년 이하의 어린이, 저체중, 신기능 장애, 인슐린 및 설폰요소제 사용, 엄격한 혈당조절 또는 지나치게 낮은 당화혈색소, 오랜 당뇨병 유병기간 등. |
저혈당 발생 시는 15~20그람의 포도당 또는 이를 함유한 탄수화물을 섭취하여 치료를 한다.
| 저혈당 치료 시 주의사항 |
|---|
| · 지방이 포함된 초콜릿, 아이스크림은 흡수속도가 느려 부적합. |
| · 저혈당 회복 후 간식이나 식사를 하여 저혈당 재발 방지. 과잉 치료 시 반동 고혈당 야기 |
| · 중증 저혈당의 경우는 응급실 또는 가까운 의료기관 방문 |
| ▷ 단순당질 15~20g에 해당하는 음식의 예 · 설탕 한 숟가락(15g) · 꿀 한숟가락(15mL) · 주스 또는 청량음료 3/4컵(175mL) · 요구르트 1병(100mL 기준) · 사탕 3~4개 |
당뇨환자의 OHA 적절성은 약물의 필요성 및 유효성, 복약 순응도, 안전성 등을 종합적으로 검토하여 평가하여야 한다.
| OHA 적절성 평가 | 약물요법 최적화 계획 |
|---|---|
| ▷ 약물 필요성 및 유효성 평가 · 혈당 조절 적절성 확인 |
· 환자의 특성을 고려하여, 혈당 조절 적절성을 파악하고, 약에 대한 복약 순응도 및 생활습관 조정 적절성을 파악하여 필요 시 의료진 알림을 통하여 약물요법 조정을 시행함. |
| ▷ 복약 순응도 평가 · 처방 용량, 용법 준수 평가 · 복약 순응도 평가 · 운동 및 영양요법 준수에 대한 평가 |
· 각 계열별 복용 시간 및 용법, 용량 준수 확인 · 복약 순응도에 문제가 확인 된 경우→교육시행 · 노인환자 혈당조절 어려움은 복약불이행과 관련되어 있을 가능성이 있음. · 운동 및 영양요법 수행에 어려움을 야기하는 요인 확인 및 교육수행 |
| ▷ 안전성 평가 ① 병용약물 평가 · 베타차단제: 저혈당 증상을 매스킹. 혈당에 영향 · 혈당 상승에 영향을 주는 약제: 코르티코스테로이드, 비정형 향정신병 약제, Calcineurin inhibitor등 · Metformin: 조영제와 병용금기 · 주요한 약물상호작용 검토 및 평가 ② 위험상병 확인 · Metformin: 신기능 저하 환자 · DPP-4저해제: 신기능 저하 환자, 췌장염 환자 · SGLT-2 저해제: 신기능 저하 환자 · Glitazone:심부전 환자(NYHA class III~IV), 중증 간질환 · α-Glucosidase inhibitor: 장관 폐색 환자, 만성 장관 질환 환자, 중증 간질환 환자 · Sufonylurea: Sulfonamide 과민반응. 신기능 저하 환자 ③ 부작용 확인 · Metformin: 젖산혈증(젖산산증), 식욕감퇴, 설사, 오심, 노쇠 환자에서 체중감소 주의(사망률 증가), Metformin 유도 비타민 B12 결핍성 신경병 및 인지기능 손상 주의 · Sulfonylurea, Meglitinide: 저혈당 · SGLT-2 저해제: 다뇨, 탈수 및 저혈압, 요로감염, 노쇠 환자에서 체중감소 주의(사망률 증가) · Glitazone: 간수치 상승, 수분 저류, 체중 증가, 심부전 악화 · α-Glucosidase inhibitor: 고창, 복통, 설사 · 저혈당 경험 확인 · 저혈당 위험요인 확인: 이전 중증 저혈당의 과거력, 자율신경병증 동반, 만성질환자 또는 중증질환 이환자, 고령, 저체중, 신기능 장애, 오랜 유병기간, 인지기능 장애 · 주사 부위 이상: 지방 비후, 염증 등 |
· 혈당조절에 어려움이 있는 환자에서 혈당상승에 영향을 주는 약제의 병용을 확인하고 의료진 알림을 시행. · CT 검사 시 Metformin의 일시적인 사용 중단의 필요성을 교육 · 신기능 저하 환자: 약물 변경 또는 용량 조정의 필요성을 판단하고 의료진 알림을 통하여 조정할 수 있도록 함. · 금기 질환이 확인된 경우: 의료진 알림을 통하여 약물요법 변경을 고려함. · Metformin의 위장관 부작용: 식사와 복용 시 경감 가능. 용량조정 필요. · 다뇨, 탈수를 보이는 경우: 적절한 수분 섭취를 교육. 요로감염은 의료진 알림 통해 치료가 필요함. · 간수치 상승: 그 정도에 따라 약물 조정 중재를 검토 · 저혈당 경험이 있는 환자의 경우: 저혈당 발생과 관련한 위험요인 확인 및 대처방안에 대한 교육이 필요. 의료진에게 해당사실을 알려 약물요법의 조정을 고려함. ·주사 부위 이상이 확인된 경우: 해당부위를 피하여 주사하도록 안내하고 의료진 알림을 시행 |
당뇨병 환자에 대한 약료 상담은 환자의 적응증 인지 여부, 복용 행태, 약물의 효과, 복약의 순응성, 식이요법, 운동요법, 동반질환 여부(특히 약물-질병 상호작용과 신장 또는/그리고 심장 질환 등 동반 여부 확인 및 평가), 병용약(진통제 등 OTC 약물 포함) 및 약물-약물 상호작용 평가, 부작용(저혈당 증상, 부종, 체중 증가, 어지러움, 설사, 구기, 식욕부진, 비뇨생식기 감염, 다뇨 등)의 확인 등을 포함한다.
| ▷ 질환명(60대, F) : 당뇨, 심근경색, 고혈압, 우울증 |
▷ 사용 약물: Aspirin 100mg qd, Lisinopril 30mg qd, Amlodipine 10mg qd, Atenolol 50mg qd, Metformin 1000mg bid, Glimepiride 4mg qd, Pioglitazione 30mg qd, Escitalopram 10mg qd, Omeprazole 20mg qd, Furosemide 40mg qd / Naproxen(OTC) |
|---|---|
| 약료 상담의 예 | 중재 예시 |
| ① 적응증: 복용 이유 인지 여부 확인 ② 복용 행태 및 효과: 복용시간, 복약의 순응성, 규칙적인 식사, 식이요법, 운동요법 등 확인 ③ 고위험 동반 질환: 신장질환, 심장질환 동반 여부 확인. 소변검사 등 확인 ④ 병용약, 상호작용: 진통제 등 다른 약 복용 여부 확인 ⑤ 부작용: 저혈당 증상(어지러움, 식은 땀, 가슴 두근거림) 경험 여부, 부종, 설사, 울렁거림 등 확인 |
· 복약 순응도를 평가하여 규칙적 복용을 교육 · 통증 완화 목적의 NSAID(Naproxen) 복용: ACEI(신배설 약물. CKD Stage 4~5에서 부적절. Stage1~3에서는 질병악화를 지연), 이뇨제 복용으로 신기능 저하의 위험이 높고 심혈관질환 및 고혈압 고려 시 NSAID 사용이 부적절. 진통제 변경이 필요함. 신기능 검사 고려. · Pioglitazone: 부종 및 체중 증가 위험성이 있어 (부종으로 Furosemide 복용 중) 의료진의 검토가 필요함. · 혈당조절을 위한 식이요법과 운동요법의 필요성을 교육 · Omeprazole: 장기간 복용 시 지속 필요성 평가가 필요. 노인 환자에서 8주를 초과한 사용은 부적절함. |
인슐린은 속효성, 초속효성, 중간형, 장시간형, 혼합형 등이 있다.
| 구분 | 성분 | 제품명 |
|---|---|---|
| 속효성 | Regular insulin | 휴물린-R |
| 초속효성 | Insulin lispro, Insulin aspart, Insulin glulisine | 휴마로그, 노보래피드, 애피드라 |
| 중간형 | NPH | 휴물린-N |
| 장시간형 | Insulin glargine, Insulin detemir, Insulin degludec | 란투스/투제오, 레버미어, 트레시바 |
| 혼합형 | Aspart+NPA Lispro+NPL Aspart+Degludec NPH+Regular |
노보믹스 플렉스펜 휴마로그믹스 퀵펜 리조덱플렉스터치주 휴물린 70/30 퀵펜 주 |
Insulin 펜형 사용법과 주의사항은 다음과 같다,
| Insulin 펜형 사용법 체크 리스트 |
|---|
| ① 투여전 손 씻기 |
| ② 주사 부위: 가장 흔히 복부(배꼽 주변은 2~3cm 피함), 상완, 엉덩이, 허벅지의 바깥 부분, 주사 부위는 최소 1cm 간격 유지(주사부위표 활용) |
| ③ 주사 부위 이상 확인: 지방비후, 염증, 부종 및 감염 |
| ④ 주사 투여 전 약액의 확인(공기방울, 부유물 등) 및 필요 시 약액 흔들기(중간형 인슐린이 섞여 있는 경우) |
| ⑤ 주사 바늘 끼우는 법: 펜 소독 후 일직선으로 연결 |
| ⑥ 주사 투여 전 priming(약액 맺힘 확인) 및 단위조작 |
| ⑦ 주사부위 소독 |
| ⑧ 주사액 투여법: 수직으로 찌르기→10초 기다리기→누른 채로 빼기. * 5mm이상의 바늘을 사용할 경우 피부 집어 올리기 |
| ⑨ 주사 후 바늘 제거 후 바늘의 올바른 폐기 |
| ⑩ Insulin 보관법: 개봉 전 냉장. 개봉 후 상온 1개월. 유효기간 확인.올바른 휴대법 |
| ⑪ 다른 사람과의 주사제 공유 금지 |
| 펜형 인슐린 주사법 (BD-Korea: Insulin Injection Technique) https://www.youtube.com/watch?v=ZSk2moRGEG0 |
Insulin 주사 시 통증을 줄이는 방법은 다음과 같다.
| 인슐린 주사 시 통증을 줄이는 방법 |
|---|
| 4mm의 짧고 가는 인슐린 주사바늘 사용 |
| 상온의 인슐린 사용: 냉장 보관 시 미리 15분 전에 꺼내놓기 |
| 알코올이 완전히 마른 후 주사 |
| 피부에 부드럽게 삽입 |
| 주입 버튼은 천천히 |
| 찔렀을 때와 동일한 각도로 빼기 |
| 주사바늘 재사용 금지 |
인슐린 펜형 적절성 평가는 OHA와 마찬가지로 약물의 필요성 및, 유효성 평가, 약제 순응도 평가, 안전성 평가 등을 포함한다.
| 적절성 평가 | 약물요법 최적화 계획 |
|---|---|
| ▷ 약물 필요성 및 유효성 평가 · 혈당 조절 적절성 확인 |
· 환자의 특성을 고려하여 혈당 조절 적절성을 파악 · 약에 대한 순응도 및 생활습관 조정 적절성을 파악 · 필요 시 의료진 알림을 통하여 약물요법 조정을 시행 |
| ▷ 복약 순응도 평가 ① 처방용량, 용법 준수 평가 ② 약제 순응도 평가 ③ 운동 및 영양요법 준수에 대한 평가 |
· 투여시간, 인슐린 주사 방법 적절성 확인 · 노인환자 혈당 조절 어려움은 약제 사용 불이행과 관련되어 있을 가능성이 있음. · 운동 및 영양요법 수행에 어려움을 야기하는 요인 확인 및 교육 수행. |
| ▷ 안전성 평가 ① 주사 부위 이상: 지방 비후, 염증 등 ② 저혈당 위험요인 확인: 이전 중증 저혈당의 과거력, 자율신경병증 동반, 만성질환자 또는 중증질환 이환자, 고령, 저체중, 신기능 장애, 오랜 유병기간, 인지기능 장애 |
· 주사 부위 이상이 확인된 경우: 해당부위를 피하여 주사하도록 안내하고 의료진 알림을 시행. · 저혈당 경험이 있는 환자의 경우: 저혈당 발생과 관련한 위험요인 확인 및 대처방안에 대한 교육이 필요. 의료진에게 해당사실을 알려 약물요법의 조정을 고려함. |
OHA 및 인슐린 주사제를 사용하는 당뇨병 환자에 대한 약료 상담은 OHA의 경우와 마찬가지로 환자의 적응증 인지 여부, 복용 행태, 약물의 효과, 복약의 순응성, 식이요법, 운동요법, 동반질환 여부(특히 약물-질병 상호작용과 신장 또는/그리고 심장 질환 등 동반 여부 확인 및 평가), 병용약(진통제 등 OTC 약물 포함) 및 약물-약물 상호작용 평가, 부작용(저혈당 증상, 부종, 체중 증가, 어지러움, 설사, 구기, 식욕부진, 비뇨생식기 감염, 다뇨 등)의 확인 및 인슐린 주사제 사용으로 인한 주사 부위 병변 등 부작용 확인, 주사제 보관 상태, 주사제 사용법 확인, 주사침 폐기법 등을 포함한다.
| ▷ 질환명(70대 후반, M): 고혈압, 당뇨, 골관절염 |
▷ 사용 약물: Lisinopril 20mg qd, Amlodipine 5mg qd, Aspirin 100mg qd, Lantus 30units sc qd, Metformin 500mg bid, Acetaminophen 325mg 1~2tablets 매 6시간마다 필요 시 복용, Tramadol 50mg 매 6시간마다 필요시 복용(하루 1회 이하 복용), Zolpidem 5mg 취침 시(필요 시) 복용 |
|---|---|
| 약료 상담의 예 | 중재 예시 |
| ① 적응증: 복용 이유 인지 여부 확인 ② 복약, 사용 행태 및 효과: 혈당 조절 상태 확인. 인슐린 주사제의 개봉 전 보관, 사용 중 보관, 인슐린 주사제 사용법 인지 여부, 주사침의 폐기법 등 확인. OHA의 복용시간, 복약의 순응성, 규칙적인 식사, 식이요법, 운동요법 등 확인 ③ 고위험 동반 질환: 신장질환, 심장질환 동반 여부 확인. 당뇨 합병증(신경병증) 확인. 소변검사 등 확인 ④ 병용약, 상호작용: 진통제 등 다른 약 복용 여부 확인 ⑤ 부작용: 저혈당 증상(어지러움, 식은 땀, 가슴 두근거림) 경험 여부, 주사 부위 부작용 여부 확인, 설사, 울렁거림 등 확인 |
· 당뇨환자는 정기적 신기능 검사가 좋음. · 순응도를 평가하여 규칙적 복용 및 사용을 교육 · 인슐린 주사는 개봉하지 않은 것은 냉장보관하고 사용 중인 것은 상온보관하에 1개월 사용 가능. · 주사 후 바늘을 반드시 분리하고 뚜껑이 있는 빈병에 모아 밀봉하여 폐기함. · 저혈당 증상이 나타날 수 있으므로 사탕을 휴대. · 저혈당 증상을 경험한 경우 의료진과 상의하여 약물 조정을 하여야 함. · 혈당조절을 위한 식이요법과 운동요법의 필요성을 교육함. |
- References
Dobrică EC, Găman MA, Cozma MA, Bratu OG, Pantea Stoian A, Diaconu CC. Polypharmacy in Type 2 Diabetes Mellitus: Insights from an Internal Medicine Department. Medicina (Kaunas). 2019 Aug 3;55(8):436. doi: 10.3390/medicina55080436. PMID: 31382651; PMCID: PMC6723949.
Peron EP, Ogbonna KC, Donohoe KL. Antidiabetic medications and polypharmacy. Clin Geriatr Med. 2015 Feb;31(1):17-27, vii. doi: 10.1016/j.cger.2014.08.017. Epub 2014 Oct 16. PMID: 25453298; PMCID: PMC4860345.
Peron EP, Ogbonna KC, Donohoe KL. Antidiabetic medications and polypharmacy. Clin Geriatr Med. 2015 Feb;31(1):17-27, vii. doi: 10.1016/j.cger.2014.08.017. Epub 2014 Oct 16. PMID: 25453298; PMCID: PMC4860345.
Horii, T., Iwasawa, M., Kabeya, Y. et al. Polypharmacy and oral antidiabetic treatment for type 2 diabetes characterised by drug class and patient characteristics: A Japanese database analysis. Sci Rep 9, 12992 (2019). https://doi.org/10.1038/s41598-019-49424-2.
Pantelis Sarafidis, Use of ACEi/ARBs, SGLT2 inhibitors and MRAs can help us reach the therapeutic ceiling in CKD, Clinical Kidney Journal, Volume 17, Issue 2, February 2024, sfae014, https://doi.org/10.1093/ckj/sfae014.
Mukoyama, M., Kuwabara, T. Role of renin-angiotensin system blockade in advanced CKD: to use or not to use?. Hypertens Res 45, 1072–1075 (2022). https://doi.org/10.1038/s41440-022-00902-7.
MOMONIAT AND COLLEAGUES. ACE inhibitors and ARBs: Managing potassium and renal function. CLEVELAND CLINIC JOURNAL OF MEDICINE VOLUME 86 • NUMBER 9 SEPTEMBER 2019.
Giulio A. Cinotti, Pietro C. Zucchelli, Effect of Lisinopril on the progression of renal insufficiency in mild proteinuric non‐diabetic nephropathies, Nephrology Dialysis Transplantation, Volume 16, Issue 5, May 2001, Pages 961–966, https://doi.org/10.1093/ndt/16.5.961.
Hershon KS, Hirsch BR, Odugbesan O. Importance of Postprandial Glucose in Relation to A1C and Cardiovascular Disease. Clin Diabetes. 2019 Jul;37(3):250-259. doi: 10.2337/cd18-0040. PMID: 31371856; PMCID: PMC6640888.
대한약사회 사이버연수원 학술자료(2024년).
Copyright © MediGloPark's All Rights Reserved.
디곡신(Digoxin)과 노인 다제약물
 ▷ Digoxin은 심방세동과 심부전에 사용되는 일반적인 약 중의 하나이지만, 치료지수가 작고 지속적인 모니터링이 필요하므로 사용이 제한적이다.
▷ Digoxin은 심방세동과 심부전에 사용되는 일반적인 약 중의 하나이지만, 치료지수가 작고 지속적인 모니터링이 필요하므로 사용이 제한적이다. 특히 노인에서 Digoxin을 심방세동이나 심부전의 일차 선택약으로 사용하는 것은 부적절하다. 심방세동에 대한 더 효과적인 대체약이 있고(대체약이 효과가 없으면 사용을 고려), 사망률 증가와 관련이 있을 수 있기 때문이다. 심부전에서도 입원률 감소 효과에 대한 의문이 있으며 사망률 증가와도 관련이 있을 수 있는 것으로 보고되었다.
노인에서는 Digoxin 독성의 발생이 비교적 빈번하며 노인 Digoxin 독성에 대한 진단도 어려운 경향이 있다. 특히 신기능의 저하, 체질량(body mass), 다제약물, 가능한 여러 상호작용등 다양한 변수들로 인해 노인에서 Digoxin의 약동학적 변화는 매우 중요하다.
| 질병, 증후 | 노인 주의사항 | 비고 |
|---|---|---|
| 심부전, 심방세동 | · Digoxin > 0.125mg/d 용량투여 부적절 · 신기능 감소 시 독성 증가 위험 · Stage 4, 5 만성 신질환 환자는 더 용량 감량이 필요함: 고용량은 추가적 이익이 없이 독성 위험이 증가하며, 1주 1회 사용의 경우도 가능함 |
BEERS Criteria |
| GFR < 30ml/min 환자 | Digoxin > 0.125mg/d 용량투여는 Digoxin 독성 위험성 증가(혈중농도 모니터링 필요) | STOPP |
| 정상적 심실기능의 심부전 | Digoxin 사용의 명확한 이익의 근거가 없음 | STOPP |
| 지속적인 서맥(<60 bpm), 방실차단 또는 재발성 원인미상 실신의 기왕력이 있거나 심박수 저하약(베타차단제, Digoxin, Diltiazem, Verapamil) 사용 환자 | Acetylcholineesterase 저해제(Donepezil, Rivastigmine 등) 사용: 심전도 이상, 실신, 상해의 위험 증가 | STOPP |
Digoxin의 약물상호작용은 약물 유출 펌프인 장내 P-glycoprotein(P-gp)을 저해하거나 유도하는 약물에서 많이 발생한다. Quinidine과 Digoxin은 모두 P-gp의 기질이므로 병용 투여 시 Quinidine 이 Digoxin 수송의 강한 저해제로서 작용하여 Digoxin의 혈중농도가 2~3배 증가하므로 Digoxin 독성 발생의 위험성이 크게 증가한다. 반대로 Rifamfin(경구 600 mg/d)은 Digoxin과 병용투여 시 P-gp의 장벽 상피내 함량을 약 3.5배 증가시키는 유도작용을 나타내어 Digoxin의 효과를 현저하게 감소시킨다.
| Digoxin 적절성 평가 | 약물요법 최적화 계획 | 환자상담 |
|---|---|---|
| ▷ 약물 필요성 및 유효성 평가 · 적응증 확인 |
· 심부전이나 심방세동 등의 적응증 확인 · 사용목적 파악: 부적절이 의심되나 이상이 없는 경우 중단 권유는 곤란할 수 있음. 부작용 확인의 경우에는 약물투여 필요성을 평가해야 함. · 용량 적절성 평가: Digoxin 처방 환자에서는 용량 적절성을 평가해야 함. 합병증이 없는 노인에서는 1일 1/2정 초과 안됨. 신기능에 따른 용량조절 필요(감량: 격일 복용~1회/1주 복용). Digoxin의 용량은 혈중농도 모니터링을 통해서 결정하는 것이 권고됨. |
· 복용약의 인지 여부 확인 |
| ▷ 복약 순응도 평가 · 처방용량, 용법 준수 평가 · 복약 순응도 평가 |
· 실제 복용 용량 확인 · 일주일 중 잊지 않고 복용하는 일수 확인 |
· 매일 복용 여부 등 복용법 인지 여부 확인 |
| ▷ 안전성 평가 · 병용약물 평가 |
· Digoxin 혈중농도 상승(P-gp 억제 등으로): 마크로라이드계 항생제(Clarithromycin 등), Itraconazole, Amidarone, Quinidine, Cyclosporine, Verapamil, Quinidine 등 →
의사 인지하의 용량조절 여부 확인 · Digoxin 혈중 농도 저하(P-gp 유도): Rifampin · 서맥 부작용 증가: 베타차단제, Verapamil, Diltiazem, 치매치료제(Donepezil, Galantamine, Rivastigmine) → 맥박 확인 필요 · Digoxin 흡수저하: Cholestyramine → 복용시간 조절 |
· 감기, 폐렴, 요로감염, 무좀, 우울증 등으로 복용중인 병용약과의 상호작용 확인 |
| ▷ 위험상병 확인 · 만성 신장병 |
· 신기능 부전, 급성신부전 야기 약물(NSAID 등) | · 신기능 저하, 신장병, 갑상선 질환 유무 확인 |
| ▷ 부작용 확인 · 오심, 구토, 설사, 식욕부진 · 서맥, 빈맥, 불규칙 맥박, 시야흐림, 항색 시야 · 정신이상(혼동) · 심전도 변화 |
· 용량이 과하거나, 최근 약물병용으로 인한 약물상호작용으로 혈중농도의 상승 가능성, 급성 신부전의 가능성으로 인한 Digoxin 독성 가능성 평가 및 학인 · 맥박수 학인 · 정기적인 Digoxin 혈중농도 모니터링 여부 확인 · Digoxin 독성이 의심되면 응급실 방문 권유 |
· 맥박 수 확인 여부 · 부작용 증상을 질문하고 발생 여부 확인 |
- References
Disdier Moulder MPA, Hendricks AK, Ou NN. Towards appropriate polypharmacy in older cardiovascular patients: How many medications do I have to take? Clin Cardiol. 2020 Feb;43(2):137-144. doi: 10.1002/clc.23304. Epub 2019 Dec 11. PMID: 31825133; PMCID: PMC7021656.
Hanratty, C.G., McGlinchey, P., Johnston, G.D. et al. Differential Pharmacokinetics of Digoxin in Elderly Patients. Drugs & Aging 17, 353–362 (2000).
Martin F. Fromm, Richard B. Kim, C. Michael Stein, Grant R. Wilkinson and Dan M. Roden. Inhibition of P-Glycoprotein–Mediated Drug Transport. Circulation. 1999;99:552–557.
Greiner B, Eichelbaum M, Fritz P, Kreichgauer HP, von Richter O, Zundler J, Kroemer HK. The role of intestinal P-glycoprotein in the interaction of digoxin and rifampin. J Clin Invest. 1999 Jul;104(2):147-53. doi: 10.1172/JCI6663. Erratum in: J Clin Invest 2002 Aug;110(4):571. PMID: 10411543; PMCID: PMC408477.
대한약사회 사이버연수원 학술자료(2024년).
Copyright © MediGloPark's All Rights Reserved.
녹내장과 다제약물
 ▷ 고안압(elevated intraocular pressure, IOP) 치료 점안제에 포함되어 고안압증 또는 개방각 녹내장 등에 사용되는 Latanoprost는 prostaglandin F2α(PGF2α) 유사체로서
PGF2α의 에스테르 prodrug이다.
Latanoprost는 모 화합물보다 각막을 통해 더 잘 흡수되며 prostaglandin F2 α 수용체에 선택적으로 작용하여 방수 배출을 증가시켜 안압을 감소시킨다.
▷ 고안압(elevated intraocular pressure, IOP) 치료 점안제에 포함되어 고안압증 또는 개방각 녹내장 등에 사용되는 Latanoprost는 prostaglandin F2α(PGF2α) 유사체로서
PGF2α의 에스테르 prodrug이다.
Latanoprost는 모 화합물보다 각막을 통해 더 잘 흡수되며 prostaglandin F2 α 수용체에 선택적으로 작용하여 방수 배출을 증가시켜 안압을 감소시킨다. Latanoprost 활성형 약물의 방수내 최고 농도는 점적(15-30ng/ml)후 1-2시간으로 알려져 있다.
프로스타글란딘류는 녹내장 치료에서 IOP 저하효과, 1일1회 사용의 편리성 및 안전성 등이 우수하여 최우선적으로 사용하는 것이 일반적이다.
베타차단제인 Timolol은 점안제로 사용 시 안압저하효과로 개방각 녹내장 등에 사용되며, 전신적으로 투여하여 고혈압 치료 등에 쓰인다. 또한 국소적인 사용으로 유아기 피부 혈관종 축소 목적으로도 쓰인다.
Dorzolamide는 고안압 치료에 사용되는 국소적 Carbonic Anhydrase(CA) 저해제로서 섬모체 돌기(ciliary proces)에서 효소를 차단하여 눈의 이온 균형과 액압을 조절한다. 경구용 CA 저해제와는 다르게 Dorzolamide 점안제는 산-염기 또는 전해질 교란이나 전신적 부작용이 경미하다. 단일성분으로도 쓰이지만 Timolol과 함께 점안제로 제조되어 쓰이기도 한다.
Timolol과 같은 베타차단제는 점안 시 무색소 섬모체 상피(nonpigmented ciliary epithelium)와 혈관에 위치하는 베타-아드레날린 수용체에 작용하여 방수의 능동수송을 제한하는 기전으로 방수생성을 감소시킨다. 장기적 사용 시 방수의 분비는 40-50% 감소한다. 한편, 베타차단제 점안제를 급성편두통 치료에 사용하는 경우도 있으며 이는 점안제로 적용 시 비점막에서 전신적 흡수가 일어나 수분내에 치료혈청농도에 도달하기 때문이다.
| 분류 | IOP 저하 점안약물 | 비고 |
|---|---|---|
| PG analogs | Bimatoprost, Latanoprost, Travoprost, Tafuloprost | 효과: >Timolol, Dorzolamide, Brimonidine |
| beta-blockers(non-selective) | Timolol, Betaxolol, Levobunolol, Carteolol, Metipranolol | 방수생성 감소로 IOP 저하 |
| 선택적 alpha2-agonist | Brimonidine | 방수분비 감소 및 포도막공막 유출(uveoscleral outflow) 증가. α2 선택성이 크므로 안구 부작용 발현률이 낮음. |
| 국소적 CA 저해제 | Sulfonamides: Dorzolamide, Brinzolamide | 섬모체 돌기(ciliary process)에서 CA 차단으로 방수 형성 감소 |
Latanoprost 점안제를 6개월 이상 사용하는 경우 많은 환자에서 속눈썹 다모증(hypertrichosis)과 착색증가 현상이 나타날 수 있다. 또한 눈꺼풀의 착색이 나타나기도 한다. 1-2년 이상 사용하는 경우에는 홍체 착색이 나타날 수 있으며 사용을 중단하여도 변화가 없는 것으로 나타났다. 이러한 안구내외의 착색현상은 멜라닌생성(melanogenesis)이 증가한 결과이며 멜라닌세포의 증식에 의한 것은 아니다.
일부 국소적 녹내장 점안제 성분들은 전신적 부작용이나 약물-약물 상호작용을 나타낼 위험성이 있으므로 상황에 따른 세밀한 모니터링이 필요하다.
| 국소적 점안제 | 전신 투여 약물 | 약물-약물 상호작용 |
|---|---|---|
| topical beta-blocker | systemic beta-blocker | 저혈압 또는 서맥의 위험성 증가 |
| topical beta-blocker | systemic ACE inhibitor | 저혈압 위험성 증가 |
| topical beta-blocker | systemic CCB | 부정맥 위험성 증가 |
| topical beta-blocker | systemic CCB(Diltiazem, Verapamil), Cadiac Glycoside(Digoxin) | 서맥의 위험성 증가 |
| topical beta-blocker | 항당뇨약 | 저혈당 증상을 가릴 위험성 |
| topical beta-blocker | adrenergic agonists(예: Albuterol) | 천식환자에서 기관지확장을 경쟁적으로 억제 |
| PGs | Atorvastatin, Simvastatin, Fluvastatin | 이상지질혈증 환자: 혈액검사에서 간 이상에 대해 위양성(false positive)을 나타낼 수 있음. |
| alpha-2 adrenergic agonist(Brimonidine) | beta-blockers, 항고혈압약, 강심배당체 | 저혈압 또는 서맥 위험 |
| 국소적 CA 저해제 | 신질환자: 금기(신배설) |
- References
Alm A. Latanoprost in the treatment of glaucoma. Clin Ophthalmol. 2014 Sep 26;8:1967-85. doi: 10.2147/OPTH.S59162. PMID: 25328381; PMCID: PMC4196887.
Negri L, Ferreras A, Iester M. Timolol 0.1% in Glaucomatous Patients: Efficacy, Tolerance, and Quality of Life. J Ophthalmol. 2019 May 2;2019:4146124. doi: 10.1155/2019/4146124. PMID: 31191995; PMCID: PMC6525866.
Apătăchioae I, Chiseliţă D. Agoniştii alfa 2 adrenergici în tratamentul glaucomului [Alpha-2 adrenergic agonists in the treatment of glaucoma]. Oftalmologia. 1999;47(2):35-40. Romanian. PMID: 10641099.
Schlote, T. Nebenwirkungen und Risikoprofil bei Anwendung von Latanoprost 0,005% (Xalatan®). Ophthalmologe 99, 724–729 (2002). https://doi.org/10.1007/s00347-002-0613-1.
Balfour, J.A., Wilde, M.I. Dorzolamide. Drugs & Aging 10, 384–403 (1997). https://doi.org/10.2165/00002512-199710050-00006
Ann M. Hoscheit. Interactions with Glaucoma Meds. Review of Optometry. Vol. No: 140:07Issue: 7/15/03. https://www.reviewofoptometry.com/article/interactions-with-glaucoma-meds.
Migliazzo CV, Hagan JC 3rd. Beta blocker eye drops for treatment of acute migraine. Mo Med. 2014 Jul-Aug;111(4):283-8. PMID: 25211851; PMCID: PMC6179466.
Copyright © MediGloPark's All Rights Reserved.
고혈압과 다제약물
 ▷
고혈압약제 3종 이상을 복용중인 환자에서는 다제약물의 위험성에 더 주의하여야 한다. 가장 일반적인 고혈압 약제는 이뇨제, 베타차단제(BB), ACE 억제제,
칼슘채널차단제(CCB), 안지오텐신 수용체 차단제(ARB) 등이다.
▷
고혈압약제 3종 이상을 복용중인 환자에서는 다제약물의 위험성에 더 주의하여야 한다. 가장 일반적인 고혈압 약제는 이뇨제, 베타차단제(BB), ACE 억제제,
칼슘채널차단제(CCB), 안지오텐신 수용체 차단제(ARB) 등이다.알파차단제인 Doxazosin과 Terazosin은 노인에서 기립성 저혈압의 위험이 있고 대체약이 있으므로 고혈압약제로 투여하는 것을 삼가해야 한다. 전립선 비대증 치료제로 사용 시는 부적절 약물로 평가되지 않기도 하지만(Beers Criteria), 국내에서는 질병에 상관 없이 전체 노인 부적절 약물로 지정되어 있다. 전립선 비대증에는 Tamsulosin, Alfuzosin등이 대체약으로 권고된다.
Doxazosin은 CYP3A4의 기질이므로 강한 CYP3 저해제는 doxazosin 노출을 증가시킬 수 있다. Doxazosin을 강한 CYP3 저해제와 동시에 사용할 때에는 혈압과 저혈압 증상을 모니터링하여야 한다.
Phosphodiesterase-5(PDE-5) 저해제와 Doxazosin을 병용하는 경우 상가적 혈압저하 효과가 나타나므로 혈압과 저혈압 증상을 모니터링하여야 한다.
| 고혈압 약제 | 특징 |
|---|---|
| Thiazide계 이뇨제: Chlorthalidone, Hydrochlorothiazide, Indapamide | 저칼륨혈증, 저나트륨혈증, 고칼슘혈증 또는 통풍의 기왕력 환자에서 악화 위험성을 증가 |
| 루프계 이뇨제: Bumetanide, Ethacrynic acid, Furosemide, Torsemide | 요실금이 동반된 환자에서 요실금 악화 위험성 증가: 투약 필요성 평가 필요 |
| sulfonamide계 이뇨제: Xipamide | |
| ACE 저해제: Alacepril, Benazepril, Captopril, Enalapril, Fosinopril, Imidapril, LIsinopril, Moexipril , Perindopril, Quinapril, Ramipril, Trandolapril | 고칼륨혈증 주의 |
| Angitensin II 수용체 길항제(ARB): Candesartan, Eprosartan, Fimasartan, Irbesartan, Olmesartan, Telmisartan, Valsartan | 고칼륨혈증 주의 |
| 칼슘채널 차단제(심장 선택성 CCB): Diltiazem, Verapamil | ▷ 심박수 저하로 심부전 환자에서 부적절 ▷ 베타차단제와 병용 시 상가적 심박수 저하로 방실블록의 위험성 증가 |
| 칼슘채널 차단제(혈관 선택성 CCB)(-dipine): Amlodipine, Benidipine, Cilnidipine, Felodipine, Isradipine, Lercanidipine, Nicardipine, Nifedipine, Nisoldipine | Nifedipine IR, 5mg, 10mg캡슐: 저혈압 위험(급격한 혈압저하) 및 심근경색 악화 위험으로 노인주의 권고 |
| 베타 차단제: Atenolol, S-atenolol, Betaxolol, Bisoprolol, Bevantolol, Carvedilol, Celiprolol, Metoprolol, Nebivolol, Propranolol | 서맥(심박수<50), 2도 방실블록 또는 완전방실블록이 있는 환자에서 완전방실블록 또는 심정지의 위험성 증가 |
| peripheral alpha-1 blockers: Doxazosin, Terazosin | 노인에서 부적절 고혈압 약제(기립성 저혈압) |
| 혈관 확장제: Minoxidil, Hydralazine, Cardralazine |
칼륨 저류 약제(ACEI, ARB, Amiloride, Triamterene)와 알도스테론 길항제(예, Spironolactone)를 병용하는 것은 고칼륨혈증의 위험성을 증가시키므로 최소한 6개월 간격으로 혈청 칼륨 농도를 정기적으로 확인하여야 한다.
ACE가 억제되면 알도스테론 분비가 감소하여 혈청 칼륨 농도가 상승하는데 칼륨보존성 이뇨제의 작용으로 상가적 고칼륨혈증이 발생할 수 있다. 이러한 상호작용은 정상적인 신기능을 유지하는 환자에서는 경미하지만, 신부전, 당뇨, 고령, 심각한 심부전과 같은 위험인자가 있는 경우에는 치명적일 수 있다. ACEI, ARB는 고혈압 조절 등으로 신장 보호 작용이 있고 CKD 진행을 지연(Stage 1~3 CKD)하지만, 3기 이상(stage 4~5)의 만성신부전 환자에서는 고칼륨혈증의 위험성이 더욱 증가하므로 ACEI, ARB 사용 시 정기적으로 혈청 칼륨 농도와 신기능을 검사하여야 하며 고칼륨혈증이 발생하면 사용중단을 고려하여야 한다. 고칼륨혈증의 증상은 무력감, 노곤함, 정신착란, 수족마비, 불규칙한 심박동 등이다.
65세 이상의 노인에서 혈압상승을 야기하는 여러 약제 및 요인들이 있다. NSAID와 같은 약물 이외에 흡연, 커피, 음주 등도 혈압을 상승시키는 원인이 된다. 커피(카페인)는 일시적인 혈압상승을 일으키는 것으로 알려져 있는데 노인 고혈압 환자에서는 주의가 필요하다.
| 질병, 증후 | 부적절 약물 또는 START |
|---|---|
| 심부전 | Diltiazem, Verapamil: EF저하(HFrEF) 환자에서 금기 |
| 실신 | 비선택성 알파차단제:
Doxazosin, Terazosin → 기립성 저혈압으로 인한 실신 위험 |
| 여성 요실금 | 알파차단제:
Doxazosin, Terazosin → (스트레스성)요실금 악화 |
| 지속적 서맥(<60bpm), 방실차단 또는 재발성 원인미상 실신의 기왕력이 있거나 심박수 저하약(베타차단제, Digoxin, Diltiazem, Verapamil) 사용 환자 | acetylcholine esterase 저해제:
Donepezil, Rivastigmine 등 → 콜린성 약물의 서맥과 상가적 서맥 위험성 증가 |
| 치료가 필요한 천식 기왕력 환자 | 비선택적 베타차단제: 천식악화 위험성 증가 | 지속성 기립성 저혈압(반복적 수축기 혈압이 20mmHg 이상 감소)환자 | 혈관확장제:
알파차단제, CCB, Nitrate, ACEI, ARB → 실신, 낙상위험 증가 |
| 나트륨혈증 | 이뇨제(특히 thiazide계): 최근 저나트륨혈증, SIADH(Syndrome of inappropriate antidiuretic hormone ADH release)의 기왕력 확인, 혈청 나트륨 농도 모니터링 |
| 빈번한 저혈당 에피소드가 있는 당뇨 | 베타차단제: 저혈당 증상을 가릴 수 있음(증상 억제) |
| 지속적으로 SBP>160mmHg 그리고/또는 DBP>90mmHg | → 항고혈압제 사용을 해야함(START) |
| 당뇨병환자이면서 SBP>140mmHg 그리고/또는 DBP>90mmHg | → 항고혈압제 사용을 해야함(START) |
| 심부전 그리고/또는 명확한 관상동맥질환 환자 | → ACE 억제제 또는 ARB 사용(START) |
| 허혈성 심질환 환자 | → 베타차단제 사용(START) |
| 안정형 심부전 환자 | → 적절한 특정 베타차단제(: Bisoprolol, Nebivolol, Metoprolol, Carvedilol) 사용(START) |
비선택적 베타차단제(Propanolol, Carbedilol, Nadolol, Pindolol, Labetalol, Penbutolol, Sotalol, Timolol) 사용 시 약물에 따라 차이가 있지만 대체로 천식이나 COPD 환자에서 질병악화의 위험성이 증가하므로 주의하여야 한다. 한편, 선택적 베타차단제로는 Metoprolol, Atenolol, Acebutolol, Betaxolol, Esmolol , Bisoprolol 그리고 Nebivolol 등이 있으며 Metoprolol 등 일부 선택적 베타차단제도 천식발작 발현 위험성 증가와 관계가 있는 것으로 보고된 연구도 있으므로 주의가 필요하다.
| 약물 - 약물 | 상호작용 |
|---|---|
| RAS 억제제(ACEI, ARB) 또는 포타슘 저류 이뇨제 ⇆ 다른 RAS 억제제 | 고칼륨혈증 위험: 만성 신장병 3기 이상의 환자에서 일상적인 병용은 부적절함 |
| 알파1 차단제 ⇆ Loop 이뇨제 | 노인여성에서 요실금 위험성 증가 |
| (SBP<90mmHg 등의 저혈압을 나타내는 중증 심부전 또는 협심증 치료 환자에서)Nitrate ⇆ PDE5-억제제(예: Sildenafil, Tadalafil, Vardenafil) | 심허탈의 위험 증가: STOPP |
고혈압 환자에서 가장 일반적인 동반질병은 이상지질혈증, 만성심부전, 제2형당뇨병, 비만, 관상동맥성 심장질환, 만성신부전 등이며 동반질병(comorbidity)에 따른 약물들이 추가되는 경우 다제 약물의 위험성에 특히 주의하여야 한다. 고혈압 환자의 동반질병으로 인한 약물들은 주로 스타틴류, 항혈소판제, PPI, 항응고제, 경구 항당뇨약, 협심증약, 인슐린 주사 등이 일반적이며 이외에 항생제, NSAID, 감기약, 비타민, 미네랄, 건강기능식품 등 다양한 제제들이 사용될 수 있으므로 이에 대한 평가가 세밀하게 이루어져야 한다.
| 고혈압 약제 적절성 평가 | 약물요법 최적화 계획 | 환자상담 |
|---|---|---|
| ▷ 약물 필요성 및 유효성 평가 · 적응증 확인 · 효과 평가 |
· 복용이유, 적응증 확인을 통해서 필요한 경우 반드시 복용해야 함을 설명(복약순응도 향상) · 고혈압 이외의 목적도 같이 고려, 설명 · 노인의 혈압조절 기준은 통상 140/90mmHg · 노인 쇠약 상태의 환자에서는 적극적인 혈압저하의 유불리를 평가 · 최근 혈압 측정치 기록 여부 확인 |
· 복용중인 혈압약의 인지 여부 확인 · 다른 질환으로 복용중인 약이 있는지 확인 |
| ▷ 복약순응도 평가 · 처방 용량, 용법 준수 평가 · 복약순응도 평가 |
· 3종 이상의 고혈압 약제 복용 후에도 조절이 안되면 저항성 고혈압(심장질환, 신장질환의 위험성 증가), 복약 순응도를 우선 평가해야 함. · 염분 섭취 등 식이습관에 대한 순응도 평가 |
· 매일 복용 여부 및 복약 실수 여부를 확인 · 혈압 및 맥박의 측정, 기록, 의사에게 측정기록 제출 여부 확인 |
| ▷ 병용약물 평가 · 혈압조절에 부정적 영향을 미치는 약물 · 전립선 치료 목적의 알파차단제 · 칼륨보충제, 칼륨저류 이뇨제 · 심혈관계 약제 총체적 평가 |
· 지속적인 NSAID나 비충혈제거제(예: Pseudoephedrine, Phenylephrine) 사용 시 혈압조절 방해 가능성을 주의 · 타 약제 복용으로 인한 기립성저혈압의 발생, 심박수(서맥)에 미치는 영향 등을 평가 · 전립선 비대증 치료 목적의 (selecticve 또는 non-selective)알파차단제 사용으로 인한 저혈압과 실신에 대한 주의 |
· 관절염이나 두통으로 인한 진통제, 감기약, 전립선비대증 치료제 등 다른 약물 복용 여부 확인 |
| ▷ 위험상병 확인 · 실신 기왕력, 심부전 · 만성 신장병, 전해질 이상 · 통풍, 요실금 |
· 통풍환자의 thiazide계 이뇨제 사용→약물전환에 대한 권고 가능 · 요실금 환자의 이뇨제(특히 루프 이뇨제)→요실금이 조절되지 않을 경우 의사와 상의하도록 권고 · 기타 상병→의사 인지 여부 확인 |
· 심장질환이나 신장질환 동반 여부 확인 · 저나트륨혈증, 고나트륨혈증 인지 여부 확인 |
| ▷ 부작용 학인 · 기립성 저혈압 · 두통(CCB, 혈관확장) · 발목부종(CCB) · 마른기침(ACE) · 탈수, 체중감소, 무기력(이뇨제) · 피로감, 성기능 장애, 악몽(BB) |
· 환자의 무기력, 어지러움, 기립성 저혈압 평가가 필요하며, 이들을 혈압, 맥박 등 객관적 수치와 연결하여 약물치료의 적절성을 평가 · 기립성 저혈압의 경우 서서히 일어나는 것을 권고 · 약물-약물, 약물-질병 상호작용으로 인한 전해질 이상(저나트륨혈증, 고칼륨혈증)의 위험성이 높은 환자→주기적인 모니터링 여부 확인 |
· 기립성 저혈압 증상 발현 여부 확인 · 요실금 확인 · 정기적인 혈액검사 여부 확인 · 신기능 및 혈액검사 수치의 이상 유무와 인지 여부 |
- References
The 2023 American Geriatrics Society Beers Criteria® Update Expert Panel: American Geriatrics Society 2023 updated AGS Beers Criteria® for potentially inappropriate medication use in older adults. J Am Geriatr Soc. 2023;1–30.
Mukoyama, M., Kuwabara, T. Role of renin-angiotensin system blockade in advanced CKD: to use or not to use?. Hypertens Res 45, 1072–1075 (2022). https://doi.org/10.1038/s41440-022-00902-7.
O’Mahony, D., Cherubini, A., Guiteras, A.R. et al. STOPP/START criteria for potentially inappropriate prescribing in older people: version 3. Eur Geriatr Med 14, 625–632 (2023). https://doi.org/10.1007/s41999-023-00777-y.
Charlene Bredy, Margherita Ministeri, Alexander Kempny, Rafael Alonso-Gonzalez, Lorna Swan, Anselm Uebing, Gerhard-Paul Diller, Michael A Gatzoulis, Konstantinos Dimopoulos, New York Heart Association (NYHA) classification in adults with congenital heart disease: relation to objective measures of exercise and outcome, European Heart Journal - Quality of Care and Clinical Outcomes, Volume 4, Issue 1, January 2018, Pages 51–58, https://doi.org/10.1093/ehjqcco/qcx031.
Huang KY, Tseng PT, Wu YC, Tu YK, Stubbs B, Su KP, Matsuoka YJ, Hsu CW, Lin CH, Chen YW, Lin PY. Do beta-adrenergic blocking agents increase asthma exacerbation? A network meta-analysis of randomized controlled trials. Sci Rep. 2021 Jan 11;11(1):452. doi: 10.1038/s41598-020-79837-3. PMID: 33432057; PMCID: PMC7801657.
Diaconu CC, Cozma MA, Dobrică EC, Gheorghe G, Jichitu A, Ionescu VA, Nicolae AC, Drăgoi CM, Găman MA. Polypharmacy in the Management of Arterial Hypertension-Friend or Foe? Medicina (Kaunas). 2021 Nov 23;57(12):1288. doi: 10.3390/medicina57121288. PMID: 34946233; PMCID: PMC8705955.
MOMONIAT AND COLLEAGUES. ACE inhibitors and ARBs: Managing potassium and renal function. CLEVELAND CLINIC JOURNAL OF MEDICINE VOLUME 86 • NUMBER 9 SEPTEMBER 2019.
대한약사회 사이버연수원 학술자료(2024년).
Copyright © MediGloPark's All Rights Reserved.
항혈전제(Antithrombotic agents)
 ▷ 항혈전제는 응고인자의 합성 감소 또는 응고과정 저해 작용을 하는 항응고제(Anticoagulants), 혈소판 기능 억제작용을 하는 항혈소판제(Antiplatelet agents),
형성된 혈전의 용해를 촉진하는 혈전 용해제(thrombolytic agents, thrombolytics) 등 3종으로 대별된다.
▷ 항혈전제는 응고인자의 합성 감소 또는 응고과정 저해 작용을 하는 항응고제(Anticoagulants), 혈소판 기능 억제작용을 하는 항혈소판제(Antiplatelet agents),
형성된 혈전의 용해를 촉진하는 혈전 용해제(thrombolytic agents, thrombolytics) 등 3종으로 대별된다.항응고제는 동맥혈전증(Arterial Thrombosis) 치료 활성도 있지만 주로 정맥 혈전증(venous thrombosis), 특히 심부정맥혈전증(deep venous thrombosis)의 예방 및 치료에 널리 사용되며, 항혈소판제는 혈소판이 많은 동맥 혈전증의 예방 및 치료에 효과가 있다. 혈전 용해제는 주로 조직 플라스미노겐 활성화제(tissue plasminogen activators, tPA) 등이 포함되며 동맥 또는 정맥 혈전증 또는 색전(emboli) 발생 후 즉시 또는 가급적 빨리 정맥투여된다.
그외 항혈전제로는 Defibrotide와 Anagrelide가 있다.
| Classes | Antithrombotic agents |
|---|---|
| Anticoagulants |
▷ Indirect Thrombin Inhibitors(Low Molecular Weight Heparins, LMWH): Dalteparin(1994년), Endoxaparin(1993년), Tinzaparin(2000년) ▷ Direct Thrombin Inhibitors: Dabigatran(2010년), Desirubin(2003년) ▷ Factor Xa inhibitors: Fondaparinux(2001년), Rivaroxaban(2011년), Apixaban(2012년), Edoxaban(2015년) ▷ Vitamin K antagonist: Warfarin(1967년) |
| Antiplatelet agents | ▷ (Irreversible) Inhibitors of COX-1: Aspirin, other NSAIDs ▷ Phosphodiesterase Inhibitors(or Adenosine uptake blockers): Cilostazole, Dipyridamole(1961년) ▷ P2Y12 inhibitors: Ticlopidine(1991년), Clopidogrel(1997년), Prasugrel(2009년), Ticagrelor(2011년), Cangrelor(2015년) ▷ PAR-1 antagonist: Vorapaxar(2014년) ▷ GP IIb/IIIa receptor inhibitors: Abciximab(1994년), Eptifibatide(1998년), Tirofiban ▷ selective 5-HT receptor subtype 2A antagonist: Sarfogrelate |
| Thrombolytics | ▷ tPA: Alteplase, Reteplase, Tenecteplase ▷ Anistreplase, Streptokinase, Urokinase |
| Other antithrombotic agents | Defibrotide, Anagrelide |
Aspirin(Acetylsalicylic acid)은 혈소판 Cyclooxygenase(COX)의 기능적으로 중요한 아미노산인 serine529 아세틸화 작용으로 혈소판의 기능을 억제한다. Aspirin의 이러한 작용에 의해 COX 효소의 촉매 자리인 tyrosine385 위치에 COX의 기질인 arachidonic acid 접근이 저해되어 혈소판 의존적 thromboxane 형성이 비가역적으로 저해된다. Aspirin은 COX-2(inducible: cytokines, 염증성 자극, 일부 성장 인자 등에 의해 발현))보다 COX-1(constitutive)에 대략 150~200배 더 강력한 억제작용이 있는데, 이에 따라 항혈전(COX-1)약제와 항염(COX-2)약제로서 사용되는 Aspirin의 투여 요구량이 다르다.
Dipyridamol은 adenosine 재흡수 억제 또는 phosphodiesterase(: cAMP 대사에 관여)를 저해하여 혈소판의 cAMP 수준을 증가시켜 혈소판 응집 억제작용을 나타낸다.
티에노피리딘(thienopyridines) 계열인 Ticlopidine, Clopidogrel, Prasugrel 등은 혈소판의 주된 ADP 수용체(Purinergic receptor, P2Y12)를 저해하여 이들의 활성과 응집작용을 차단한다.
Ticagrelor는 thienopyridines 계열이 아니지만 thienopyridines와 유사한 작용을 갖는 혈소판 응고 저해제이다.
Vorapaxar는 혈소판의 PAR-1(protease-activated receptor 1) 억제제로서 혈소판 응집 저해작용을 하며 고위험 환자군에서 죽상동맥경화(atherosclerotic) 이벤트 위험성 감소 목적으로 주로 사용된다.
glycoprotein IIb/IIIa (GP IIb/IIIa) receptor 억제제는 fibrinogen과 vWF(von Willebrand factor)의 작용을 이들 혈소판의 원형질막(plasma membrane) GP IIb/IIIa 수용체에서 차단하여 fibrinogen의 결합을 저해하는 기전으로 혈소판 응집 예방에 즉각적인 효과를 나타낸다. 이러한 약제들은 정맥투여하여 급성 관상동맥질환과 경피적 관상동맥 중재술(percutaneous coronary artery intervention, PCI)에서 즉각적인 혈소판 저해효과를 얻기 위해 사용한다.
Sarfogrelate는 선택적 혈소판 및 혈관 평활근 세포(vascular smooth muscle cells, VSMCs) 5-HT(hydroxytryptamine, serotonin) 수용체 subtype 2A 길항제로서 5-HT 수용체 차단에 의한 혈소판 응집 억제 작용과 VSMCs 증식 억제작용이 있어 만성동맥폐색증 환자에서 허혈증상 치료 시 말초순환 개선을 위해 사용하며 허혈성 심질환 또는 말초혈관질환 치료에도 효과가 있는 것으로 알려져 있다.
Defibrotide는 돼지 장점막 유래 단사 PDRNs(single stranded polydeoxyribonucleotides)의 혼합복합체로서 항혈전 및 피브린용해촉진(profibrinolytic) 활성을 나타내며 성인 및 소아의 간정맥폐쇄질환(hepatic veno-occlusive disease, HVOD) 등에 쓰인다.
Anagrelide는 혈소판 생성을 저해하여 혈소판 수를 감소시켜 항혈소판 작용을 나타내므로 본태성 혈소판증가증(essential thrombocytosis)과 동맥 또는 정맥 혈전증 위험성 증가와 관련된 고혈소판증을 일으키는 기타의 원인 치료에 사용된다.
한편, 죽상혈전증(粥狀血栓症, atherothrombosis)에서 문제가 되는 혈소판 응집을 억제하는 항혈소판 치료는 급성관상동맥증후군(acute coronary syndrome)과 경피적 관상동맥 중재술(percutaneous coronary intervention, PCI)에서 매우 중요하다.
이중항혈소판요법(Dual Antiplatelet Therapy, DAPT)은 통상 아스피린과 P2Y12 억제제를 동시에 투여하며 환자에 따라 출혈과 혈전증의 위험성을 고려하여 6개월 또는 12개월까지 시행하는 것이 일반적이다. 한편, 더 많은 연구가 진행되어야 함을 전제로 약물용출성 스텐트의 경우에는 3개월 DAPT후 P2Y12 억제제 단일요법이 12개월 DAPT보다 나쁘지 않은 것으로 보고되었다.
| 구분(thienopyridines or non-thienopyridines) | P2Y12 수용체 억제제 | 비고 |
|---|---|---|
| 1세대 | Ticlopidine | 부작용(neutropenia, anemia, GI distress, thrombotic thrombocytopenic purpura)으로 사용이 제한됨. |
| 2세대 | Clopidogrel | ticlopidine을 대체함. 임상 자료가 많음. |
| 3세대 | Prasugrel | adenosine diphosphate P2Y12 수용체를 비가역적으로 차단하여 혈소판 응집을 억제함. |
| 4세대 | Ticagrelor, Cangrelor, Enilogrel | non-thienopyridines: Ticagrelor, Cangrelor |
clopidogrel은 CYP3A4 효소에 의해 대사되어 활성을 나타내는 prodrug이므로 CYP3A4에 의해 대사되는 일부 PPI(ptoton pump inhibitor), 스타틴류, 항진균제 등과 동시에 투여 시 항혈소판 효과가 감소할 수 있다.
반대로 CYP3A4 활성을 유도하는 제제는 clopidogrel의 반응성을 증가시킬 수 있으므로 주의가 필요하다.
한편, Ticagrelor는 케토코나졸, 클래리스로마이신 등과 같은 강한 CYP3A4 억제제와 병용 투여시 Ticagrelor의 대사가 저해되어 부작용이 증가할 수 있다.
와파린(warfarin)은 체내 비타민 K 활성화 필수 효소인 vitamin K epoxide reductase complex 1 (VKORC1)을 경쟁적으로 저해하여 작용을 나타낸다. VKORC1에 대한 이러한 경쟁적 저해는 비타민 K의 고갈을 초래하여 활성 응고 인자들의 합성 감소를 유도한다. 응고인자 II, VII, IX, 그리고 X, 뿐만아니라 응고 조절 인자인 protein C와 protein S의 간 합성에 비타민 K가 필수적으로 필요하다. 즉, 비타민 K는 이러한 비타민 K 의존성 응고인자들의 합성에 필수적인 보조인자이다.
와파린은 R과 S 이성질체로 구성된 라세미 혼합물(racemic mixture)이며, S 이성질체가 R 이성질체보다 3~5배 더 강력하다.
| 구분 | warfarin 특징 및 주의사항 |
|---|---|
| 작용기전 | VKORC1 억제 |
| 흡수 | 신속, 거의 대부분 흡수됨 |
| 반감기 | 36~42시간 |
| 최고 효과 발현 | · 응고인자의 반감기 고려 시 5~7일 · 작용개시: 24~72시간이지만 환자의 INR(International Normalized Ratio)은 치료 시작 후 36~72시간 이내에 증가 |
| 작용 지속 시간 | 2~5일 |
| 용량 | 환자간 및 환자내 적정용량의 차이가 크며, 정기적인 혈액응고검사(prothrombin time, INR) 결과에 따라서 용량조절(total weekly dose 기준) |
| 투여시간 | 1일 1회 오후 또는 저녁 투여 권고(환자의 개별적 최신 lab value에 근거한 용량 설정 용이). 최신 용량 인지가 중요함. |
| 최고혈중농도 | 대략 4시간 |
| 주의사항 | · 약물-약물, 약물-질병 상호작용 주의 · Vitamin K 함유음식, 식이 주의 · 개체간, 개체내 용량차이 주의: PT(INR) 정기적 모니터링 필요 |
| 주 적응증 | · Deep Vein Thrombosis(DVT) 예방및 치료 · Pulmonary Embolism(PE) · Prosthetic Cardiac Valve Replacement · Atrial fibrillation · Stroke, cardioembolic origin |
| 간 대사 | · primarily CYP2C9 → CYP2C9 효소의 유전적 다양성은 각 개인의 와파린 대사에 영향을 줌. · minor: CYP2C8, 2C18, 2C19, 1A2, 3A4 |
| 배설 반감기 | 20~60시간(평균 40시간): 개인차가 심함 |
| 배설 | 주로 신사구체 여과 배설(6-, 7-, 8-, 10-hydroxywarfarin 등): 소변배설 92% |
| 식품 | · 비타민 K 고함유 식품(: 시금치, 부추, 근대, 무청, 냉이, 쑥, 비름, 갓김치, 케일, 녹차 등.
조금 높은 식품: 양상추, 상추, 양배추, 배추, 미나리, 브로콜리, 미역, 김, 다시마 등)에 의한 와파린 효과 감소: 적정량을 일관되게 섭취 · 크랜베리 주스 제한: CYP2C9 저해로 출혈 위험성 증가(INR 상승) · 자몽주스 제한: CYP1A2 및 CYP3A4 저해로 출혈 위험성 증가(INR 상승) |
와파린의 심각한 부작용인 현저한 대량출혈, 즉 두개내 출혈(intracranial hemorrhage), GI 출혈, 토혈(hematomesis), 안구내 출혈, 혈관절증(hemarthrosis) 등 뿐만 아니라 일반적인 부작용인 쉬운 출혈 경향과 멍 발생에 대한 충분한 교육이 환자에게 필요하다. 그외 구역, 구토, 복통, 팽만감, 고창, 미각변화, purple toe syndrome(보통 치료 개시 3~8주 후), 피부괴사(와파린 치료 후 획득성 protein C 결핍에 기인) 등의 부작용도 나타날 수 있다. 저항성칼슘형성(calciphylaxis = calcific uremic arteriolopathy)도 드물지만 나타날 수 있다. 특히 노인은 출혈 합병증의 위험성이 크므로 세심한 모니터링이 필요하며 더욱 보수적인 용량요법(dosage regimen)이 요구된다.
와파린 사용 시 병용할 수 있는 약과 주의하여야 할 약이 있다
| 구분 | 병용 가능한 약 | 주의가 필요한 약 |
|---|---|---|
| 해열, 소염진통제 | 아세트아미노펜(타이레놀: 하루 3정 이하) 이부프로펜(부루펜): 최소 단기간 나프록센: 최소 단기간 |
아스피린, 피록시캄, 록소닌, 쎄레브렉스, 폰탈, 모니플루메이트, 탈리플루메이트 |
| 파스 및 연고 | 케토프로펜 파스(케토톱, 케펜텍) | 메틸살리실레이트 포함 연고 및 파스 |
| 코감기 | 액티피드 | 거담제 | 암브록솔(뮤코펙트), 리나치올, 엘도스테인(엘도스) |
| 진해제 | 덱스트로메토르판, 지미코프, 코푸시럽 | 옥소라민(페브론) |
| 항균제 | 아목시실린, 설타미실린(유나신), 오구멘틴, 록시스로마이신(루리드), 세파계 항생제 | 클래리스로마이신, 메트로니다졸, 설파메톡사졸(박트림), 시프로플록사신, 스포라녹스 또는 플루코나졸 등의 항진균제 |
| 위장관계약 | 파모티딘(가스터), 니자티딘, 제산제(뉴란타, 아루사루민, 포스겔, 알마겔: 와파린과 2시간 차이를 두고 복용) | 시메티딘(타가메트), 오메프라졸, 레보프라잔 |
| 소화제 및 기타 위장약 | 소화제(베아제, 훼스탈, 파자임 등), 모사프라이드, 모티리움, 엑소롱, 효모균제제, 무타실, 아락실, 마그밀 | |
| 항히스타민제 | 페니라민, 유시락스, 지르텍, 알레그라 등 | 생약, 한약, 건강보조식품 |
와파린의 효과를 증가시키거나 저하시키는 식품, 보조식품, 한약재 등을 주의하여야 한다.
| 와파린 효과 증가(INR 상승) | 와파린 효과 감소(INR 저하) |
|---|---|
| 크랜베리 주스(Cranberry juice), 자몽 주스(Grapefruit juice), 단삼, 당귀, 호로파(Boldo-fenugreek), 구기자, 악마의 발톱(Devil's claw), Curbicin, 글루코사민, 콘드로이친, Fish oil, 마늘, 생강, 은행잎, 멜라토닌, 파파야 추출물, 망고 등 | St. John's wort, 녹차, 코엔자임 Q10, 비타민 K 함유 종합비타민, 낫또(비타민 K 함유), 두유, 아보카도(다량), 비타민 K 다량 함유 식품, 인삼 |
항응고제 중 NOAC(New or Novel Oral Anticoagulants)은 Thrombin(Factor II) 또는 Factor Xa를 저해하여 작용을 나타내며 많은 적응증에서 와파린을 대체하고 있다.
| NOAC | 기전 |
|---|---|
| Dabigatran | Thrombin(Factor II) 저해 |
| Rivaroxaban, Apixaban, Edoxaban, Betrixaban, Darexaban(YM150) | Factor Xa 저해 |
항응고제에 대한 Beers, STOPP(Screening Tool of Older Persons' Prescriptions)/START(Screening Tool to Alert to Right Treatment) criteria의 노인주의 권고사항은 다음과 같다.
| 항응고제 사용 시 노인주의 사항 | 권고 |
|---|---|
| 출혈의 위험이 유의하게 높은 상태, 즉 조절되지 않는 중증 고혈압, 출혈 체질, 최근 경미하지 않은 자발출혈환자에서 aspirin, clopidogrel, dipyridamole, warfarin, NOAC의 사용 | STOPP |
| 만성 심방세동 환자에서 warfarin 또는 NOAC과 aspirin의 병용(aspirin의 추가적 이익 없음) | STOPP |
| 안정형 협심증, 뇌혈관 질환 또는 말초혈관질환에서 항혈소판제와 warfarin 또는 NOAC의 병용(이중요법으로 추가되는 이익 없음) | STOPP |
| 지속되는 유발 원인 없이 첫번째 발생한 폐색전증에서 12개월을 초과하여 warfarin 또는 NOAC의 사용 | STOPP |
| 만성 심방세동이 있는 환자에서 warfarin 또는 NOAC 사용 | START |
Beers, STOPP/START criteria에서 NOAC 사용 시 신기능과 관련하여 GFR <30mL/min 미만 환자에서 Dabigatran 사용 또는 GFR < 15mL/min 미만 환자에서 factor Xa inhibitors(Rivaroxaban, Apixaban 등) 사용에 주의를 권고 하고 있다.
| NOAC | 주의사항 |
|---|---|
| Dabigatran | · 75세 이상, Clcr < 30mL/min: 75세 이상 노인에서 위장관 출혈 증가, Clcr < 30mL/min에서의 유효성, 안전성 자료 없음 |
| ... | ... |
NOAC의 적응증 및 용량은 다음과 같다.
| NOACs | 적응증 및 용량 |
|---|---|
| Rivaroxaban(자렐토 2.5mg, 10mg, 15mg, 20mg) | · 심방세동: 20mg OD. Clcr 15~50mL/min의 경우는 15mg OD · 심방세동 + 스텐트: 10mg OD + P2Y12 억제제 · 심부정맥혈전증 + 폐색전증 치료와 재발 위험 감소: 처음 3주간 15mg BID, 이후 20mg OD(CrCl < 30ml/min의 경우는 권장하지 않음) · 주요 정형외과 수술 후 정맥 혈전 색전증 예방: 10mg OD · 심근경색: 2.5mg BID + Aspirin, Clopidogrel · CrCl 15~30mL/min: 주의 필요 |
| Apixaban(엘리퀴스 2.5mg, 5mg) | · 정맥혈전색전증의 예방, 재발 예방: 2.5mg BID · 심방세동: 5mg BID(80세 이상, 60kg이하 또는 Scr > 1.5: 2.5mg BID). CrCl 15~30mL: 2.5mg BID · 정맥혈전색전증의 치료: 7일간 10mg BID 이후 5mg BID · CrCl < 15mL/min 환자에서는 권장하지 않음. |
| Edoxaban(릭시아나 15mg, 30mg, 60mg) | · 심방세동, 심부정맥혈전증 및 폐색전증의 치료와 재발 위험 감소: 체중 60kg 이하, CrCl 15~50mL/min, P-gp 저해제 병용 시 30mg OD. 체중 60kg 초과 시 60mg OD · CrCl < 15mL/min 환자에서는 권장하지 않음 · P-gp 저해제: Verapamil, Quinidine, Cyclosporine, Dronedarone, Azithromycin, Clarithromycin, Erythromycin, Itraconazole(oral) |
| Dabigatran(프라닥사 110mg, 150mg) | · 심방세동: 150mg BID · 정맥 혈전색전증의 치료 및 재발 위험 감소: 150mg BID · 출혈의 위험이 있는 환자, 75세 이상, CrCl 30~50mL/min: 110mg BID · CrCl < 30mL/min 환자에서는 권장하지 않음 |
항응고제 사용의 적절성 평가는 약물의 필요성 및 유효성, 복약 순응도, 안전성 등의 검토 및 평가를 포함한다.
| 항응고제의 적절성 평가 | 약물요법 최적화 계획 |
|---|---|
| ▷ 약물 필요성 및 유효성 평가 · 적응증 및 적응증 지속 확인 |
· 복용 이유, 적응증 확인, 필요한 경우 복용 이유 설명을 통해 복약 순응도 향상 · 적응증 미지속의 경우(예: 환자 활동 제한에 따른 VTE 예방 목적으로 사용한 경우 등): 중단 가능성은 반드시 의사와 확인. 임의중단 불가 |
| ▷ 복약 순응도 평가 · 처방 용량, 용법 준수 평가 · 복약 순응도 평가 |
· 1주일에 몇 회 복용 잊는지 평가 · 복용량 인지 여부 평가 · 복용을 잊은 경우 대처법 평가 · Warfarin 모니터링 후 용량 변경 인지 여부 |
| ▷ 안전성 평가 - 병용약물 평가 · tNSAIDs: 출혈위험 증가 · 항혈소판제, 혈액순환 개선제: 출혈위험 증가, 의도적 병용 확인 · 항응고제 대사 억제/유도제 병용 여부 · 감염치료제(H. pylori 감염 포함), 경구용 진균제, 결핵약 등 병용 여부 |
· tNSAIDs의 경우 가급적 다른 약제로 변경 또는 최소한의 용량으로 단기간 사용(tNSAIDs 일부는 INR 상승, 또는 INR 상승없이 출혈위험 증가) · 항혈소판제는 스텐트 시술 등으로 인한 의도적인 병용인지, 의사가 인지하고 있는지 확인 필요 · NOAC과 상호작용이 있는 약물은 용량조절 확인 · warfarin은 병용 전후 PT 모니터링 권유 |
| ▷ 안전성 평가 - 위험상병 확인: · 출혈 기왕력 · 만성 신장병 등 고위험 동반질환 확인 · 체중, 연령 대비 용량 확인 |
· 출혈 기왕력 확인 시 의사의 인지 여부 확인 · 만성 신장병 등 고위험 질환 동반 여부와 이에 대한 의사의 인지 여부 확인 · 체중이나 연령에 따른 용량 적절성 평가 |
| ▷ 부작용 확인 · 출혈 징후 |
· 멍, 출혈 징후(적색뇨, 적변 등) 확인 · 다른 병의원 방문 시 항응고제 복용 사실 고지 교육 · 출혈 위험 증가 행위 주의: 근육주사, 침 등의 위험성 안내로 출혈 부작용 감소 |
| ▷ 일반약 복용/식이 주의사항, 기타 | · Aspirin, Ginko biloba 등 자가약 복용 여부 확인 및 검토 · NSAIDs 복용 검토 및 삼가를 권고 · 진통제 필요 시 Acetaminophen 추천 · Warfarin: 건강기능식품, 홍삼, 종합비타민은 추천되지 않음 · 녹황색 야채, 견과류 등은 일정량 유지를 추천 · 낫또 섭취 시 INR 감소로 warfarin 처방량 증가 가능성 확인 및 낫또 섭취 중단 시 항응고제 용량 조절 필요성 여부를 의사에게 검토 요구 중재 |
- References
Secco GG, Parisi R, Mirabella F, Fattori R, Genoni G, Agostoni P, De Luca G, Marino PN, Lupi A, Rognoni A. P2Y12 inhibitors: pharmacologic mechanism and clinical relevance. Cardiovasc Hematol Agents Med Chem. 2013 Jun;11(2):101-5. doi: 10.2174/1871525711311020005. PMID: 22963529.
Min P, Kang TS, Cho Y, et al. P2Y12 Inhibitor Monotherapy vs Dual Antiplatelet Therapy After Deployment of a Drug-Eluting Stent: The SHARE Randomized Clinical Trial. JAMA Netw Open. 2024;7(3):e240877. doi:10.1001/jamanetworkopen.2024.0877
Hulot, JS., Collet, JP. & Montalescot, G. Thienopyridine-Associated Drug-Drug Interactions: Pharmacologic Mechanisms and Clinical Relevance. Curr Cardiol Rep 13, 451–458 (2011).
Hakkola, J., Hukkanen, J., Turpeinen, M. et al. Inhibition and induction of CYP enzymes in humans: an update. Arch Toxicol 94, 3671–3722 (2020).
Patel S, Singh R, Preuss CV, et al. Warfarin. [Updated 2023 Mar 24]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK470313/
David Q. Pham, Antony Q. Pham, Interaction potential between cranberry juice and warfarin, American Journal of Health-System Pharmacy, Volume 64, Issue 5, 1 March 2007, Pages 490–494, https://doi.org/10.2146/ajhp060370
Kaminsky LS, Zhang ZY. Human P450 metabolism of warfarin. Pharmacol Ther. 1997;73(1):67-74. doi: 10.1016/s0163-7258(96)00140-4. PMID: 9014207.
Calvin H. Yeh, Kerstin Hogg and Jeffrey I. Weitz. Overview of the New Oral Anticoagulants: Opportunities and Challenges. Arteriosclerosis, Thrombosis, and Vascular Biology. 2015;35:1056–1065.
LiverTox: Clinical and Research Information on Drug-Induced Liver Injury [Internet]. Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases; 2012-. Antithrombotic Agents. [Updated 2020 Sep 25]. Available from: https://www.ncbi.nlm.nih.gov/books/NBK548679/
Schrör K. Aspirin and platelets: the antiplatelet action of aspirin and its role in thrombosis treatment and prophylaxis. Semin Thromb Hemost. 1997;23(4):349-56. doi: 10.1055/s-2007-996108. PMID: 9263351.
Hirata, T.D.C., Dagli-Hernandez, C., Genvigir, F.D.V. et al. Cardiovascular Pharmacogenomics: An Update on Clinical Studies of Antithrombotic Drugs in Brazilian Patients. Mol Diagn Ther 25, 735–755 (2021). https://doi.org/10.1007/s40291-021-00549-z
Saini HK, Takeda N, Goyal RK, Kumamoto H, Arneja AS, Dhalla NS. Therapeutic potentials of sarpogrelate in cardiovascular disease. Cardiovasc Drug Rev. 2004 Spring;22(1):27-54. doi: 10.1111/j.1527-3466.2004.tb00130.x. PMID: 14978517.
대한약사회 사이버연수원 학술자료(2024)
Copyright © MediGloPark's All Rights Reserved.
포괄적 노인평가와 다학제적 개입
 ▷ 포괄적 노인평가(Comprehensive Geriatric Assement, CGA)는 다학제적 진단과 치료과정으로서 의약적, 정신(심리)적, 신체적 기능들과 사회경제적 문제 등을 평가한다.
이는 노쇠한 노인 환자들을 위한 조화와 통일성 있는 계획의 수립에 매우 유용하다.
▷ 포괄적 노인평가(Comprehensive Geriatric Assement, CGA)는 다학제적 진단과 치료과정으로서 의약적, 정신(심리)적, 신체적 기능들과 사회경제적 문제 등을 평가한다.
이는 노쇠한 노인 환자들을 위한 조화와 통일성 있는 계획의 수립에 매우 유용하다.노인에서 쇠약하다는 것은 여러가지 만성질환을 동시에 가지고 있다는 것을 의미하며, 이와 관련된 건강전문가, 사회복지사, 의약, 간호 등을 포함하는 다학제 팀(Multidisciplinary Team, MDT) 중심으로 관리되어야 한다.
주로 담당의사 또는 일반의, 약사, 선임간호사, 물리치료사, 작업치료사, 지역사회 재활팀 등이 MDT 미팅에 참여하여야 하지만 상황에 따라 다양한 형태의 MDT 미팅이 이루어질 수 있다.
또한 환자가 원하는 사항을 설정하고 진행과정을 피드백하거나 예상되는 상황을 관리하기 위하여 환자 및 환자가족과 소통하는 것이 절대적으로 필요하다.
형태나 내용의 차이는 있을 수 있지만, 환자중심의 목표 설정 등을 포함한 노인 MDT 미팅의 핵심적인 요소들은 공통적이다.
| MDT 미팅의 핵심적 원칙 |
|---|
| 1. 환자중심의 목표를 설정하여야 한다. |
| 2. 의료문제, 생활기능, 인지 또는 정신의학적 건강, 시회적 환경 등의 영역들을 망라한다. |
| 3. 핵심적 지식 분야의 대표를 둔다. |
| 4. 개방적으로 함께 의견을 개진한다. |
| 5. 전체의 목표를 승인한다. |
| 6. 시간 구성에 따른 다음 단계를 승인한다. |
| 7. 책임을 할당한다. |
| 8. 진행과정을 다시 논의하기 위해 규칙적으로 재소집한다. |
| 9. MDT 미팅의 결과물을 공유한다. |
- References
Jung-Yeon Choi, Vasuki Rajaguru, Jaeyong Shin, Kwang-il Kim, Comprehensive geriatric assessment and multidisciplinary team interventions for hospitalized older adults: A scoping review, Archives of Gerontology and Geriatrics, Volume 104, 2023, 104831, ISSN 0167-4943, https://doi.org/10.1016/j.archger.2022.104831. (https://www.sciencedirect.com/science/article/pii/S0167494322002187)
Graham Ellis, Nick Sevdalis, Understanding and improving multidisciplinary team working in geriatric medicine, Age and Ageing, Volume 48, Issue 4, July 2019, Pages 498–505, https://doi.org/10.1093/ageing/afz021
Copyright © MediGloPark's All Rights Reserved.
비정형 삼환계 항우울제 - 티아넵틴(Tianeptine)
 ▷ 주요우울장애(major depressive disorder, MDD)의 약물치료는 복잡하며, 환자의 상태에 따라 정교하게 이루어져야 한다. 가장 우선적인 치료약물은 선택적 세로토닌 재흡수 저해제(selective serotonin reuptake inhibitor, SSRI), 세로토닌과 노르에피네프린 재흡수 저해제(serotonnin and norepinephrine reuptake inhibitor, SNRI), 그리고 세로토닌 조절제(serotonin modulator, SM) 등이다..
▷ 주요우울장애(major depressive disorder, MDD)의 약물치료는 복잡하며, 환자의 상태에 따라 정교하게 이루어져야 한다. 가장 우선적인 치료약물은 선택적 세로토닌 재흡수 저해제(selective serotonin reuptake inhibitor, SSRI), 세로토닌과 노르에피네프린 재흡수 저해제(serotonnin and norepinephrine reuptake inhibitor, SNRI), 그리고 세로토닌 조절제(serotonin modulator, SM) 등이다..티아넵틴(Tianeptine)은 구조적 유사성으로 삼환계 항우울제로 분류가 되었지만 다른 항우울제와 다르게 분자적, 기전적 특이점이 있으므로 비정형 삼환계 항우울제로 분류되며 불안과 과민성 대장증후군 치료 시 매우 효과적이다.
주요우울장애를 가진 환자들의 여러 뇌 영역에서는 glutamate 수준의 저하가 나타난다. 티아넵틴은 글루탐산성 신호를 안정화시키며 NMDA(N-methyl-d-aspartate) 수용체에 대한 저해 및 AMPA(aminomethylphosphonic acid) 수용체에 대한 간접적 효과를 나타내는데 이들 상호작용에 의해 항우울효과가 강화된다. 즉, 티아넵틴의 항우울효과에 대한 주된 작용기전은 기존의 역설적 세로토닌 재흡수 촉진 기전보다 오히려 glutamate 조절로 밝혀졌으며, mu-opioid 수용체에 대해 전적 작용제(full agonist)로서 작용하여 도파민 방출을 촉발하고 이에 따른 도취감을 나타낼 수 있으므로 중독이나 약물의 오남용을 주의하여야 한다.
우울증 치료 시 티아넵틴의 표준 용량은 1일 20-50mg이지만 기분전환용으로 오용 시 과량복용하여 중독은 물론 치명적일 수 있으므로 문제가 되고 있다. 티아넵틴의 반감기는 2.5시간으로 짧으며 위장관에서 빠르게 흡수된다. 노인환자와 신부전 환자의 경우 반감기가 현저하게 증가하고 과량복용 시 혈액투석이 효과가 없으므로 특히 주의가 필요하다.
티아넵틴은 만성적 사용자들에서 의존성과 내성이 발생하므로 주의가 필요하다. 특히 티아넵틴의 반감기가 짧으므로 중독과 오용의 문제가 더 증대될 수 있다. 오피오이드적 사용 시 그 치료에는 buprenorphine, naloxone과 같은 약이 필요할 수 있다.
- References
Edinoff AN, Sall S, Beckman SP, Koepnick AD, Gold LC, Jackson ED, Wenger DM, Cornett EM, Murnane KS, Kaye AM, Kaye AD. Tianeptine, an Antidepressant with Opioid Agonist Effects: Pharmacology and Abuse Potential, a Narrative Review. Pain Ther. 2023 Oct;12(5):1121-1134. doi: 10.1007/s40122-023-00539-5. Epub 2023 Jul 15. PMID: 37453966; PMCID: PMC10444703.
Alamo C, García-Garcia P, Lopez-Muñoz F, Zaragozá C. Tianeptine, an atypical pharmacological approach to depression. Rev Psiquiatr Salud Ment (Engl Ed). 2019 Jul-Sep;12(3):170-186. English, Spanish. doi: 10.1016/j.rpsm.2018.09.002. Epub 2019 Jan 3. PMID: 30612921.
Bailey SJ, Almatroudi A, Kouris A. Tianeptine: an atypical antidepressant with multimodal pharmacology. Curr Psychopharmacol [Internet]. 2018 Jan 2 [cited 2023 Mar 5];6(2). Available from http://www.eurekaselect.com/152697/article.
Gassaway, M., Rives, ML., Kruegel, A. et al. The atypical antidepressant and neurorestorative agent tianeptine is a μ-opioid receptor agonist. Transl Psychiatry 4, e411 (2014). https://doi.org/10.1038/tp.2014.30
Copyright © MediGloPark's All Rights Reserved.
가바펜티노이드(가바펜틴, 프레가발린)
 ▷ 항전간제인 가바펜틴은 시냅스 전 전압의존성(電壓依存性, voltage-gated) Ca2+과 Na+ 통로들을 줄여 시냅스 전달을 감소시킨다. 또한 외포작용(exocytosis)을 줄이고 시냅스 전 말단의 신경전달물질 방출을 감소시킨다. 가바펜틴은 칼슘 통로들의 α2–δ1 subunit에 작용하여 흥분성 시냅스의 형성을 감소시키며, α2–δ1 subunit에 특이적으로 친화성이 있고 α2–δ3 subunit들에는 친화성이 없는 것으로 연구되었다.
▷ 항전간제인 가바펜틴은 시냅스 전 전압의존성(電壓依存性, voltage-gated) Ca2+과 Na+ 통로들을 줄여 시냅스 전달을 감소시킨다. 또한 외포작용(exocytosis)을 줄이고 시냅스 전 말단의 신경전달물질 방출을 감소시킨다. 가바펜틴은 칼슘 통로들의 α2–δ1 subunit에 작용하여 흥분성 시냅스의 형성을 감소시키며, α2–δ1 subunit에 특이적으로 친화성이 있고 α2–δ3 subunit들에는 친화성이 없는 것으로 연구되었다.GABA에 대한 가바펜틴의 영향에 대한 연구는 일치하지 않는데, 인체 연구에서는 GABA 수준이 증가하는 것으로 나타났으나 시험관내 연구에서는 영향이 없는 것으로 나타났다.
가바펜틴은 신경전달물질인 glutamate 수준에 영향이 없는 것으로 연구되었으며, NMDA(N-methyl-D-aspartate) glutamate성 수용체와 PKC–ERK1/2(protein kinase C–extracellular signal-regulated kinase 1/2) 경로들에 대해서는 가바펜틴의 길항효과가 있는 것으로 알려졌다.
가바펜틴은 위산 조절제에 의해 효과가 감소하며 부작용은 심하지 않은 편이나 졸림, 어지럼증 등의 부작용으로 서서히 증량하여야 한다. 또한 금단증상 방지를 위해 서서히 감량하여야 한다. 가바펜틴은 흥분성 신경전달물질의 방출 억제작용 외에 세로토닌의 혈중 수준을 증가시키는 작용도 있는 것으로 보고되었다.
대규모 임상연구에서 가바펜틴의 탐닉적 오용과 이에 따른 보건상의 문제점들을 제시하고 있다. 가바펜틴 오용에 따른 현상은 개인마다 다양하게 나타나지만 보통 희열, 향상된 사교성, 마리화나와 유사한 기분 고양, 이완, 평온감 등이다. 동일한 가바펜티노이드(gabapentinoid)인 프레가발린(pregabalin)이 가바펜틴보다 더 중독성이 있으며, 이들의 과량복용이나 진정제와 같은 다른 약물과의 병용으로 인해 치명적인 결과가 니타날 수 있으므로 주의가 필요하다.
가바펜틴은 간의 대사효소, 혈장단백과의 상호작용이나 약물-약물 상호작용이 비교적 없는 약물로 알려져 있다. 따라서 간질환이 있는 고령 환자에게도 적절한 약이다, 그러나 losartan과 같은 일부 약물들은 가바펜틴과 병용 시 현저한 약물-약물 상호작용이 나타날 수 있다.
| 약물 | 가바펜틴과의 상호작용 결과 | 비고 |
|---|---|---|
| losartan | 운동신경 손상 | 동물실험 |
| ethacrynic acid | 운동 수행능 손상 | 동물실험 |
| morphine | 기면상태(嗜眠狀態), 구역, 현기증, 무도병(chorea), 시공(時空)의 혼미(spatiotemporal disorientation), 환시(visual hallucination), 정신병적 삽화 등 | 임상연구 |
| 카페인 | 항경련효과의 감소, 카페인에 의한 전기경련 역치의 감소, 가바펜틴의 보호효과 감소 등 | 동물실험 |
| carvedilol | 동물실험에서 가바펜틴의 항경련 활성 증가 | 뇌전증 치료에 응용 가능 |
| sertraline | 항경련 효과의 감소 | 동물실험 |
| tramadol | +가바펜틴(저용량)→통증감소에 상승효과 | 용량의존적(동물실험) |
| metamizol | +가바펜틴→염증성 통증 감소에 상승작용 | 용량의존적(동물실험) |
| sevelamer | 가바펜틴 효과의 감소 | 모니터링 필요. |
| cimetidine | 가바펜틴의 청소율 저하(12%) |
한편, 중증 근육무력증(Myasthenia gravis)이나 근육간대경련(myoclonus) 문제가 있는 환자에게 가바펜틴을 사용하는 것은 증상을 악화시킬 수 있으므로 조심하여야 한다. 특이적으로 한 임상연구에서는 가바펜틴 투여(400mg/day) 후 중증 근무력증(눈의 쇠약, 안면쇠약, 저작기관 쇠약, 피로, 혈청 아세틸콜린 수용체 항체의 증가 등)에서 나타나는 것과 유사한 증상들이 나타날 수 있는 것으로 보고하였다.
- References
Quintero GC. Review about gabapentin misuse, interactions, contraindications and side effects. J Exp Pharmacol. 2017 Feb 9;9:13-21. doi: 10.2147/JEP.S124391. PMID: 28223849; PMCID: PMC5308580.
Smith BH, Higgins C, Baldacchino A, Kidd B, Bannister J. Substance misuse of gabapentin. Br J Gen Pract. 2012 Aug;62(601):406-7. doi: 10.3399/bjgp12X653516. PMID: 22867659; PMCID: PMC3404313.
U. Bonnet, N. Scherbaum, How addictive are gabapentin and pregabalin? A systematic review, European Neuropsychopharmacology, Volume 27, Issue 12, 2017, Pages 1185-1215, ISSN 0924-977X, https://doi.org/10.1016/j.euroneuro.2017.08.430.
Copyright © MediGloPark's All Rights Reserved.
리튬과 조증, 양극성 장애
 우울증과 조증 삽화를 경험하는 양극성 장애에서 리튬은 효과적인 유지 치료제로서 기분을 안정화시키고 자살의 위험성을 감소시킨다.
여러 연구에서 리튬은 양극성 장애의 1차 선택약으로서 장기간 치료에 우선적으로 사용할 수 있는 것으로 보고되었다.
우울증과 조증 삽화를 경험하는 양극성 장애에서 리튬은 효과적인 유지 치료제로서 기분을 안정화시키고 자살의 위험성을 감소시킨다.
여러 연구에서 리튬은 양극성 장애의 1차 선택약으로서 장기간 치료에 우선적으로 사용할 수 있는 것으로 보고되었다.리튬은 19세기에 덴마크 신경학자인 Lange에 의해 처음으로 사용되었으며 1970년대에 유럽과 미국을 위시한 여러나라에서 양극성 장애 치료제로 등록되었다. 그 후 항경련제인 carbamazepine, valproate, lamotrigine 등과 비전형적 항정신병약들이 양극성 장애의 장기 치료제로 등록되었다.
양극성 장애에서는 뇌의 구조변화가 강하게 발생하는데 리튬은 신경보호작용을 하며 신경세포가 모여있는 회백질(灰白質, gray matter) 용적을 증가시키는 작용을 한다. 대체로 리튬은 뇌에서 적응기전을 활성화하는 외인성 보조제 역할을 한다.
리튬은 1가 양이온으로서 매우 반응성이 강하고 광범위하게 퍼져 있어서 대부분의 조직과 세포에 침투가 되므로 신경영양적 경로에서 생물학적 효과들에 대해 높은 예민도와 특이성을 나타낸다. 따라서 임상학적 치료 영역이 넓기도 하지만 부작용의 양상도 넓게 나타나는 것으로 알려져 있다.
리튬은 재발 위험성을 최소하하기 위해서 리튬의 혈청농도를 0.6~0.8mmol/L로 유지하는 것이 필요하다. 급성 조증 치료 시에는 0.6~1.0mmol/L까지 증가시켜야 하며 우울증에는 0.4~0.8mmol/L로 유지하는 것이 일반적이다. 리튬 배설은 신기능을 변화시키는 약물들에 의해 쉽게 영향을 받는데 ACE 저해제, 안지오텐신 수용체 길항제, 이뇨제, 그리고 비스테로이드성 소염진통제 등이 대표적이다.
| 약물 | 상호작용 |
|---|---|
| ACE 저해제, 안지오텐신II 수용체 길항제(sartans) | 리튬의 혈청농도 증가(리튬 독성 증가 → 리튬농도 모니터링 및 감량 고려) |
| thiazide계 이뇨제 | 나트륨 재흡수 증가. 리튬배설 감소. 혈청 리튬농도 증가 ( → thiazide계 이뇨제 회피 또는 모니터링 필요) |
| Amiloride | 집합관에서 상피 나트륨채널을 통해 리튬이 들어오는 것을 차단함 ( → 추천 이뇨제 임: 리튬 축적 감소. 신기능 개선) |
| 루프 이뇨제 (furosemide) , 칼륨보존성 이뇨제 (spironolactone) , 삼투성 methylxanthine (theophylline) | 리튬농도에 영향 |
| 비스테로이드성 소염진통제(NSAIDs) | cyclo-oxygenase(COX) 저해 → PG E2 감소 → 수입성 세동맥(afferent arteriole) 혈관 확장 감소 → 사구체로의 혈류가 감소 → 사구체 여과 감소 → 리튬 배설 감소 ( → 리튬 감량을 고려) |
| Acetazolamide | 리튬 배설 증가 |
리튬은 위장관 내에서 광범위하게 흡수되며, 가장 일반적이고 뚜렷한 약물-약물 상호작용은 본질적으로 약동학적이다. 신장 배설이 리튬의 혈청농도를 결정하는 가장 중요한 인자이므로 사구체 여과나 세뇨관 재흡수와 같은 신기능에 영향을 미치는 약물들과 같이 투여할 때 주된 약물상호작용이 나타난다.
탈수, 열성질환, 설사나 구토 등 위장관 질환, 약물상호작용, 수술기주위(手術期周圍) 관리 및 수술 등으로 인한 혈행동태적(血行動態的) 변화나 혈액 용적의 변화는 리튬의 혈청농도에 영향을 미치므로 리튬의 혈중 수준을 검사하여야 한다.
리튬의 반감기는 24시간이며 통상 5~7일 후 안정상태가 된다.
리튬이 분명한 신경보호 성질을 가지고 있고 리튬을 장기 복용 시 치매 위험성을 낮춘다는 보고도 있지만, 이와 관련하여 리튬이 치매 위험을 감소키기거나 예방하는지는 아직 명확하지 않다. 치매의 가장 일반적인 형태인 알츠하이머병의 경우 리튬이 아밀로이드와 타우의 병리를 감소시키고, 뉴런의 손실을 적게 하며, 시냅스 가소성 촉진과 인지기능 개선을 하는 것으로 많은 연구에서 나타났다. 여러 임상 연구에서 리튬은 알츠하이머병의 위험성을 감소시키고 가벼운 인지기능 손상과 초기 알츠하이머병의 진행을 막아주는 것으로 나타났다.
또한 리튬은 파괴적 칼슘 항상성을 안정화 하여 알츠하이머병의 후속 신경병인학적 과정을 약화시키는 것으로 나타났다.
리튬은 갈증, 구강건조, 피부이상, 진전(tremor), 기면상태(somnolence), 갑상선저항증 등 다양한 부작용을 유발할 수 있다. 리튬의 피부에 대한 영향은 리튬의 정상적 치료 혈청 수준에서도 발생할 수 있다. 리튬에 의한 피부반응의 형태는 뭉친 여드름(응괴성 여드름, acne conglobata), 화농성 한선염(hidradenitis suppurativa), 모포염(毛包炎, 毛囊炎, folliculitis), 탈모(alopecia), 미세모, 반구진 발진(macular/maculopapular rashes), 그리고 확산성, 홍반성, 소양성, 반구진성 분출 등이다.
| 독성 | 리튬의 부작용 | 조치 |
|---|---|---|
| 급성 | 어떠한 급성 부작용이나 이상증상(소변증가, 피부이상 등) | 리튬농도 측정 |
| 두통, 피로 | 복용중단 고려 | |
| 갈증, 구강건조, 금속성 미감 | 약물 검토 | |
| 부정맥 | 입원 | 설사, 구역, 구토, 다뇨증 | 수화(hydration) 검토. 혈액투석 고려 | 떨림(진전) | 약물 모니터링 및 검토 |
| 만성 | 인지적 영향(brain fog 등), 운동실조, 흥분, 정신착란, 게으름(나태) | 변화를 모니터링, 리튬농도를 최적화, 신경학적 의뢰 |
| 갑상선 또는 부갑상선 기능부전 | 변화를 모니터링, 리튬농도를 최적화, 내분비학적 의뢰 | |
| 신부전 | 변화를 모니터링, 리튬농도를 최적화, 신장병학적 의뢰 |
리튬에 의한 발진은 리튬 복용을 중단 후 5일이 경과하면 보통 진정된다. 또한, 리튬을 복용 시 저염식을 피해야 한다. 저염식의 경우 리튬의 혈중 농도가 증가하여 부작용 발생의 위험성이 커진다.
급성 양극성 장애 성인 환자에 대한 여러 치료제들의 약물학적인 효능, 수용성, 내약성, 안전성 등을 분석한 연구에서 aripiprazole, olanzapine, quetiapine, risperidone 등이 위약 대비 좀 더 우수한 수용성을 나타냈다.
| 급성 양극성 장애 치료제 리뷰(Kishi T. 등, 2022) | 결과 |
|---|---|
| aripiprazole, asenapine, carbamazepine, cariprazine, haloperidol, lithium, olanzapine, paliperidone, quetiapine, risperidone, tamoxifen, valproate, ziprasidone | outperformed response to treatment |
| aripiprazole, olanzapine, quetiapine, risperidone | lower all-cause discontinuation |
| topiramate | higher all-cause discontinuation |
| aripiprazole, asenapine, carbamazepine, cariprazine, haloperidol, lithium, olanzapine, paliperidone, quetiapine, risperidone, tamoxifen, valproate, ziprasidone | outperformed the improvement of mania symptoms |
| aripiprazole, asenapine, carbamazepine, cariprazine, haloperidol, lithium, olanzapine, paliperidone, quetiapine, risperidone, valproate, ziprasidone | lower discontinuation due to inefficacy |
| aripiprazole, olanzapine, quetiapine, risperidone | better acceptability than the placebo |
- References
McKnight RF, de La Motte de Broöns de Vauvert SJGN, Chesney E, Amit BH, Geddes J, Cipriani A. Lithium for acute mania. Cochrane Database Syst Rev. 2019 Jun 1;6(6):CD004048. doi: 10.1002/14651858.CD004048.pub4. PMID: 31152444; PMCID: PMC6544558.
Cookson J. Use of antipsychotic drugs and lithium in mania. British Journal of Psychiatry. 2001;178(S41):s148-s156. doi:10.1192/bjp.178.41.s148.
Nolen WA. More robust evidence for the efficacy of lithium in the long-term treatment of bipolar disorder: should lithium (again) be recommended as the single preferred first-line treatment? Int J Bipolar Disord. 2015 Jan 31;3:1. doi: 10.1186/s40345-014-0017-6. PMID: 25642404; PMCID: PMC4312318.
Seong Sool Shim, Ken Berglund, Shan Ping Yu; Lithium: An Old Drug for New Therapeutic Strategy for Alzheimer’s Disease and Related Dementia. Neurodegener Dis 5 December 2023; 23 (1-2): 1–12.
Swetha P, Rajeevi , Gupta PCB. Lithium induced rash: a case report. Indian J Psychiatry. 2022 Mar;64(Suppl 3):S691. doi: 10.4103/0019-5545.342043. Epub 2022 Mar 24. PMCID: PMC9129587.
Kishi, T., Ikuta, T., Matsuda, Y. et al. Pharmacological treatment for bipolar mania: a systematic review and network meta-analysis of double-blind randomized controlled trials. Mol Psychiatry 27, 1136–1144 (2022). https://doi.org/10.1038/s41380-021-01334-4
Malhi GS, Bell E, Outhred T, Berk M. Lithium therapy and its interactions. Aust Prescr. 2020 Jun;43(3):91-93. doi: 10.18773/austprescr.2020.024. Epub 2020 Jun 2. Erratum in: Aust Prescr. 2020 Aug;43(4):141. PMID: 32675910; PMCID: PMC7358048.
Copyright © MediGloPark's All Rights Reserved.
아나스트로졸(anastrozole), 레트로졸(letrozole), 엑스메스탄(exemestane)
 ▷ 아나스트로졸(anastrozole)과 레트로졸(letrozole)은 비스테로이드성 aromatase 저해제이며
엑스메스탄(exemestane)은 스테로이드성 aromatase 저해제이다.
아나스트로졸은 레트로졸, 엑스메스탄 등과 함께 2세대 aromatase 저해제로서 완경 후 여성의 호르몬 수용체 양성 유방암 초기에 보조치료제로 많이 쓰이고 있으며
타목시펜보다 유방암 재발율을 더 효과적으로 감소시키는 것으로 알려져 있다. 유방암 세포의 증식에 필요한 에스트로겐은 완경 후 난소에서 더 이상 만들어지지 않는다 할지라도
인체는 다른 곳에서 에스트로겐을 계속 만들기 때문에 에스트로겐에 의한 종양 성장이 지속적으로 촉진된다.
▷ 아나스트로졸(anastrozole)과 레트로졸(letrozole)은 비스테로이드성 aromatase 저해제이며
엑스메스탄(exemestane)은 스테로이드성 aromatase 저해제이다.
아나스트로졸은 레트로졸, 엑스메스탄 등과 함께 2세대 aromatase 저해제로서 완경 후 여성의 호르몬 수용체 양성 유방암 초기에 보조치료제로 많이 쓰이고 있으며
타목시펜보다 유방암 재발율을 더 효과적으로 감소시키는 것으로 알려져 있다. 유방암 세포의 증식에 필요한 에스트로겐은 완경 후 난소에서 더 이상 만들어지지 않는다 할지라도
인체는 다른 곳에서 에스트로겐을 계속 만들기 때문에 에스트로겐에 의한 종양 성장이 지속적으로 촉진된다.아나스트로졸은 bezyltriazole 유도체로서 aromatase에 경쟁적으로 결합하여 강력하고 선택적인 작용으로 에스트로겐 합성을 감소시키며 부신 스테로이드 호르몬에는 거의 영향을 미치지 않는 특징이 있다.
아나스트로졸은 주로 간에서 대사가 되며 혈장 반감기가 40-50시간이므로 1일 1회 투여가 적절하다.
아나스트로졸은 간 CYP450 효소에 의해 대사되는 약물들과 상호작용은 없으며, 유방암 환자에서 아나스트로졸과 타목시펜 또는 그 대사물인 N-desmethyltamoxifen 사이에 임상적으로 중요한 약물-약물 상호작용은 없었던 것으로 보고되었다.
한편, aromatase 효소인 CYP19은 이론적으로 메타돈의 대사에서 중요한 역할을 하는데 aromatase 저해제는 이 효소를 억제하여 체내 메타돈 수준이 증가하므로 호흡억제와 QTc 연장과 같은 매우 심각한 부작용 발생의 위험성이 커진다.
엑스메스탄은 CYP3A4에 의해 광범위하게 대사되므로 CYP3A4 활성을 유도하는 약물들은 엑스메스탄 활성을 저하시킬 수 있다. 반대로 CYP3A4 저해제들은 엑스메스탄의 대사를 저해하여 농도 증가로 부작용이 증가하게 된다.
| 약물상호작용 | 위험성 | |
|---|---|---|
| Aromatase Inbibitors | CYP19 저해로 methadone의 수준 증가 | 호릅억제. QTc 연장 |
| Exemestane | CYP3A4 inducers | 효과 저하 |
| Exemestane | CYP3A4 inhibitors | 부작용 증가 |
일부 생약제제는 phytoestrogen으로 알려진 화합물을 함유하여 다양한 에스트로겐 활성을 나타내어 에스트로겐 생성을 촉진하므로 aromatase 저해제의 효과를 상쇄 또는 저하시킬 수 있으므로 주의하여야 한다.
| aromatase 저해제 복용 시 유의사항 | 비고 | ||
|---|---|---|---|
| aromatase 저해제 | 완경 후 여성에서 최적의 유방암치료제임. 생존률 개선 및 2차적 침습성 유방암 발생 위험성의 저하(40%) | ||
| Anastrozole, Letrozole | 회피약물: 에스트로겐 유도체(estrdiol 등) | 효과감소 | |
| Anastrozole, Letrozole | 주의약물: aripiprazole, pimozide, defetilide, hydrocodone, methadone | 부작용 증가 | |
| Exemestane | 회피 또는 주의약물: 에스트로겐 유도체(estrdiol 등), efavirenz, nevirapine, rifampin, rifabutin, St John’s wort, carbamazepine, phenobarbital, phenytoin | 효과감소 | |
| Exemestane | 회피 또는 주의약물: saxagliptin, hydrocodone, methadone | 부작용 증가 | |
| 보조제 | 회피 또는 주의약물: Aletris, Alfalfa, Androstenediol, Androstenedione, Anise, Black/Blue cohosh, Chasteberry, Deer velvet, Diindolylmethane (DIM), Dong quai Fennel Flaxseed Ginseng, Guggul, Isoflavones/plant estrogens, Hu zhang, Kudzu, Licorice (plant), Maca, Milk thistle, Noni juice, Panax ginseng, Red clover, Red raspberry leaf, Resveratrol, Saw palmetto, Scarlet Pimpernel, Star anise, Wild yam, Valerian | 보조제로서 복용은 위험할 수 있음. |
- References
Sanford, M., Plosker, G.L. Anastrozole. Drugs 68, 1319–1340 (2008). https://doi.org/10.2165/00003495-200868090-00007
Heery M, Farley S, Sparkman R, Healy J, Eighmy W, Zahrah G, Zelkowitz R. Precautions for Patients Taking Aromatase Inhibitors. J Adv Pract Oncol. 2020 Mar;11(2):184-189. doi: 10.6004/jadpro.2020.11.2.6. Epub 2020 Mar 1. PMID: 33532117; PMCID: PMC7848814.
Copyright © MediGloPark's All Rights Reserved.
디오스민(Diosmin)에 의한 CYP3A 효소활성의 감소
 ▷
디오스민(diosmin)은 플라본(flavone) 배당체로서 수 많은 플라보노이드 중 하나이며 감귤류에서 많이 발견된다.
디오스민은 많은 연구에서 항산화, 항고혈당(antihyperglycemic), 항염, 항돌연변이(antimutagenic), 항균, 항암, 항궤양,
간 및 신경보호 작용 등 많은 생물학적 특징이 있는 것으로 보고되었다.
▷
디오스민(diosmin)은 플라본(flavone) 배당체로서 수 많은 플라보노이드 중 하나이며 감귤류에서 많이 발견된다.
디오스민은 많은 연구에서 항산화, 항고혈당(antihyperglycemic), 항염, 항돌연변이(antimutagenic), 항균, 항암, 항궤양,
간 및 신경보호 작용 등 많은 생물학적 특징이 있는 것으로 보고되었다.디오스민은 치질과 하지정맥류에 주로 쓰이며 부종을 감소시키고 정상적인 혈관기능으로 회복시키는 작용을 한다. 또한, 혈류가 제한되는 정맥부전 환자에서 염증을 감소시키고 혈류를 정상으로 회복시키는데 도움이 된다.
순환기계를 비롯한 많은 주요 인체기관에 대한 디오스민의 유익한 효과가 밝혀짐에 따라 만성정맥부전(chronic venous insufficiency, CVI) 등 다양한 질병의 치료에 가장 많이 찾는 천연물 중의 하나이다. 특히 각종 암세포에서 세포자연사(apoptosis)를 유도하는 것으로 알려져 있으며 당뇨 뿐만 아니라 이와 관련된 합병증인 신경병증(neuropathy)과 이상지질혈증(dyslipidemia) 치료에도 효과가 있는 것으로 보고되었다.
디오스민은 단독으로도 우수한 약물이지만 다른 플라보노이드와 병용투여 시에도 우수한 효과가 나타난다. 응급의 급성치핵에 대한 약물치료에 diosmin, troxerutin 및 hesperidin의 병용투여가 비교적 안전하며 매우 효과적인 것으로 보고되었는데 이들 약물을 투여 후 12일 경과 시 통증, 출혈, 지속적 부종 및 혈전환자 비율이 의미있게 감소하는 것으로 나타났다.
경구투여 시 디오스민은 diosmetin으로 전환되어 흡수되며 글루쿠로나이드 결합체(glucuronide conjugate)로 에스테르화 되어 소변으로 배설된다.
한편, 연구결과에 따라 논란의 여지가 있지만 디오스민에 의해 간 마이크로솜의 CYP3A4 효소활성이 감소하여 CYP3A4 기질약물들의 대사가 저해될 수 있다는 보고가 있으므로 CYP3A에 의해 대사되는 약물들은 주의가 필요하다. 한 연구에서 디오스민이 CYP3A4를 저해하여 그 기질이 되는 carbamazepine의 대사가 감소하고, 그 결과로서 cabamazepine의 혈중농도가 상승하였으며, 배설은 감소하였고, carbamazepine의 활성형 대사물의 형성도 감소한 것으로 나타났다.
| CYP3A 기질약물 |
|---|
| Alfentanil Alprazolam Amlodipine Amprenavir Buspirone Chlorpheniramine Citalopram Cyclosporine Dapsone Diltiazem Efavirenz Erythromycin Felodipine Fentanyl Indinavir Isradipine Itraconazole Lidocaine Loratidine Methadone Midazolam Nelfinavir Nicardipine Nifedipine Oxycodone Simvastatin Sirolimus Tacrolimus Zolpidem |
- References
Huwait E, Mobashir M.: Potential and Therapeutic Roles of Diosmin in Human Diseases. Biomedicines. 2022 May 6;10(5):1076.
Giannini I, Amato A, Basso L, Tricomi N, Marranci M, Pecorella G, Tafuri S, Pennisi D, Altomare DF: Flavonoids mixture (diosmin, troxerutin, hesperidin) in the treatment of acute hemorrhoidal disease: a prospective, randomized, triple-blind, controlled trial. Tech Coloproctol. 2015 Jun;19(6):339-45.
Bedada SK, Neerati P.: Modulation of CYP3A enzyme activity by diosmin and its consequence on carbamazepine pharmacokinetics in rats. Naunyn Schmiedebergs Arch Pharmacol. 2018 Feb;391(2):115-121.
Bedada SK, Boga PK.: Influence of diosmin on the metabolism and disposition of carbamazepine in healthy subjects. Xenobiotica. 2017 Oct;47(10):879-884.
Orzetti, S.; Baldo, P. Toxicity Derived from Interaction between Natural Compounds and Cancer Therapeutic Drugs Metabolized by CYP3A4: Lessons Learned from Two Clinical Case Reports. Int. J. Mol. Sci. 2023, 24, 15976. https://doi.org/10.3390/ijms242115976.
Copyright © MediGloPark's All Rights Reserved.
타목시펜(tamoxifen, Nolvadex® or Soltamox®)
 ▷ 타목시펜(tamoxifen, Nolvadex® or Soltamox®)은 에스트로겐(그리고/또는 프로게스테론)을 증식에 필요로 하는
호르몬 수용체 양성(hormone receptor-positive, hormone-positive) 유방암에 대한 선택적 에스트로겐 수용체
조절제이다. 호르몬 수용체 양성 유방암은 전체 유방암의 70-75%를 차지한다.
▷ 타목시펜(tamoxifen, Nolvadex® or Soltamox®)은 에스트로겐(그리고/또는 프로게스테론)을 증식에 필요로 하는
호르몬 수용체 양성(hormone receptor-positive, hormone-positive) 유방암에 대한 선택적 에스트로겐 수용체
조절제이다. 호르몬 수용체 양성 유방암은 전체 유방암의 70-75%를 차지한다. 에스트로겐은 난포(卵胞, ovarian follicle)와 부신(副腎, adrenal gland)에서 주로 생성되며, 에스트로겐 수용체는 호르몬 등의 결합으로 세포핵내(細胞核内, intranuclear) DNA전사(転写, transcription)를 조절하는 핵내수용체(核內受容體, nuclear receptor)이다. 에스트로겐 수용체의 기능은 17β-estradiol에 의해 중개(仲介)되며, 세포의 재생 뿐만 아니라 세포의 성장과 분화과정에서 유전자 전사를 활성화 시킨다.
타목시펜은 에스트로겐 수용체의 두 아형(subtype)인 에스트로겐 α 및 β 수용체 중 에스트로겐수용체α에서 17β-estradiol과 경쟁적 작용을 하여 17β-estradiol의 유사분열촉진(有絲分裂促進, mitogenic) 작용을 차단한다. 즉, 에스트로겐수용체α는 호르몬이 없으면 불활성화 되는데, 타목시펜은 에스트로겐수용체α에 작용하여 세포증식을 억제한다.
타목시펜의 효과에 대한 내성 발생은 호르몬치료에서 주된 장애물이다. 대부분 수 년 이내에 에스트로겐 양성 유방암 환자의 30%에서 타목시펜 획득내성이 발생한다.
타목시펜은 prodrug으로서 cytochrome P450 (CYP) 2D6 효소에 의한 대사물인 endoxifen이 유방암 치료에 직접적인 효과가 있다. 타목시펜의 약물-약물 상호작용에 대해서는 논란이 있지만, CYP2D6 저해제와 효소 유도제(enzyme inducer) 모두 타목시펜의 효과를 저하시킬 수 있는 것으로 보고되어 있다. 효소 유도제는 타목시펜과 타목시펜 대사물, 특히 활성형 대사물인 endoxifen을 불활성형인 glucuronide 대사물로 강하게 전환시키는 것으로 알려져 있다.
| 분류 | 약물 |
|---|---|
| CYP2D6 Inhibitors | Abiraterone Diphenhydramine Paroxetine Amiodarone Dronedarone Perphenazine Berberine (Goldenseal) Eliglustat Promethazine Bupropion Fluoxetine Propafenone Celecoxib Halofantrine Propoxyphene Chloroquine Haloperidol Quinacrine Chlorpheniramine Hydroxychloroquine Quinidine Chlorpromazine Lorcaserin Quinine Cinacalcet Lumefantrine Ritonavir Clobazam Mirabegron Rolapitant Cobicistat Moclobemide Terbinafine Darifenacin Panobinostat Thioridazine |
| Enzyme/transporter inducers | Aminoglutethimide Etravirine Phenytoin Armodafinil Fosphenytoin Primidone Bexarotene Griseofulvin Rifabutin Bosentan Lesinurad Rifampin Carbamazepine Lumacaftor Rifapentine Dabrafenib Mitotane St John’s wort Dexamethasone Modafinil Troglitazone Efavirenz Nevirapine Vemurafenib Enzalutamide Oxcarbazepine Vinblastine Eslicarbazepine Phenobarbital |
타목시펜 치료 시 천연물 중 당귀(Angelica sinensis), 작약(Paeonia lactiflora), 지황(Rehmannia glutinosa), 황기(Astragalus mongholicus), 감초(Glycyrrhiza glabra) 등은 에스트로겐과 유사한 활성을 나타내므로 타목시펜의 항암효과를 저하시킬 수 있다.
밀크시슬, 녹차, 미리세틴(myricetin), 모린(morin), 바이칼레인(baicalein), 커큐민(Curcumin), 캠퍼롤(Kaempferol), 퀘르세틴(quercetin) 등은 타목시펜과 그 대사물의 생체이용률을 증가시키는 것으로 알려져 있으나, 커큐민의 경우 타목시펜의 효과를 감소시킨다는 보고도 있어서 천연물과 타목시펜을 같이 사용하는 것에 대한 임상적 연구 결과들은 논란의 여지가 있고 제한적이므로 더 심층적인 연구가 필요하다.
타목시펜을 복용 중인 환자가 주의하여야 할 사항은 다음과 같다.
| 분류 | 타목시펜 치료 시 회피악물 또는 주의사항 | 비고 |
|---|---|---|
| 항우울제 | bupropion, duloxetin, fluoxetine, paroxetine | 항암효과 감소 |
| 심장약 | amiodarone, dronedarone, quinidine, sotalol, ticlopidine | 항암효과 감소 |
| HIV 치료제 | cobicistat, ritonavir, tipranavir, elvitegravir, emtricitabine, tenofovir alafenamide, tenofovir disoproxil fumarate | 항암효과 감소 |
| 정신신경용제 | perphenazine, pimozide, thioridazine | 항암효과 감소 |
| 항감염제 | hydroxychloroquine, quinidine, rifampin, terbinafine | 항암효과 감소 |
| 기타 | cinacalcet, conivaptan, haloperidol, mirabegron | 항암효과 감소 |
| 항응고제 | warfarin | 모니터링 필요 |
| 에스트로겐제제 | 모든 에스트로겐제제 | 주치의와 상의 |
| 비타민 | 비타민 E, 비타민 C | 항암효과 감소 |
| 기타 | colchicine, dabigatran, rifaximin, rivaroxaban | 부작용 증가 위험 |
| 음주 | alcohol(금주 또는 제한 필요) | 약효감소 |
| 수술 | 출혈 증가의 위험성이 있으므로 수술 전 수 일 동안 복약중지가 필요할 수도 있음. | 외과의와 상의 |
| 생약 | 당귀(Angelica sinensis), 작약(Paeonia lactiflora), 지황(Rehmannia glutinosa), 황기(Astragalus mongholicus), 감초(Glycyrrhiza glabra) | 에스트로겐과 유사한 활성 |
| 안과 | 망막증(retinopathy) 주의(2년 이상 타목시펜을 복용하는 경우 6개월마다 검진이 필요) | 시력저하 |
Cox2 저해제인 celecoxib는 타목시펜의 에스트로겐 양성 유방암 세포 성장 억제작용을 촉진하는데, 무독성 용량에서 타목시펜과 세레콕시브 조합은 신생혈관생성 억제작용을 나타낸다. PKC(Protein Kinase C)와 mTOR(mammalian Target Of Rapamycin, mechanistic Target Of Rapamycin) 저해제인 everolimus도 타목시펜과 병용치료 시 타목시펜 단독치료에 비하여 의미있는 임상적 유익성이 있는 것으로 알려져 있다.
타목시펜 치료를 향상시키고 그 세포독성을 개선하는 천연물의 예는 카르노산(carnosic acid)이 있다. 카르노산은 타목시펜과 병용치료 시 유방암세포의 세포자연사(apoptosis)를 유도한다. 다른 예로는 에쿠올(equol), 티모퀴논(thymoquinone), 카페익산 페네틸 에스테르(caffeic acid phenethyl ester), 리코펜(lycopene), 아연 등이 있다. 또한, 동물실험에서 타목시펜 치료에 가장 효과적으로 도움을 주는 영양소로는 리보플라빈, 나이아신 및 코엔자임Q10으로서 과산화지질(lipid peroxide) 수준을 회복시키고 항암 활성을 촉진하는 것으로 나타났다.
비타민 E는 삶의 질 개선, 유방암의 화학예방법(chemo-prevention), 타목시펜의 부작용 극복에 효과적인 것으로 알려져 있고 항산화 효과가 있어서 산화적 스트레스로 부터 세포를 보호하는 필수적 역할을 한다. 토코트리에놀(tocotrienol)과 비타민 E 에스테르는 강한 화학예방활성을 나타내며, 특히 토코트리에놀은 8mcg/mL의 농도에서 에스트로겐 양성 유방암 세포의 성장을 완전하게 저해하며, 세포자연사(apoptosis)를 촉발시키는 것으로 알려져 있다. 그러나 항산화 비타민 보조제가 호르몬 치료, 방사선 치료, 그리고 화학요법에서 암세포도 보호하는 역할을 하게 되어 실제적으로는 치료 효과를 떨어뜨릴 수 있다는 연구 결과들이 있다. 따라서 타목시펜 치료 시 비타민 E 결핍증이 없다면 비타민 E 복용은 추천되지 않는다. 비타민 E와 다른 항산화제들의 생물학적 활성은 개인별로 여러 요인들에 의존하므로 환자의 상태를 신중히 모니터링하여 장기복용에 따른 부작용의 감소, 통증관리, 효과적인 영양요법 등을 고려한 다학제적 치료가 되어야 한다.
비타민 C는 항산화 작용과 면역기능 촉진 작용이 있어서 암 치료 중 특히 많이 복용하는 보조제이지만, 타목시펜의 유방암 세포에 대한 지질 과산화(lipid peroxidation) 세포독(cytotoxic) 활성에 대해 암세포를 용량의존적으로 보호하여 항암작용을 저해하므로 타목시펜 치료 시 결핍증이 없는 경우 비타민 C 보조제 복용은 피해야 한다.
비타민 D와 그 유사체들은 유방암의 다양한 호르몬 수용체 발현에 대한 조절작용이 있고 타목시펜에 대한 감수성을 증가시키는 유익한 효과가 기대되는 것으로 알려져 있다. 즉, 타목시펜은 항암작용에도 불구하고 반대편 부위에 에스트로겐 수용체 α-양성(estrogen receptor α-positive) 종양의 확산을 촉진할 수 있고 에스트로겐 수용체 α-음성 종양 발생의 위험성도 증가시키는 것으로 알려져 있는데, 비타민 D가 NF-κB(Nuclear factor kappa B)를 저해하여 에스트로겐 수용체 α의 발현을 하향조절하므로 에스트로겐 수용체-음성 암세포에서 기능적 에스트로겐 수용체 α를 유도하여 타목시펜에 대한 감수성을 증가시킬 수 있으며, 비타민 D와 타목시펜을 같이 사용하면 타목시펜 내성 종양에 효과적일 수 있는 것으로 보고되었다. 따라서 비타민 D는 유방암의 예방 및 치료에 도움이 되는 것으로 생각되나 이에 대한 좀 더 대규모의 심층적 연구가 필요한 것으로 보인다.
타목시펜 치료 시 보통 나타나는 부작용 중의 하나인 비알콜성 지방간은 타목시펜이 에스트로겐 수용체 활성을 억제하여 발생한다. 동물실험에서 비타민 D는 타목시펜에 의해 발생한 간 지질대사장애에 개입하여 지방간을 억제할 수 있는 것으로 나타났다.
한편, 타목시펜의 부작용은 다양하지만 망막독성에 대한 여러 연구에서 1일 20mg을 2년 이상 복용한 환자의 12%에서 망막증(retinopathy)이 나타나는 것으로 보고되었다. 이들 중 절반 정도의 환자에서 시력의 병증을 나타냈다. 망막변화에는 주로 결정성 침착물(crystalline deposits), 낭포황반부종(cystoid macular edema, CME), 내부 망막층의 과반사성 침착물(hyperreflective deposits), 그리고 모세혈관확장증(毛細血管擴張症, telangiectasia) 등이 있다.
타목시펜에 의한 망막증이 나타나면 암의 예후에 따라 타목시펜 치료를 중단하기도 하지만, 타목시펜 치료를 중단해도 일단 변화된 시력의 개선은 거의 없다. 유리체내 스테로이드 주사요법 또는 항혈관 내피성장인자(antivascular endothelial growth factor) 치료가 시행되고 있으나 좀 더 연구가 필요하다. 따라서 타목시펜 치료를 2년 이상 받고 있는 경우에는 광간섭단층촬영(optical coherence tomography, OCT) 스크리닝을 통해 망막변화를 6개월마다 관찰해서 타목시펜 치료에 의한 시력손상의 위험성이 나타나기 전에 타목시펜 치료를 조정할 수 있는지 의사와 검토하여야 한다.
타목시펜은 유방암 진단 후 새로운 유방암 발생 및 재발을 위해 최소 5년 동안 복용하며 10년까지 복용하는 경우도 있다. 타목시펜 치료는 생존률을 높이며 재발성 침습성 유방암의 재발 위험성을 40%까지 낮추는 것으로 알려져 있다.
타목시펜의 일반적인 부작용은 다음과 같다.
| 타목시펜의 일반적인 부작용 |
|---|
| 갱년기 유사 증상(얼굴이 화끈거림, 야간한출, 질 건조증 등), 체중증가 또는 체액저류(부종), 생리불순 또는 무월경, 하지부종, 구역감, 질 분비물, 피부 발진, 남성 발기부전, 피로, 두통 등 |
- References
Chan, WJ.J., Adiwidjaja, J., McLachlan, A.J. et al: Interactions between natural products and cancer treatments: underlying mechanisms and clinical importance. Cancer Chemother Pharmacol 91, 103–119 (2023). https://doi.org/10.1007/s00280-023-04504-z.
Philip D. Hansten: The Underrated Risks of Tamoxifen Drug Interactions. Eur J Drug Metab Pharmacokinet (2018) 43:495–508.
Yen C, Zhao F, Yu Z, Zhu X and Li CG; Interactions Between Natural Products and Tamoxifen in Breast Cancer: A Comprehensive Literature Review. Front. Pharmacol. 13:847113. doi: 10.3389/fphar.2022.847113
Stephen Tenney, Aruoriwo Oboh-Weilke, David Wagner, Mike Yuan Chen: Tamoxifen retinopathy: A comprehensive review. Survey of Opthalmology. Volume 69, Issue 1, P42-50, 2024.
Mary Heery: Precautions for Patients Taking Tamoxifen or Aromatase Inhibitors. J Adv Pract Oncol. Vol 14, No 6, 2023. Farid Khallouki et al: An Update on Tamoxifen and the Chemo-Preventive Potential of Vitamin E in Breast Cancer Management. J Pers Med. 2023, 13, 754.
Subramani T, Yeap SK, Ho WY, Ho CL, Omar AR, Aziz SA, Rahman NM, Alitheen NB. Vitamin C suppresses cell death in MCF-7 human breast cancer cells induced by tamoxifen. J Cell Mol Med. 2014 Feb;18(2):305-13. doi: 10.1111/jcmm.12188. Epub 2013 Nov 25. PMID: 24266867; PMCID: PMC3930417.
Babu JR, Sundravel S, Arumugam G, Renuka R, Deepa N, Sachdanandam P. Salubrious effect of vitamin C and vitamin E on tamoxifen-treated women in breast cancer with reference to plasma lipid and lipoprotein levels. Cancer Lett. 2000 Apr 3;151(1):1-5. doi: 10.1016/s0304-3835(99)00340-7. PMID: 10766415.
Ahmed, N.S., Samec, M., Liskova, A. et al. Tamoxifen and oxidative stress: an overlooked connection. Discov Onc 12, 17 (2021). https://doi.org/10.1007/s12672-021-00411-y
Thabet RH, Gomaa AA, Matalqah LM, Shalaby EM. Vitamin D: an essential adjuvant therapeutic agent in breast cancer. Journal of International Medical Research. 2022;50(7). doi:10.1177/03000605221113800
Maoxuan Wu, Jie Wang, Wanqing Zhou, Mengting Wang, Chunyan Hu, Ming Zhou, Kailin Jiao, Zhong Li, Vitamin D inhibits tamoxifen-induced non-alcoholic fatty liver disease through a nonclassical estrogen receptor/liver X receptor pathway, Chemico-Biological Interactions, Volume 389, 2024, 110865, ISSN 0009-2797, https://doi.org/10.1016/j.cbi.2024.110865.
Copyright © MediGloPark's All Rights Reserved.
부프레노르핀(buprenorphine)
 ▷ 부프레노르핀(buprenorphine)은 통증치료와 오피오이드 사용 장애에 많이 사용된다. 통증치료에는 패취제(예, 노스판패취)가 많이 쓰인다.
▷ 부프레노르핀(buprenorphine)은 통증치료와 오피오이드 사용 장애에 많이 사용된다. 통증치료에는 패취제(예, 노스판패취)가 많이 쓰인다.부프레노르핀은 양귀비꽃으로부터 유래된 오피오이드 알카로이드 테바인(thebaine)의 반합성 유도체로서 높은 친유성을 갖고 있다.
부프레노르핀은 약물규제법령상 스케줄 III(Schedule III) 약물로 분류되는 부분적 오피오이드 작용제로서 그 최대효과는 전적작용제(全的作用劑, full agonist)보다 약하다. 용량을 높여도 그 효과가 증가하지 않는 천정효과(ceiling effect)를 나타내므로 호흡억제의 부작용이 제한적이어서 전적 오피오이드 작용제에 비해 더 안전하다.
부프레노르핀은 μ오피오이드 수용체에 대해 친화성은 높지만 내재성 활성(内在性活性, intrinsic activity)은 낮으며, 모르핀(morphine), 메타돈(methadone) 및 다른 전적작용제를 그들 수용체에서 치환할 수 있다. 전적작용제는 부프레노르핀을 치환할수 없으므로 부프레노르핀은 헤로인과 여타 전적 오피오이드 작용제의 강한 작용을 효과적으로 약화시킨다.
부프레노르핀은 결합한 수용체로부터 천천히 분리되므로 작용시간이 길다. 최종적 반감기는 정맥주사후 3시간부터 28시간, 설하 투여의 경우는 37시간이다.
부프레노르핀은 cytochrome P450(CYP) 3A4 대사를 광범위하게 받기 때문에 이에 따른 강한 약물-약물 상호작용이 발생할 수 있으며 CYP2C8도 대사에 관여한다. CYP3A4의 기질인 부프레노르핀은 케토코나졸(ketoconazole)과 같은 CYP3A4 저해제에 의해 부프레노르핀의 체내 수준 또는 약력학적(pharmacodynamic) 효과가 증가하므로 주의하여야 한다.
| 분류 | CYP3A 저해제 |
|---|---|
| Strong CYP3A inhibitors(Cause ≥ 5-fold increase in AUC of sensitive CYP3A substrate) | atazanavir, clarithromycin, indinavir, itraconazole, ketoconazole, nefazodone, nelfinavir, ritonavir, lopinavir/ritonavir, saquinavir/ritonavir, telithromycin |
| Moderate CYP3A inhibitors(Cause ≥ 2 but <5-fold increase in AUC of sensitive CYP3A substrate) | aprepitant, diltiazem, erythromycin, fluconazole, fosamprenavir, grapefruit juice, verapamil |
| Weak CYP3A inhibitors(Cause ≥ 1.25 but <2-fold increase in AUC of sensitive CYP3A substrate) | cimetidine |
한편, 리팜피신(rifampicin, rifampin)과 같은 강한 CYP3A4 유도제(inducer)는 부프레노르핀의 효과를 저하시킨다.
| CYP3A4 유도제 |
|---|
| phenobarbital, phenytoin, rifampicin, St. John’s Wort and glucocorticoids |
부프레노르핀의 부작용은 다른 오피오이드류와 유사하며 일반적인 부작용은 다음과 같다.
| 부프레노르핀의 일반적인 부작용 |
|---|
| 변비, 수면장애, 졸음, 발한, 두통, 구기, 성욕저하 등. |
- References
Elinore F. McCance-Katz, Lynn Sullivan and Srikanth Nallani: Drug Interactions of Clinical Importance among the Opioids, Methadone and Buprenorphine, and other Frequently Prescribed Medications: A Review. Am J Addict. 2010 ; 19(1): 4–16.
Jahnavi Kharidia, EleanorM.Howgate, CelineM.Laffont, Yongzhen Liu,and Malcolm A. Young: Evaluation of Drug-Drug Interaction Liability for Buprenorphine Extended-Release Monthly Injection Administered by Subcutaneous Route. Clinical Pharmacology in Drug Development. 2021:10(9):1064-1074.
ROGER ZOOROB, ALICIA KOWALCHUK AND MARIA MEJIA DE GRUBB: Buprenorphine Therapy for Opioid Use Disorder. Am Fam Physician. 2018;97(5):313-320.
Copyright © MediGloPark's All Rights Reserved.
쇠약함(노쇠)에 따른 다제약물 위험성의 증가
 ▷ 쇠약(또는 노쇠, Frailty)하다는 것은 여러가지의 요인들이 복합되어 일어나는 증상으로 감염이나 약물 부작용과 같은 외부의 스트레스 요인들에 대해 회복력이
감소되어 있다는 것을 의미한다.
▷ 쇠약(또는 노쇠, Frailty)하다는 것은 여러가지의 요인들이 복합되어 일어나는 증상으로 감염이나 약물 부작용과 같은 외부의 스트레스 요인들에 대해 회복력이
감소되어 있다는 것을 의미한다.쇠약함에 따른 5가지의 대표적 증상은 다음과 같다.
| 노인병학적 5대 문제 | |
|---|---|
| 1 | 낙상(落傷, Falls) |
| 2 | 부동성(不動性, Immobility) |
| 3 | 섬망(譫妄, Delirium) 또는 망상(妄想, Delusion) |
| 4 | 실금(失禁, Incontinence) |
| 5 | 약물 부작용에 대한 민감성 |
여러질병을 동시에 가지고 있는 경우(multimorbidity)가 많기 때문에 쇠약한 환자들에서 다제약물은 일반적인 상황이다. 특히 노인 또는 쇠약 환자에서 신기능 저하와 같은 약물동력학적 변화는 약물에 대한 민감성을 증가시켜 약물 부작용, 낙상, 인지기능 손상, 섬망발생 등의 가능성이 증가하게 된다. 이러한 문제는 결국 많은 약물들에 노출된 노쇠한 환자들에서 입원과 유병율을 증가시키는 결과를 초래하게 된다.
따라서 이러한 상황에서는 약물 리뷰 등을 포함한 효과적인 개입이 매우 유익하다.
약물동력학적 변화, 동시다발적 만성질환, 약물의 효과, 복약충실도 등 환자에게 중요한 모든사항들이 약물 리뷰에서 빠짐없이 검토되어야 한다.
- References
Onder G, Marengoni A.: Polypharmacy. JAMA. 2017;318(17):1728. doi:10.1001/jama.2017.15764.
Chang, T.I., Park, H., Kim, D.W. et al: Polypharmacy, hospitalization, and mortality risk: a nationwide cohort study. Sci Rep 10, 18964 (2020). https://doi.org/10.1038/s41598-020-75888-8
All Wales Medicines Strategy Group. Polypharmacy in older people: A guide for healthcare professionals. March 2023.
Copyright © MediGloPark's All Rights Reserved.
다제약물은 최고의 적절성을 유지하여야 한다.
 ▷ 다양하고 복잡한 상황에 있는 환자에게 다제약물(polypharmacy)이 최고의 적절성을 유지하기 위해서는 최선의 증거에 근거하여 최적화되어 처방되어야 한다.
▷ 다양하고 복잡한 상황에 있는 환자에게 다제약물(polypharmacy)이 최고의 적절성을 유지하기 위해서는 최선의 증거에 근거하여 최적화되어 처방되어야 한다.다제약물의 문제는 처방된 약물이 환자에게 부적절하거나 의도된 약물의 유익성이 판단되지 않을 때 발생한다.
부적절한 다제약물의 예는 다음과 같다.
| 부적절한 다제약물의 예 | |
|---|---|
| 1 | 증거에 근거하지 않은 치료 |
| 2 | 약물의 위험성이 치료의 유익성을 상회하는 경우 |
| 3 | 약물상호작용이 의도하지 않은 부작용을 야기하는 경우 |
| 4 | 과도한 알약 부담으로 임상적으로 유용한 복약충실성 달성이 어려운 경우 |
| 5 | 처방약의 부작용을 치료할 목적으로 다른 약물을 처방하는 경우 |
영국의 King's Fund(2023년)에서 제시하는 고위험 다제약물 식별의 실제는 다음과 같다.
| 고위험 다제약물의 실제 | |
|---|---|
| 1 | 환자가 10개 또는 그 이상의 약물을 규칙적으로 복용하는 경우 |
| 2 | 환자가 4~9개의 약물을 규칙적으로(예, 매일 또는 매주) 복용하면서 다음의 경우에 해당하는 경우 a) 심각한 부적절 처방에 해당하는 약이 최소한 하나가 있는 경우 b) 확실하고 강한 약물-약물 상호작용 위험성의 근거가 있거나 임상적 금기에 해당하는 경우 c) 복약충실성의 문제 등 약물복용 곤란에 대한 임상적 기록의 근거가 있는 경우 d) 단 하나의 주 진단기록이 있거나 전혀 없는 경우(많은 수의 약물들이 다수의 임상적 조건이 없는 환자에게 합당하지 않은 것으로 예상되는 경우) e) 말기케어나 임시방편적 케어를 받는 것이 확실한 경우 |
- References
Onder G, Marengoni A.: Polypharmacy. JAMA. 2017;318(17):1728. doi:10.1001/jama.2017.15764.
Chang, T.I., Park, H., Kim, D.W. et al: Polypharmacy, hospitalization, and mortality risk: a nationwide cohort study. Sci Rep 10, 18964 (2020). https://doi.org/10.1038/s41598-020-75888-8
All Wales Medicines Strategy Group. Polypharmacy in older people: A guide for healthcare professionals. March 2023.
Copyright © MediGloPark's All Rights Reserved.
노인인구와 다제약물의 위험성
 ▷ 다제약물(polypharmacy)은 동시에 여러 가지의 많은 약물을 복용할 때 발생하는데, 매일 5개 이상의 약물을 동시에 복용하는 경우를 말한다.
이러한 상황은 당뇨, 고혈압, 심부전, 골다공증, 파킨슨병, 그리고 우울증을 포함한 정신질환 등 많은 만성질환과 장기간 약물치료가 필요한 통증이나 불면증 증상을 가진 환자들에서 빈번하게 나타난다.
▷ 다제약물(polypharmacy)은 동시에 여러 가지의 많은 약물을 복용할 때 발생하는데, 매일 5개 이상의 약물을 동시에 복용하는 경우를 말한다.
이러한 상황은 당뇨, 고혈압, 심부전, 골다공증, 파킨슨병, 그리고 우울증을 포함한 정신질환 등 많은 만성질환과 장기간 약물치료가 필요한 통증이나 불면증 증상을 가진 환자들에서 빈번하게 나타난다.다제약물은 특히 노령인구에서 주된 건강이슈로 대두되고 있다.
최소한 1개 이상의 처방약을 지속적으로 복용하는 300만명 이상의 65세 이상 노인환자들을 대상으로 다제약물과 입원 및 사망률간의 관계를 조사한 연구(Tae Ik Chang 등, 2020년)에 따르면, 평균 5년간 추적 조사 시 참여자 46.6%에서 5개 이상의 약물을 복용하는 다제약물을 경험하는 것으로 나타났으며 67.4%의 입원율, 그리고 15.3%의 사망률을 나타냈다. 하루 처방약의 수가 증가할수록 입원과 사망의 위험성도 증가하는 것으로 나타났다.
노인은 근육량과 체내 수분량이 비교적 저하되어 있는 반면에 체지방량은 증가하므로, 친유성 약물들의 분포용적은 감소하고 지용성 약물들의 분포용적은 증가하는 경향이 있다. 또한 BBB(blood-brain barrier) 기능의 저하로 약물의 CNS 도달이 용이해지는 상황에 주의하여야 한다. 체내 흡수된 약물의 해독과 소실률도 노인에서는 감소하며, 간혈류, 간의 약물 청소율도 감소한다. 특히 노인에서 나타나는 신장 혈류 감소는 가장 심각한 약력학적 변화로서 약물의 신배설 저하를 야기하므로 다제약물에 대한 세심한 주의가 필요하다.
약은 올바르게 보관하고 정확하게 복용을 하여야 하는데 여러 가지의 다른 약물들을 동시에 복용하게 되는 상황에서는 실수가 빈번하게 있을 수 있다. 또한 DUR 시스템 등 처방 검토 도구의 사용에도 불구하고 의사는 환자가 어떠한 약을 복용중인지 모르고 처방을 하는 경우도 발생하는데, 동일한 효능군의 약을 두 번 처방하거나 다른 약물들의 대사나 흡수에 영향을 주는 약물상호작용이 발생하는 약을 처방하게 되는 경우도 발생할 수 있다.
하나의 질환이나 증상을 치료할 목적으로 쓰이는 약물이 다른 질환이나 증상에 부정적인 영향을 주는 약물-질병 상호작용이 발생할 수도 있는데, 한 예로서 비스테로이드성 소염진통제가 혈압상승을 유발하고 신기능을 악화시키므로 고혈압이나 신기능에 문제가 있는 환자에게 사용하는 것이 부적절한 경우이다. 환자가 많은 약물을 복용하는 경우에는 다음과 같은 사항에 주의하여야 한다.
| 다제약물과 환자 주의사항 | |
|---|---|
| 1 | 복용 중인 약들에 대한 최신의 정확한 목록을 작성하여야 한다. 이 목록에는 처방약 뿐만 아니라 일반의약품, 생약제제, 그리고 보조제 등을 포함하여야 한다. 이 목록은 항상 지니고 있어야 하며 처방약의 변동이 있으면 바로 갱신하도록 한다 |
| 2 | 작성한 목록을 바탕으로 복용중인 약과 보조제 등을 의사와 약사에게 반드시 알려야 한다. |
| 3 | 환자는 본인이 처방을 받은 약들을 왜 복용해야 하는지 이해하여야 한다. 조심해야 할 부작용에 대하여 의사 및 약사와 상의하고 어떠한 증상이 복용하게 될 약물의 부작용인지 의사 및 약사에게 문의하여야 한다. |
| 4 | 환자는 약물치료에 대하여 주기적으로 의사 및 약사와 상의하여야 한다. 환자가 증상의 소실 등 여러 이유로 복용할 필요가 없게 된 것으로 판단되는 약을 제외할 수 있는지 의사와 상의하여야 한다. 환자가 기억에 장애가 있으면 가족이나 돌보미 등의 도움을 받아야 한다. |
| 5 | 처방약의 복용을 갑자기 중단하지 않아야 한다. 환자가 약물을 올바로 복용하는데 문제가 있으면 약물치료를 단순화할 수 있거나 복용 횟수를 줄일 수 있는 약물로 변경할 수 있는지 의사와 상의하여야 한다. 필요하면 주간 또는 일간 알약 박스와 같은 보조물이나 도구 등을 사용하도록 한다. |
만성질환 환자가 유의하여야 할 약제는 다음과 같다.
| 만성질환 환자 유의약제 |
|---|
| NSAIDs 2성분 이상 사용 |
| 항응고제 |
| 고혈압 약제 3성분 이상 사용 |
| Dogoxin |
| 소화기관용 약제 3성분 이상 사용 |
| Corticosteroids 지속적 사용 |
| 마약성 진통제(비암환자) |
| 경구혈당강하제 3성분 이상 사용 |
| 인슐린 펜형 |
| 삼환계 항우울제 |
| 중추신경계 억제 약물 3성분 이상 사용 |
| 항콜린성 약제 2성분 이상 사용 |
여러 약물을 동시에 복용하는 경우 발생하는 약물-약물 상호작용(Drug-Drug Interactions, DDIs)은 약동학적(pharmacokinetic), 약력학적(pharmacodynamic) 상호작용과 약제학적 배합금기(pharmaceutical incompatibility) 및 이들 기전들의 조합 또는 알려지지 않은 기전 등에 기인하며 신기능을 포함한 신체 기능의 저하를 나타내는 노인에서는 그 위험성이 더욱 증가한다. 일례로 노인환자에서 통증 경감 목적으로 사용하는 NSAIDs와 관련된 DDI의 경우 단백결합력이 높은 NSAID가 혈장내에서 다른 단백결합약물과 경쟁적으로 결합하여 약효에 영향을 줄 수 있다.
| DDIs | 특징 |
|---|---|
| 약동학적(pharmacokinetic) DDIs | 약물의 흡수(absorption), 분포 용적(volume of distribution), 대사(metabolism), 배설(excretion)의 변화 등 |
| 약력학적(pharmacodynamic) DDIs | 약물의 혈장 수준 불변에도 발생하는 상가적(additive), 상승적(synergistic), 또는 길항적(antagonistic) 영향 등 |
| 약제학적 배합금기(pharmaceutical incompatibility) | 산과 염기의 조합 등 |
- References
Onder G, Marengoni A.: Polypharmacy. JAMA. 2017;318(17):1728. doi:10.1001/jama.2017.15764.
Chang, T.I., Park, H., Kim, D.W. et al: Polypharmacy, hospitalization, and mortality risk: a nationwide cohort study. Sci Rep 10, 18964 (2020). https://doi.org/10.1038/s41598-020-75888-8.
Moore N, Pollack C, Butkerait P. Adverse drug reactions and drug-drug interactions with over-the-counter NSAIDs. Ther Clin Risk Manag. 2015 Jul 15;11:1061-75. doi: 10.2147/TCRM.S79135. PMID: 26203254; PMCID: PMC4508078.
Esumi S, Ushio S, Zamami Y. Polypharmacy in Older Adults with Alzheimer's Disease. Medicina (Kaunas). 2022 Oct 13;58(10):1445. doi: 10.3390/medicina58101445. PMID: 36295605; PMCID: PMC9608980.
대한약사회 사이버연수원 학술자료(2020).
Copyright © MediGloPark's All Rights Reserved.
신경병증성 통증(신경통)과 영양
 ▷ 신경병증성 통증은 만성통증인 경우가 많고, 당뇨병성 말초신경질환, 대상포진 후 신경통, 뇌졸중 후 통증, 환상지통(幻想肢痛, phantom limb pain), 경추성 신경통,
후두신경통 등 다양한 질병에서 나타난다는 특징이 있으며, 불안 및 우울증과도 관련이 있는 것으로 알려져 있다.
▷ 신경병증성 통증은 만성통증인 경우가 많고, 당뇨병성 말초신경질환, 대상포진 후 신경통, 뇌졸중 후 통증, 환상지통(幻想肢痛, phantom limb pain), 경추성 신경통,
후두신경통 등 다양한 질병에서 나타난다는 특징이 있으며, 불안 및 우울증과도 관련이 있는 것으로 알려져 있다.체성감각 신경계(somatosenory system)질환으로 발생하는 신경병증성 통증의 치료제로는 일반 진통제, 삼환계 항우울제, 세로토닌-노르에피네프린 재흡수 억제제, 항전간제 등이 많이 쓰이고 있으나, 부작용 등 여러 이유로 치료약 이외에 통증 감소에 도움이 되는 비약물치료를 찾는 경우가 증가하고 있다. 비약물치료는 운동요법, 통합인지행동치료, 그리고 영양보조제 등이 대표적이다
신경병증성 통증 개선에 도움이 되는 보조제로는 표1과 같이 아연, 마그네슘, 비타민 D, 비타민 B군, 커큐민, 세인트존스워트 등이 있다.
외과적 또는 침습적 비약물치료로는 마사지요법, 통증유발점주사(Trigger Point Injection, TPI), 침술요법, 경피적 전기신경자극(Transcutaneous Electrical Nerve Stimulation, TENS), 운동피질자극(Motor Cortex Stimulation, MCS) 등이 있다.
질병 치료나 예방에 도움을 주는 식품, 또는 식품에서 추출한 특정 성분 등을 의미하는 뉴트라수티컬(Nutraceutical, Nutrition + Pharmaceutical)과 여러 비약물학적 보조제들은 기존의 약물학적 치료와 함께 만성 신경병증성 통증 치료에서 서로 상승효과를 나타낼 것으로 기대가 되고 있다.
표1. 만성 신경병증성 통증 보조제
| 보조제 | 독성 발현량 및 주의사항 | 보조제 함량 | 비고 |
|---|---|---|---|
| 아연 | 100mg/일 | 30~50mg | 항염작용(metallothionein), 신경성장인자(Nerve Growth Factor, NGF) 감소작용(NGF는 신경병증성 통증에서 나타나는 말초감각의 과민증에 대한 주된 유발인자임). |
| 마그네슘 | 5000mg/일 | 250~500mg | 시냅스후 막에 존재하여 학습과 기억 등 뇌발달과 기능에 관여하며, 통증변환의 주 수용체이기도 한 NMDA 수용체에 결합. |
| 비타민 D | 10000IU/일 | 400~5000IU | 염증성 사이토카인의 조절에 관여한다는 학설이 있으나 추가적 연구가 필요함. |
| 비타민 B1, B6 | 25, 50, 100mg/일 | 고함량(25, 50mg/일)의 비타민 B1, B6을 투여 시 저함량(1mg/일)보다 당뇨병성 신경병증성 통증에 더욱 효과적임. | |
| 비타민 B9 | 400~1000mcg DFE | 비타민 B1, B6, B9, B12 등 B 복합체가 신경병증성 통증 치료에 효과적임. B1, B6, B12 조합은 당뇨병 쥐모델에서 접촉성 이질통증(異質痛症, Tactile Allodynia)을 개선함. | |
| 비타민 B12 | 500~1000mg | 신경병증성 통증치료에서 비타민 B의 작용기전은 명확하지 않음. 단, 비타민 B12는 신경복구와 수초발생(myelination)에 관여하여 신경병증성 통증을 개선함. | |
| 커큐민(curmin) | 8000g/1일 | 500~1000mg | 미토겐활성화단백질 키나아제(Mitogen-Activated Protein kinase)를 저해하고 그 신호를 억제하여 치료효과를 나타냄. 항염작용. 항산화작용. |
| 세인트존스워트(St. John's Wort, SJW) | 약물상호작용 주의 | 100~900mg | SJW는 다른 우울제와 유사하게 모노아민 산화효소의 저해와 시냅스에서 아민의 재흡수를 저해하여 우울증과 신경병증성 통증을 개선함. 신경병증성 통증에 관여하는 단백질 키나아제 C 경로를 저해하여 통증을 경감시킨다는 학설도 있음. Cytochrome P450 및 P-gycoprotein의 기질이 되는 약물과 심각한 상호작용이 있으므로 주의가 필요함. |
SJW와 약물과의 상호작용은 다양하지만 특히 주목되는 것은 cyclosporin 혈중농도의 감소, 세로토닌 재흡수 억제제와 같이 투여 시 나타나는 세로토닌증후군과 무기력증, 경구피임제와 같이 사용 시 피임실패로 인한 임신, 항레트로바이러스제(예, indinavir, nevirapine)와 항암제(예, irinotecan, imatinib)의 혈장농도 감소 등이다.
한편, 만성 신경병증성 통증의 치료에 쓰이는 대표적인 항우울제와 항전간제는 표 2와 같다.
Venlafaxine, Duloxetine, Bupropion, Paroxetine, Citalopram 등은 삼환계 항우울제에 비해 부작용 위험성이 비교적 낮으며, Fluoxetine은 신경병증성 통증에 효과가 인정되지 않는 것으로 알려져 있다.
표2. 신경병증성 통증(신경통) 치료제
| 분류 | 성분 | 효과 | 비고 |
|---|---|---|---|
| Tertiary amine tricyclic antidepressants | Amitriptyline, Doxepin, Imipramine | effective | |
| Secondary amine tricyclic antidepressants | Desipramine, Nortriptyline | effective | |
| Serotonin and noradrenaline reuptake inhibitors(SNRIs) | Venlafaxine, Duloxetine | effective | |
| Norepinephrine and dopamine reuptake inhibitor | Bupropion | effective | |
| Selective Serotonin Reuptake Inhibitors(SSRIs) | Paroxetine, Citalopram | modest | |
| Anticonvulsants(α2δ Subunit Ligand) | Gabapentin | effective | 위산 조절제에 의해 효과가 감소함. 부작용은 심하지 않으편이나 졸림, 어지럼증 등의 부작용으로 서서히 증량함. 금단증상 방지를 위해 서서히 감량함. 흥분성 신경전달물질의 방출 억제작용 외에 세로토닌의 혈중 수준 증가도 보고됨. |
| Anticonvulsants(α2δ Subunit Ligand) | Pregabalin | effective | 졸림, 어지럼증 등의 부작용으로 서서히 증량함. 금단증상 방지를 위해 서서히 감량함. |
- References
Khaled M. Abdelrahman and Kevin V. Hackshaw: Nutritional Supplements for the Treatment of Neuropathic Pain. Biomedicines 2021, 9, 674.
Randy A. Sansone and Lori A. Sansone: Pain, Pain, Go Away. Antidepressants and Pain Management. Psychiatry (Edgmont). 2008 Dec; 5(12): 16–19.
Francesca Borrelli and Angelo A. Izzo: Herb–Drug Interactions with St John’s Wort (Hypericum perforatum): an Update on Clinical Observations. The AAPS Journal, Vol. 11, No. 4, December 2009.
Copyright © MediGloPark's All Rights Reserved.
우울증과 영양
 ▷ 단백질, 비타민 B군, 비타민 D, 마그네슘, 아연, 셀레늄, 철, 칼슘, 오메가3 지방산 등이 결핍되면 뇌와 신경계에 심각한 충격을 주어 우울증상의 발현에 영향을 미칠 수 있다.
반면에, 구리와 철과 같은 영양소가 과잉이 되면 정신건강에 부정적 영향을 줄 수 있다.
▷ 단백질, 비타민 B군, 비타민 D, 마그네슘, 아연, 셀레늄, 철, 칼슘, 오메가3 지방산 등이 결핍되면 뇌와 신경계에 심각한 충격을 주어 우울증상의 발현에 영향을 미칠 수 있다.
반면에, 구리와 철과 같은 영양소가 과잉이 되면 정신건강에 부정적 영향을 줄 수 있다.우울증은 가장 일반적인 정신질환 중 하나로서 그 발병률이 꾸준히 증가하고 있다.
2023년 Magdalena Zielińska 등은 식품 중 영양소의 역할과 중요성, 그리고 우울증의 위험성 증가와 관련된 영양소 결핍의 영향을 명확히 하고자 2018-2023년의 논문들을 조사한 결과를 발표하였다. 이에 따르면 단백질, 비타민 B군, 비타민 D, 마그네슘, 아연, 셀레늄, 철, 칼슘, 오메가3 지방산 등이 결핍되면 뇌와 신경계에 충격을 주어 우울증상의 발현에 영향을 미칠 수 있는 것으로 나타났다. 물론, 이러한 식품 중의 영양소 자체가 우울증의 위험성이나 치료에 도움이 되는 유일한 요소가 아니므로, 신체활동, 수면, 스트레스 관리, 그리고 사회적 지지 등 많은 다양한 면들이 정신건강 유지에 매우 중요한 역할을 한다는 것을 주지하여야 한다.
표1. 우울증과 영양소
| 분류 | 성분 | 기능 | 비고 |
|---|---|---|---|
| 대량 영양소 | 단백질 | 뇌 신경전달물질의 아미노산 공급원 | 트립토판->세로토닌, 티로신 또는 페닐알라닌->노르에피네프린 |
| 탄수화물 | 뇌의 구성성분, 에너지원 | 낮은 혈당지수(glycemic index, GI)를 갖는 식품이 우울증의 위험을 효과적으로 낮춤. | |
| 다불포화지방산 | 오메가3(DHA, EPA), 오메가6(아라키돈산) | 항염, 신경 내분비과정 조절, 신경전달물질을 활성화 | 오메가3 섭취가 부족하면 우울증 위험성이 증가함 |
| 비타민 | B1, B6, B9, B12 | 모노아민 산화효소 생성, DNA 합성 및 메틸화, 인지질의 유지 등에 관여 | 비타민 B1, B6, B9, B12와 같은 B군의 결핍은 우울증과 관련이 있으며 신경기능에 필수적임. |
| 비타민 D | 세로토닌을 적정 수준으로 유지하고 도파민과 노르에피네프린 수준을 조절 | 비타민 D가 결핍되면 우울증의 위험성이 8-14% 증가함. | |
| 미네랄 | 마그네슘 | 시상하부-뇌하수체-부신(Hypothalamic-Pituitary-Adrenal, HPA) 축의 조절에 영향 | NMDA(N-methyl-d-aspartate) 수용체의 길항제로서 마그네슘 결핍은 NMDA 수용체의 과잉활성을 초래함. |
| 아연 | 항염 및 항산화작용. 코티솔 등 호르몬 조절, 세포면역반응, 신경발생, 신경가소성, 해마와 피질에서 뇌유래 신경영양인자(BDNF)의 발현 등에 영향 등. | 아연은 마그네슘과 같이 NMDA 수용체 길항제임. | |
| 셀레늄 | (신경)세포의 산화적 손상에 보호 작용(항산화) | ||
| 구리 | 신경발생, 시냅스발생, 신경전달, 인지, 학습 및 기억 등 여러 과정과 NMDA 기능에 관여 | 구리의 결핍과 과잉 모두 뇌기능에 부정적 영향이 있음. | |
| 철분 | 노르에피네프린은 뇌 내 철 대사와 관련됨. 뇌유래 영양인자(BDNF) 수준이 철에 의해 조절됨. | 체내 철 수준이 높은 경우 오히려 우울증상이 더 심해지는 것으로 나타난 연구결과도 있어 적절한 수준의 철분 유지가 중요함. | |
| 칼슘 | 시상하부-뇌하수체-부신(HPA) 시스템의 조절에 관여 | 세포외부의 칼슘이온 농도의 변화는 감정조절과 관계됨. |
우울증은 여러 원인들로 발병하는데, 염증성 반응과 사이토카인 수준의 증가, 시상하부-뇌하수체-부신 축(hypothalamic–pituitary–adrenal axis, HPA axis)의 조절장애, 신경전달물질의 불균형, 교감 및 부교감신경계의 기능장애, 내피기능장애(endothelial dysfunction) 등 다양한 원인들이 있다. 신경생물학적 연구들에서 우울증은 신경망의 연결이나 기능의 손상뿐만 아니라, 대뇌피질 및 대뇌변연계 신경의 위축 등과 관련이 있는 것으로 밝혀졌다. 이들 변화들은 구조적, 기능적, 신경화학적 결손의 결과로서, 그중에서도 γ-aminobutyric acid (GABA)와 글루타메이트(glutamate)와 관련된 문제들이 특히 주목되고 있다. 우울증의 병태생리학적 관점에서 가장 일반적인 것 중의 하나는 모노아민 신경전달물질과 관련이 있다는 가설로서, 세로토닌, 도파민, 그리고 노르에피네프린의 수준이 우울증환자에서 낮게 나타나는 것이다. 이러한 신경전달물질들의 합성과 방출에는 여러 가지 요소들이 필요한데, 그 중에는 식품 중의 영양소도 포함된다. 대량영양소, 미네랄, 비타민 섭취의 변화와 같은 식이적인 변화가 체내에서 염증과정을 조절하고 분자 시스템과 세포 과정에 영향을 주어 인지기능에 영향을 줄 수 있다. 결국, 뇌기능에 필수적인 식품 중 영양소의 공급을 최적화하는 것은 우울증 질환에서 그 중요성이 더욱 강조되고 있다.
▷ 대량영양소(단백질, 섬유소 등)와 물
단백질은 뇌 내 신경전달물질의 전구물질인 아미노산의 공급원으로서 중요하다. 이 신경전달물질들은 방향족 아미노산으로부터 합성되는데, 세로토닌이 트립토판으로부터, 노르에피네프린이 티로신 또는 그 전구체인 페닐알라닌으로부터 합성된다. 따라서 이들 아미노산들의 결핍은 뇌 내 신경전달물질의 감소를 초래할 수 있다.
포화지방산이나 트랜스지방은 우울증의 위험성을 증가시키며, 반면에 불포화지방산은 우울증의 위험성을 낮출 수 있다.
또한, 뇌는 구조적 기능적 구성 성분으로서 뿐만 아니라 주된 에너지원으로 탄수화물을 필요로 한다. 탄수화물은 세로토닌, 도파민, 노르에피네프린과 같은 신경전달물질 수준에 영향을 주어 기분과 뇌기능에 영향을 미친다. 더욱이 글루타메이트, 아세틸콜린, 그리고 가바(GABA)와 같은 신경전달물질의 유효성은 외부의 포도당 공급에 의해 조절되며, 낮은 혈당지수(glycemic index, GI)를 갖는 식품이 우울증의 위험을 효과적으로 낮출 수 있다. 고혈당지수의 식품은 우울증 위험성에 심각한 영향을 주는 것으로 조사되었다.
섬유소도 우울증 예방에 의미 있는 영향을 주는데, 5그람의 식이섬유 섭취량 증가로 우울증의 위험성을 5% 낮춘다는 조사결과가 있으며 곡류 및 과일의 섬유소, 불용성 섬유소 등이 근소하지만 우울증 감소와 관련이 있는 것으로 알려져 있다.
뇌 무게의 75%는 물로 이루어져 있으며 탈수는 신경계 기능에 영향을 미칠 수 있는데, 1% 이상의 탈수에서 분노, 정신착란, 우울 및 피로의 위험성이 증가하는 것으로 알려져 있다.
▷ 다불포화지방산 - 오메가3
다불포화지방산(polyunsaturated fatty acids)은 인체 내에서 자체적으로 합성이 되지 않으므로 식품이나 보충제를 통해 공급하여야 한다. 다불포화지방산은 신경 구조와 기능에 다양한 효과를 나타내며, 항염효과가 있고, 신경내분비과정을 조절하며, 주된 신경전달물질을 활성화하여 우울증 예방에 기여한다. 성숙한 뇌 건조중량의 20%는 다불포화지방산으로서 주로 DHA(docosahexaenoic acid) 및 EPA(eicosapentaenoic acid)를 주로 포함한 오메가3와 아라키돈산을 주로 포함하는 오메가6 지방산으로 구성된다. DHA는 신경막의 적절한 기능 유지에 필수적인데, 오메가3 다불포화지방산의 섭취가 적으면 자살시도의 위험성과 우울증 위험성이 증대되는 것으로 알려져 있다.
▷ 비타민 B군 - 비타민 B1, B6, B9, B12
비타민 B군은 인체에서 하는 많은 기능 외에 모노아민 산화효소(monoamine oxidase) 생성, DNA 합성 및 메틸화, 그리고 인지질의 유지 등에 관여하여 신경계의 기능을 정상적으로 유지하는데 필수적이다. 특히 비타민 B1, B6, B9, B12와 같은 B군의 결핍은 우울증과 관련이 있는 것으로 알려져 있으며 신경기능에 필수적이다. 또한, 비타민 B9와 B12가 결핍되면 항우울제에 대한 반응이 약화되며, 비타민 B9와 B12의 섭취가 뇌구조에 영향을 주는 것으로 알려져 있다. 특히 우울증을 경험한 채식주의자는 비타민 B6, B9, B12를 보충하여 적절한 뇌 건강을 유지하는데 도움이 되도록 하여야 한다.
▷ 비타민 D
비타민 D는 햇빛에 노출하거나 음식물 또는 보충제 등을 통해 얻을 수 있는데, 비타민 D가 결핍되면 우울증의 위험성이 8-14% 증가하는 것으로 알려져 있다. 이러한 결과에 대한 가설 중 하나는 비타민 D 수용체가 대뇌피질과 대뇌변연계의 여러 부분에 존재하고 뇌의 이러한 여러 영역이 우울증과 병태생리학적으로 관계된다는 것이다. 비타민 D 수용체가 변연계를 구성하는 요소 중 하나로서 기억, 공간개념 및 감정적인 행동의 조절, 학습, 새로운 것의 인식 등에 관여하는 해마(hippocampus)에서도 발견되어 기억과 감정기능에 중요한 것으로 보인다. 더욱이 비타민 D는 뇌유래 신경영양인자(腦由來神經榮養因子, Brain-Derived Neurotrophic Factor, BDNF), 뉴로트로핀(Neurotrophin, NT)-3과 같은 신경성장 물질과 신경 성장인자(Nerve Growth Factor, NGF)의 생성을 강력하게 조절한다. 또한, 비타민 D가 우울증에서 병태생리학적으로 중요한 면역염증성 과정을 조절하는데 있어서 중요한 조정역할을 하며, 혈청 비타민 D 수준이 우울증 환자에서 대조군에 비해 더 낮게 나타나는 것으로 알려져 있다. 다른 가설은 비타민 D가 결핍되어 있는 사람들의 신경세포에서 더 높은 수준의 반응성 산소들과 칼슘이온이 발견된다는 것이다. 그리고 비타민 D는 뇌에서 세로토닌을 적정 수준으로 유지하고 도파민과 노르에피네프린 수준을 조절하여 우울증 예방에 효과적이다.
▷ 미네랄
마그네슘, 아연, 철, 구리, 셀레늄과 같은 몇 가지 미네랄들이 항산화작용 뿐만 아니라 세포기능과 신경조절작용의 조정에 중요한 역할을 하는 것으로 알려져 있다.
마그네슘 결핍은 중추신경계 기능에 변화를 야기할 수 있는데, 특히 대뇌변연계와 대뇌피질에서 글루탐산성 전달 (glutamatergic transmission)에 영향을 미치게 된다. 뇌의 이들 영역은 우울증 원인의 병태생리학적 관점에서 매우 중요하다.
- 마그네슘
마그네슘 결핍은 코르티코트로핀 분비 호르몬(Corticotropin-Releasing Hormone, CRH)의 분비에 영향을 미쳐 부신피질자극호르몬(Adrenocorticotrophic Hormone, ACTH) 수준의 증가를 초래하게 된다. 이 기전은 시상하부-뇌하수체-부신(Hypothalamic-Pituitary-Adrenal, HPA) 축의 조절에 영향을 미쳐 우울증에 관련되는 것으로 보인다. 마그네슘은 시냅스후 막(Postsynaptic membrane)에 존재하는 이온성 글루탐산 수용체(Ionotropic glutamate receptor)의 일종인 NMDA(N-methyl-d-aspartate) 수용체의 길항제로서 마그네슘 결핍은 NMDA 수용체의 과잉활성을 초래할 수 있다. NMDA 수용체는 글루탐산과 결합 시에 나트륨, 칼슘은 신경세포 안으로 들어오고, 칼륨은 신경세포 밖으로 나가는 이온통로로 기능하는데, 과도하게 활성화가 되면 칼슘이온의 흐름이 증가하여 신경독성이 초래된다.
그럼에도 마그네슘의 섭취와 혈청 마그네슘 수준, 그리고 우울증의 위험성 간의 관계는 좀 더 많은 연구와 조사가 필요한 것으로 보인다.
- 아연
뇌의 아연 수준 변화가 우울증으로 발전할 수 있고 아연을 보충하면 그 상황을 고치는데 도움이 될 수 있다고 보고되어 있다. 또한 아연은 항우울제의 효과를 보조할 수 있고 몇몇 환자들에서 우울증상을 개선하는 것으로 알려져 있다. 아연의 항우울 효과는 아연의 항염 및 항산화작용에 의한 것일 수 있으며, 더욱이 아연은 NMDA 수용체 길항제로서 작용하기도 한다. 그리고 아연은 코티솔(cortisol) 수준을 포함하는 호르몬 조절, 세포면역반응(cellular immune response), 신경발생(neurogenesis), 신경가소성(neuronal plasticity), 해마와 피질에서 뇌유래 신경영양인자(BDNF)의 발현 등에 영향을 주며, 아연 이온은 시냅스 전달을 조절하거나 신경전달물질로서 작용한다. 한편, 아연 수송체(zinc transporters)와 아연-감지 GPR39 수용체가 우울증과 관련한 병인 및 치료학적 개입에서 중요한 것으로 강조되고 있다. 여러 연구결과로서 아연은 우울증의 위험성을 낮추고 증상을 개선하는데 매우 유익한 것으로 알려져 있다.
- 셀레늄
셀레늄은 우울증에 고려되는 모든 식이인자들 중 가장 관련이 많은 것 중의 하나이다. 셀레늄은 셀레늄함유단백질의 적절한 기능에 요구되는 필수미량원소로서 뇌와 신경계에서 항산화 작용에 필요하다. 또한 셀레늄은 세포의 산화적 손상에 보호 작용을 하여 염증이나 신경질환과 같은 질병 발생을 억제하는데 도움이 된다. 셀레늄의 뇌기능에서 신경조절 역할과 관련하여 셀레늄과 우울증 간의 관련성에 대한 많은 연구가 이루어지고 있으나 몇몇 연구에서는 상반된 결과가 나타나기도 한다.
- 구리
혈중 구리 수준이 높은 환자들에서 우울증상의 발현이 상승하는 것으로 알려져 있다. 인체 내 구리의 불균형이 우울증의 한 원인일 수 있다고 추측될 수 있지만, 구리가 신경계의 발달 및 기능에서 중요한 역할을 하는 여러 과정들이 있다. 즉, 신경발생, 시냅스발생, 신경전달, 인지, 학습 및 기억 등 여러 과정과 NMDA(N-methyl-d-aspartate) 기능에 관여하는 것으로 알려져 있다. 구리는 뇌유래 신경영양인자(BDNF)와 신경 성장인자(Nerve Growth Factor, NGF)의 활성을 보조하는데, 이 두 신경영양인자들은 신경 가소성과 신경망에 영향을 줄 수 있다. 우울증과 모노아민의 관계에서 구리이온은 dopamine β-hydroxylase(DBH)와 상호작용을 하므로 도파민의 노르에피네프린으로의 전환은 구리 의존적이다. 구리의 결핍과 과잉 모두 뇌기능에 부정적 영향을 미칠 수 있으며, 성상교세포가 구리원소의 항상성과 관련하여 중요한 조절역할을 하는 것으로 알려져 있다.
- 철분
정신질환에 미치는 철분의 영향에 대한 많은 연구들이 진행되고 있다. 노르에피네프린은 뇌 내 철 대사와 관련이 있는 것으로 알려져 있는데, 이는 전전두엽(前前頭葉) 뉴런(prefrontal neurons)의 신경가소성과 기능에 영향을 주며 해마에도 영향을 미치는 것으로 알려져 있다. 또한, 뇌유래 영양인자(BDNF) 수준이 철에 의해 조절되는데, 이는 신경전달물질의 정상적인 합성에 필요하며 신경에 존재하는 방향족 수산화효소(aromatic hydroxylase)에도 필요하다. 이러한 이유로 철의 신경생체이용율과 뇌가 혈액으로부터 철분을 얻는 획득능력은 뇌유래 영양인자(BDNF)와 우울증을 포함한 감정과정에 관여하는 신경전달물질들의 적절한 수준 유지를 위해 중요하다. 글루탐산성 시스템(glutamatergic system)의 기능부전이 우울증 발현과 관계가 있다는 학설에 대해 많은 연구가 이루어지고 있다. 철 결핍은 글루탐산성 시스템 변화에 영향을 주어 감정 장애(mood disorder)를 야기할 수 있다. 철은 신경전달물질인 글루타메이트를 생성하고 배출하는 대사반응의 효소 보조인자로서 중요한 역할을 한다. 또한, 빈혈이나 철 결핍이 여성의 산후 우울증의 한 원인이 되는 것으로 알려져 있다. 한편, 젊은 성인 남성에서는 체내 철 수준이 높은 경우 오히려 우울증상이 더 심해지는 것으로 나타난 연구도 있다. 따라서 적절한 수준의 철분 유지가 중요한 것으로 보인다.
- 칼슘
우울증의 병태생리학적 관점에서 칼슘의 역할은 여러 기전에 포함되는 것으로서 설명될 수 있다. 그중 하나는 시상하부-뇌하수체-부신(HPA) 시스템의 조절에 관여하는 것이다. 더욱이 세포외부의 칼슘 유입은 많은 신경학적 과정에서 중요한 요소이다. 세포외부의 칼슘이온 농도의 변화는 감정조절과 관계가 있는데, 이는 원형질막의 안정화에 대한 칼슘의 직접적인 효과에 의한 것일 수 있으며, NMDA 또한 신경가소성에 영향을 미치는 것으로 알려져 있다.
이러한 우울증상과 신경계에 대해 지금까지 알려진 많은 연구 결과에도 불구하고 인과관계의 확실한 결론을 위해 좀 더 많은 연구가 필요하며, 횡단연구(cross-sectional study) 뿐만 아니라 종단(longitudinal) 임상대조연구 등을 통하여 심층적으로 확인할 필요가 있다.
- References
Magdalena Zielińska et al: Dietary Nutrient Deficiencies and Risk of Depression (Review Article 2018–2023). Nutrients. 2023 Jun; 15(11): 2433.
Zhengyang Quan et al: Appropriate Macronutrients or Mineral Elements Are Beneficial to Improve Depression and Reduce the Risk of Depression. Int. J. Mol. Sci. 2023, 24, 7098.
Kuan-Pin Su et al: Omega-3 Polyunsaturated Fatty Acids in Prevention of Mood and Anxiety Disorders. Clinical Psychopharmacology and Neuroscience. 2015;13(2):129-137.
Copyright © MediGloPark's All Rights Reserved.
비타민 D 보충과 치매발생율 감소
 비타민 D 보충과 치매발생의 위험성에 대해서는 많은 관련 메커니즘들이 보고되어 있다.
비타민 D 보충과 치매발생의 위험성에 대해서는 많은 관련 메커니즘들이 보고되어 있다.비타민 D 수용체는 뇌 전반에 걸쳐서 나타나는데, 특히 해마(海馬, hippocampus)와 치상회(齒狀回, dentate gyrus)와 같은 기억과 관련된 뇌 영역도 포함한다. 유사하게 비타민 D의 활성형을 합성하는 효소인 1α-hydroxylase가 여러 뇌 영역에서 생성된다. 활성형 비타민 D인 1,25dihydroxy-vitamin D3는 신경성장인자인 뉴로트로핀-3(neurotrophin-3) 및 교세포 유래 신경성장인자(glial-derived neurotrophic factor)와 같은 뉴로트로핀의 발현과 신경세포들의 생존, 성장 및 기능 등을 조절한다. 또한, 실험실적 연구에서 비타민 D는 대식세포를 자극하여 알츠하이머병의 특징인 아밀로이드 플라크(amyloid plaques)의 제거를 촉진한다. 또한 비타민 D는 아밀로이드에 의한 세포독성과 1차 피질 뉴런(primary cortical neurons)의 아프토시스(apoptosis)를 감소시킨다. 또한, 노년 래트를 대상으로 한 실험에서는 비타민 D를 보충 시 노화와 관계된 학습과 기억의 퇴행이 개선되는 것으로 나타났다. 더욱이 비타민 D 결핍은 뇌혈관질환과도 관련된 것으로 알려져 있는데, 25-hydroxyvitamin D가 결핍되면 허혈성 뇌졸중(ischemic stroke) 발생이 증가한다는 메타분석 결과도 있다. 318명의 노인들을 대상으로 한 횡단적 단면연구(橫斷的 斷面硏究, cross-sectional study)에서 25-hydroxyvitamin D 결핍에 의해 혈관성 치매와 관련된 대뇌백질 고강도신호(White Matter Hyperintensity, WMH)의 크기가 증가하는 것으로 나타났으며, 큰 혈관들의 경색도 증가하는 것으로 나타났다.
결국 비타민 D의 결핍은 신경퇴화 및 혈관과 관련된 메커니즘을 통해 치매와 알츠하이머병의 위험성을 증가시키는 것으로 볼 수 있다.
이와 관련하여 2014년 1658명을 대상으로 한 연구에서는 비타민 D 결핍이 전 원인(all-cause) 치매와 알츠하이머병의 증가와 관련이 있으며, 25-hydroxyvitamin D 충분그룹(≥50 nmol/L)에 비하여 심각한 결핍그룹(<25 nmol/L)과 결핍그룹(≥25nmol/L, <50 nmol/L)의 상대위험비(Hazard Ratio)는 각각 2.22(95%CI: 1.02-4.83)와 1.69(95%CI:1.06-2.69)로 조사되어 전 원인 치매와 알츠하이머병의 위험성이 50nmol/L 아래에서 현저하게 증가하는 것으로 나타났다.
한편, Maryam Ghahremani 등은 비타민 D 보충과 이에 따른 치매발생율의 변화에 대해 NACC(National Alzheimers's Coordinating Center) 데이터세트의 다양한 인종으로 구성된 12,388명의 참여자들을 대상으로 한 전향코호트연구(prospective cohort study) 결과를 2023년 발표하였다.
이 연구에서 비타민 D를 사용한 경우에 사용하지 않은 경우보다 치매발생율이 40% 낮게 나타났으며, 이러한 비타민 D의 효과가 남성보다 여성에서 더 큰 것으로 나타났다. 또한, 알츠하이머병의 유전적 위험인자인 apolipoprotein E ε4 비보유자에서 보유자에 비해 더 비타민 D의 효과가 큰 것으로 나타났다.
여성에서 효과가 더 크게 나타난 것은 에스트로겐과 활성형 비타민 D, 그리고 노인여성에서 감소하는 에스로겐 수준 등에서 그 원인을 찾아볼 수 있다. 에스트로겐은 비타민 D를 활성화하는 효소의 활성을 증가시키므로, 갱년기와 완경단계에서 에스트로겐 수준이 감소하여 비타민 D 결핍이 야기되는 가설을 생각해 볼 수 있다. 연구에 참여한 여성의 평균 연령은 71.2세로서 대부분의 여성이 완경된 상태로서 낮은 에스트로겐 수준으로 인해 활성형 비타민 D의 수준도 낮게 나타나는 것으로 추측할 수 있으며, 이에 따라 비타민 D 보충이 노인여성에서 더 큰 효과를 나타낸 것으로 보인다.
또한, 정상인지(normal cognition)와 경도인지장애(輕度認知障礙, mild cognitive impairment)의 두 경우를 조사하였을 때 비타민 D 보충이 두 경우 모두에서 치매발생율을 낮추는 것으로 나타났으나, 정상인지기능 단계에서 비타민 D 보충이 시작된 경우 치매발생 감소율이 56%로서 경도인지장애 단계의 33%에 비해 더 강력한 효과를 나타내는 것으로 조사되어 질병단계에서 조기개입의 중요성이 강조되고 있다.
이러한 종적연구(longitudinal study)를 통하여 비타민 D 사용이 10년 이상에 걸쳐 치매 없는 삶과 치매발생율 저하에 관계된 것으로 나타났으며 칼슘-비타민 D, 콜레칼시페롤(비타민 D3), 에르고칼시페롤(비타민 D2) 등 다양한 형태의 비타민 D에서 일치되는 결과가 나타났다.
이러한 결과와 고용량의 비타민 D 섭취가 인지기능을 더욱 개선할 수 있고 치매발생 위험의 감소에 기여하는 것으로 알려져 있음에도 불구하고, 혈중 비타민 D 수준, 사용기간, 약용량과 반응관계, 비타민 D 결핍의 결과 등에 대한 더 심층적인 연구가 이루어져야 할 것이다.
- References
Maryam Ghahremani et al: Vitamin D supplementation and incident dementia: Effects of sex, APOE, and baseline cognitive status. Alzheimer’'s & Dementia: Diagnosis, Assessment & DiseaseMonitoring 2023;15:e12404.
Thomas J. Littlejohns et al: Vitamin D and the risk of dementia and Alzheimer disease. Neurology 83(920-928) September 2, 2014.
Shelley J. Allen, Judy J. Watson and David Dawbarn: The Neurotrophins and Their Role in Alzheimer’s Disease. Current Neuropharmacology, 2011, 9, 559-573.
Copyright © MediGloPark's All Rights Reserved.
파킨슨병과 프로바이오틱스
 파킨슨병은 중년과 노년에서 빈발하는 신경퇴행성질환중 하나로서
(미생물-)장-뇌 축이 파킨슨병의 발생에서 주된 역할을 하는 것으로 알려져 있다.
파킨슨병은 중년과 노년에서 빈발하는 신경퇴행성질환중 하나로서
(미생물-)장-뇌 축이 파킨슨병의 발생에서 주된 역할을 하는 것으로 알려져 있다. 위장관 내 미생물의 변화는, 뇌세포 사이의 신경전달을 돕는 단백질로서 파킨슨병의 주요 발병원인 중 하나인, 알파시누클레인의 오접힘(잘못 접힘)과 비정상적 응집을 야기할 수 있다. 비정상적인 알파시누클레인은 생리학적 메커니즘으로 제거되지 않으며 미주신경을 통해 중추신경계로 이동된다. 비정상적 수준의 알파시누클레인은 흑질치밀부(substantia nigra pars compacta)에 응집되어 세포질에서 호산성 루이소체를 형성하고 도파민작용성 신경에서 미토콘드리아 기능부전을 일으킬 뿐만아니라 미세아교세포(微細阿膠細胞, microglia)에서 염증반응을 촉진하기도 한다.
이러한 병리학적 변화는 산화적 스트레스의 증가를 초래하여 파킨슨병의 특징인 신경세포의 세포자멸사(細胞自滅死, apoptosis)를 촉발시킨다. 이 산화적 스트레스의 증가로 알파시누클레인의 산화와 비정상적 응집이 강화되고 결국 양성 피드백(positive feedback) 루프를 형성하게 된다.
이러한 현상은 장내 미생물과도 밀접한 관련이 있는데, 위장관 미생물군의 변화에 의해서 장관내 알파시누클레인이 비정상적으로 축적되면 (미생물-)장-뇌 축을 통해 중추신경계로 전달되는 알파시누클레인의 양이 증가하여 파킨슨병 환자의 뇌내 도파민성 신경의 결손과 미세아교세포들의 염증반응이 증가하게 된다.
따라서 파킨슨병 치료에서 (미생물-)장-뇌 축의 관점상 프로바이오틱스와 프리바이오틱스를 이용한 장내미생물군의 세균불균형을 개선하는 것은 다른 치료법과 더불어 큰 의미를 갖는 것으로 알려져 있다.
- References
Qingchun Lei et al: Roles of α‑synuclein in gastrointestinal microbiome dysbiosis‑related Parkinson's disease progression (Review). Molecular Medicine Reports 24: 734, 2021.
Andrée-Anne Poirier et al: Gastrointestinal Dysfunctions in Parkinson’s Disease: Symptoms and Treatments. Parkinson’s Disease : Volume 2016, Article ID 6762528, 23 pages, http://dx.doi.org/10.1155/2016/6762528
Copyright © MediGloPark's All Rights Reserved.
루테인과 눈 건강
 루테인은 항염작용이 있는 것으로 알려진 일종의 카로티노이드(carotenoid)로서
많은 연구에서 눈에 이로운 효과를 나타내는 것으로 보고하고 있다.
카로티노이드는 각종 식품에 많이 들어 있는 영양소로서 특히 과일과 야채에
많이 분포한다. 충분한 양의 카로티노이드 섭취는 여러 질환에 유익하며, 특히
광독성적 손상으로부터 망막을 보호하는 등 안 질환에서
우수한 효과를 나타내는 것으로 알려져 있다. 카로티노이드 중에서도 가장
주목하고 있는 것중의 하나인 루테인은
강력한 항산화작용을 가지고 있어 노화와 관련된 질환의
위험성을 효과적으로 낮추어줄 수 있다. 루테인은 엽황소(葉黃素, xanthophyll), 즉
옥시카로티노이드로서 인간을 포함한 모든 포유동물은 카로티노이드를 합성할 수
없으므로 외부로부터 섭취하여야 한다.
노화와 관련된 황반질환은 시력상실이나 시력손상을 일으킬 수 있는데
루테인은 이러한 황반질환과 백내장을 개선하거나 예방하는데 도움이 되는 것으로 알려져 있다.
여러 연구에서 루테인은 안질환 외에 다른 다양한 질환에서도 긍정적인 효과가
있는 것으로 알려져 있는데 인지기능 개선, 암 발병율 저하, 심혈관 건강 지표의 개선 등이
보고되고 있다.
루테인은 항염작용이 있는 것으로 알려진 일종의 카로티노이드(carotenoid)로서
많은 연구에서 눈에 이로운 효과를 나타내는 것으로 보고하고 있다.
카로티노이드는 각종 식품에 많이 들어 있는 영양소로서 특히 과일과 야채에
많이 분포한다. 충분한 양의 카로티노이드 섭취는 여러 질환에 유익하며, 특히
광독성적 손상으로부터 망막을 보호하는 등 안 질환에서
우수한 효과를 나타내는 것으로 알려져 있다. 카로티노이드 중에서도 가장
주목하고 있는 것중의 하나인 루테인은
강력한 항산화작용을 가지고 있어 노화와 관련된 질환의
위험성을 효과적으로 낮추어줄 수 있다. 루테인은 엽황소(葉黃素, xanthophyll), 즉
옥시카로티노이드로서 인간을 포함한 모든 포유동물은 카로티노이드를 합성할 수
없으므로 외부로부터 섭취하여야 한다.
노화와 관련된 황반질환은 시력상실이나 시력손상을 일으킬 수 있는데
루테인은 이러한 황반질환과 백내장을 개선하거나 예방하는데 도움이 되는 것으로 알려져 있다.
여러 연구에서 루테인은 안질환 외에 다른 다양한 질환에서도 긍정적인 효과가
있는 것으로 알려져 있는데 인지기능 개선, 암 발병율 저하, 심혈관 건강 지표의 개선 등이
보고되고 있다.- References
Silvio Buscemi et al: The Effect of Lutein on Eye and Extra-Eye Health. Nutrients 2018, 10, 1321; doi:10.3390/nu10091321.
Xiaoming Gong et al: Carotenoid Lutein Selectively Inhibits Breast Cancer Cell Growth and Potentiates the Effect of Chemotherapeutic Agents through ROS-Mediated Mechanisms. Molecules 2018, 23, 905; doi:10.3390/molecules23040905.
Copyright © MediGloPark's All Rights Reserved.
비타민 D와 면역
 비타민 D는 칼슘이나 뼈의 항상성에 미치는 고전적 효과 외에도 인체 내에서 여러가지 중요한 역할을 수행한다.
비타민 D는 칼슘이나 뼈의 항상성에 미치는 고전적 효과 외에도 인체 내에서 여러가지 중요한 역할을 수행한다.면역세포인 수지상 세포, 대식세포, T세포 및 B세포는 비타민 D 수용체와 1알파-하이드록실라제(1alpha-hydroxylase)를 발현하며, 시험관내 연구에서 비타민 D의 활성형인 1, 25-디하이드록시비타민 D(1, 25-dihydroxyvitamin D)는 항염작용을 나타낸다. 또한 역학적 연구에서 비타민 D 결핍은 감염성 질환과 류머티스성 관절염, 전신적 홍반성 루프스(lupus erythematous), 다발성 경화증(multiple sclerosis)과 같은 염증성 자가면역 질환의 발현율을 증가시키고 질환을 악화시키는 것으로 나타났다. 비타민 D는 면역세포에 직접 작용하여 자가면역질환에서 중요한 역할을 한다. 임상연구에서도 비타민 D 결핍은 감염성 질환의 발병율과 관계가 있으며, 자가면역질환의 개시 및 진행과도 관계가 있는 것으로 보고되고 있다.
비타민 D를 보충하여 몇몇 염증성 질환을 예방하거나 치료를 하려는 시도가 있지만 이러한 비타민 D의 유용성에도 불구하고 그 효과는 아직 명백하지는 않다. 각 질환에서 비타민 D의 활성화 메커니즘을 결정하고 적절한 치료원칙을 정립하기 위해서는 앞으로 더 많은 연구가 필요한 것으로 보고되고 있다.
- References
Tomoka Ao et al: The Effects of Vitamin D on Immune System and Inflammatory Diseases. Biomolecules 2021, 11, 1624. https://doi.org/10.3390/biom11111624
Cynthia Aranow: Vitamin D and the Immune System. J Investig Med. 2011 August ; 59(6): 881–886. doi:10.231/JIM.0b013e31821b8755.
Copyright © MediGloPark's All Rights Reserved.
이상지질혈증과 코엔자임Q10
 코엔자임Q10은 지용성의 항산화제로서 심장, 간, 신장 등에 많이 분포하며 ATP 생성에 필수적인 미토콘드리아의 전자전달계에서
중요한 역할을 담당한다. 코엔자임Q10의 인체조직과 혈중에서의 수준은 노화와, 심근질환, 퇴행성질환, 당뇨 등과 같은
많은 질병상태에서 현저하게 감소한다. 이러한 다양한 질환에서 코엔자임Q10의 보충 시 그 효과를 확인하기 위한 많은 연구가 있었으나
그 결과는 일정하지 않다.
코엔자임Q10은 지용성의 항산화제로서 심장, 간, 신장 등에 많이 분포하며 ATP 생성에 필수적인 미토콘드리아의 전자전달계에서
중요한 역할을 담당한다. 코엔자임Q10의 인체조직과 혈중에서의 수준은 노화와, 심근질환, 퇴행성질환, 당뇨 등과 같은
많은 질병상태에서 현저하게 감소한다. 이러한 다양한 질환에서 코엔자임Q10의 보충 시 그 효과를 확인하기 위한 많은 연구가 있었으나
그 결과는 일정하지 않다. 한 연구에 의하면 코엔자임Q10은 24주간 투여 시 포도당, 인슐린, 중성지방, LDL 콜레스테롤 등의 혈중 수준을 개선하였으며, 아디포넥틴(adiponectin) 농도를 증가시키고 레시스틴(resistin) 농도를 감소시키는 것으로 나타났다. 아디포넥틴과 레시스틴은 렙틴(leptin) 등과 더불어 지방조직에서 분비되는 세포신호물질인 아디포카인(adipokine)류의 일종이다. 아디포넥틴은 인슐린 감수성 증가, 면역반응 촉진, 포도당 대사 촉진, 지방산 분해 촉진 등의 작용을 하며, 레시스틴은 인슐린 내성 증가, 면역반응 촉진 등의 작용을 한다.
코엔자임Q10 투여 시 나타나는 아디포넥틴과 레시스틴의 변화는 글루코리피드(glucolipid) 상태의 개선효과와 관계가 있는 것으로 보이며, 이러한 개선 효과는 코엔자임Q10이 아디포넥틴의 수준을 증가시키는 작용이 있기 때문인 것으로 보고되고 있다.
이러한 결과로서 코엔자임Q10은 여러가지 대사성질환을 가지고 있으면서 경미한 이상지질혈증을 나타내는 사람들에게 매우 좋은 선택이 될 것으로 기대가 되고 있다.
- References
Zhang et al: Coenzyme Q10 supplementation improves adipokine profile in dyslipidemic individuals: a randomized controlled trial. Nutrition & Metabolism (2022) 19:13.
Mohammad Vahid Jorat et al: The effects of coenzyme Q10 supplementation on lipid profiles among patients with coronary artery disease: a systematic review and meta-analysis of randomized controlled trials. Lipids in Health and Disease (2018) 17:230.
Copyright © MediGloPark's All Rights Reserved.
전립선질환과 쏘팔메토
 쏘팔메토(Saw Palmetto, Serenoa repens) 추출물은 다양한 지방산과 피토스테롤(phytosterol)들을 함유하며 비뇨기 기능부전 치료를 목적으로 서구에서 널리 사용되어 왔다.
더욱이 쏘팔메토 추출물은 천연약제로서 비교적 안전하고 부작용이 적어서
양성전립선비대증에 대체요법으로 사용되어질 수 있다는 보고도 있다.
쏘팔메토(Saw Palmetto, Serenoa repens) 추출물은 다양한 지방산과 피토스테롤(phytosterol)들을 함유하며 비뇨기 기능부전 치료를 목적으로 서구에서 널리 사용되어 왔다.
더욱이 쏘팔메토 추출물은 천연약제로서 비교적 안전하고 부작용이 적어서
양성전립선비대증에 대체요법으로 사용되어질 수 있다는 보고도 있다. 여러 연구에 따르면, 쏘팔메토 추출물의 비뇨기 증상 개선효과는 주로 항안드로겐 효과와 하부 요로계의 자율신경계 수용체에 대한 효과에 의한 것으로 보고되고 있다. 인체에서 가장 활발한 안드로겐인 5알파-디하이드로테스토스테론(5α-dihydrotestosterone, DHT)은 테스토스테론으로부터 5알파-환원효소(5α-reductase)에 의해 전환되며 전립선 비대증 등 생리학적 또는 병리학적 과정에서 중요한 역할을 한다. 쏘팔메토 추출물은 5알파-환원효소를 저해하는 것으로 알려져 있는데, 쏘팔메토 추출물의 스테롤(sterol)성분들과 지방산류가 효소결합자리에서 테스토스테론과 경쟁적 상호작용을 하여 효소억제 작용을 한다. 따라서 디하이드로테스토스테론의 생성이 감소하고 안드로겐 수용체 결합에 대한 디하이드로테스토스테론의 경쟁적 상호작용도 감소하게 된다. 또한 많은 연구에서 쏘팔메토 추출물이 안드로겐 대사를 조절하며 안드로겐의 작용을 차단하는 것으로 보고하고 있다.
이러한 결과들은 양성전립선비대증 등의 비뇨기질환에 쏘팔메토 추출물이 유용하게 이용될 수 있다는 것을 확인해주고 있으나 이에 대한 더 많은 연구가 필요한 것으로 보인다.
- References
Meng Liu et al: The Therapeutic Potential of Saw Palmetto Extract in Urological Disorders. Natural Product Communications (2021) 16(11): 1–8.
J. Curtis Nickel et al: Rethinking the Role of Saw Palmetto Extract for Men with Lower Urinary Tract Symptoms in North America. Uro 2022, 2, 137–150.
Copyright © MediGloPark's All Rights Reserved.
다발성 경화증과 비타민 D
 다발성 경화증은 이상감각의 초기증상과 운동장애를 특징으로 하며, 중추신경계에서 나타나는 염증성의 탈수초성 질환(demyelinating disease)으로서 보통 성인이 되면서 발병한다.
여러 연구에서 아동기의 비타민 D 결핍이 다발성 경화증의 발병과 관련이 있는 것으로 보고되었으며, 비타민 D가 면역조절작용이 있는 것으로 알려져 있기 때문에
낮은 비타민 D로 인해 비정상적 면역반응이 발생해서 다발성 경화증이 발생한다는 가설이 일반적이다. 그러나 비타민 D 수용체는 뉴런,
희소돌기아교세포(Oligodendrocyte), 성상교세포(星狀膠細胞, astrocyte), 미세아교세포(微細阿膠細胞, microglia) 등 많은 세포들에 존재하며,
비타민 D가 중추신경계의 발달과 기능에 많은 영향을 주기 때문에 낮은 비타민 D로 인해 중추신경계가 염증에 취약해지고 다발성 경화증 발병에 이르게 될
가능성이 있다.
다발성 경화증은 이상감각의 초기증상과 운동장애를 특징으로 하며, 중추신경계에서 나타나는 염증성의 탈수초성 질환(demyelinating disease)으로서 보통 성인이 되면서 발병한다.
여러 연구에서 아동기의 비타민 D 결핍이 다발성 경화증의 발병과 관련이 있는 것으로 보고되었으며, 비타민 D가 면역조절작용이 있는 것으로 알려져 있기 때문에
낮은 비타민 D로 인해 비정상적 면역반응이 발생해서 다발성 경화증이 발생한다는 가설이 일반적이다. 그러나 비타민 D 수용체는 뉴런,
희소돌기아교세포(Oligodendrocyte), 성상교세포(星狀膠細胞, astrocyte), 미세아교세포(微細阿膠細胞, microglia) 등 많은 세포들에 존재하며,
비타민 D가 중추신경계의 발달과 기능에 많은 영향을 주기 때문에 낮은 비타민 D로 인해 중추신경계가 염증에 취약해지고 다발성 경화증 발병에 이르게 될
가능성이 있다. 면역계와 신경계에서 비타민 D의 역할과 어린이에서 비타민 D 결핍이 어떠한 방식으로 다발성 경화증 발병에 영향을 주는지에 대해 분석한 한 연구에 따르면, 어린이에서 낮은 비타민 D는 다른 자가면역질환보다 다발성 경화증과 더욱 밀접한 관련이 있는 것으로 보이며, 비타민 D 결핍이 중추신경계가 염증에 취약해지는 중요한 원인이 될 수 있는 것으로 보고하였다.
따라서, 어린이의 비타민 D 결핍은 면역계와 중추신경계 모두에서 유전자 조절장애에 의해 성인이 되면서 다발성 경화증이 발생하는 하나의 위험한 원인이 될 수 있는 것으로 보고되고 있다.
- References
Sara E. Gombash et al: Vitamin D as a Risk Factor for Multiple Sclerosis: Immunoregulatory or Neuroprotective?. Front. Neurol., 16 May 2022.
Martina B. Sintzel et al: Vitamin D and Multiple Sclerosis: A Comprehensive Review. Neurol Ther (2018) 7:59–85.
Copyright © MediGloPark's All Rights Reserved.
이상지질혈증 치료제와 코엔자임Q10
 스타틴은 관상동맥질환의 예방 및 치료에 광범위하게 쓰인다. 그러나 스타틴의 이러한 유용성에도 불구하고 스타틴과 관련된
근육통과 같은 근육증상 부작용은 스타틴 복용 중단의 중요한 원인이 되고 있다. 이러한 근육통과 같은 부작용에 대한 대안으로 코엔자임Q10 투여와 같은
보조치료가 하나의 좋은 방법이 될 수 있는 것으로 보고되어 있다.
스타틴은 관상동맥질환의 예방 및 치료에 광범위하게 쓰인다. 그러나 스타틴의 이러한 유용성에도 불구하고 스타틴과 관련된
근육통과 같은 근육증상 부작용은 스타틴 복용 중단의 중요한 원인이 되고 있다. 이러한 근육통과 같은 부작용에 대한 대안으로 코엔자임Q10 투여와 같은
보조치료가 하나의 좋은 방법이 될 수 있는 것으로 보고되어 있다. 코엔자임Q10은 지용성 퀴놀론으로서 세포막의 소수성 부분에 분포하며 미토콘드리아의 에너지 대사와 근육세포막의 안정화에 중요한 역할을 한다. 즉, 코엔자임Q10은 미토콘드리아의 산화적 인산화 과정에서 전자전달에 관여하며, 활성산소에 의한 산화 스트레스를 막아주고, 항산화제인 아스코르브산과 토코페롤의 활성형을 만들어 미토콘드리아의 에너지 대사 유지와 근육 세포막 유지에 중요한 역할을 한다. 이러한 코엔자임Q10의 혈중농도가 스타틴 치료에 의해 감소된다는 보고가 있으나 그 결과가 모두 일치하지는 않는다. 스타틴 치료와 코엔자임Q10의 혈중농도 감소에 대한 무작위 배정 임상시험(Randomized Controlled Trial, RCT)들을 메타분석한 연구에서 친유성 스타틴과 친수성 스타틴 모두 코엔자임Q10의 감소를 발생시키며 두 그룹간의 의미 있는 차이는 없는 것으로 보고하였다. 또한, 저중정도의 강도를 갖는 스타틴과 고강도의 스타틴 모두 혈중 코엔자임Q10 농도의 감소에 영향을 미치는 것으로 나타났으며 이러한 영향은 스타틴 치료기간과 밀접한 관련 없이 발생하는 것으로 보고되었다. 이러한 스타틴 치료에 따른 혈중 코엔자임Q10 농도 감소의 기전은 분명하지 않으나 몇가지 가설이 제시되고 있다. 그중 하나는 스타틴 치료에 의해 코엔자임Q10의 합성이 감소된다는 것으로, 코엔자임Q10 합성과정에서 코엔자임Q10의 전구체인 farnesyl pyrophophate가 스타틴 치료로 차단되어 혈중 코엔자임Q10의 농도와 근육내 코엔자임Q10이 감소한다는 것이다. 두번째 가설은 스타틴 치료에 의해 식품 중 코엔자임Q10의 흡수가 감소할 수 있다는 것으로서, 마우스를 이용한 연구에서 스타틴에 의한 PXR(Pregnane Xenobiotic Receptor) 의존성 경로의 활성화와 스타틴의 항균성에 의한 장내 세균불균형(gut dysbiosis)으로 인해 장내 코엔자임Q10의 흡수가 영향을 받는 것으로 보고되어 있다.
따라서 스타틴계열의 약을 복용 시 코엔자임Q10 영양소의 고갈에 주의하여야 한다.
▷ 이상지질혈증약과 고갈 영양소
| 분류 | 성분명 | 고갈 영양소 |
|---|---|---|
| 스타틴 | 아토르바스타틴(Atorvastatin), 심바스타틴(Simvastatin) 등. | 코엔자임Q10(CoQ10) |
- References
Qu, H., Meng, Yy., Chai, H. et al: The effect of statin treatment on circulating coenzyme Q10 concentrations: an updated meta-analysis of randomized controlled trials. Eur J Med Res 23, 57 (2018).
Tatjana Rundek et al: Atorvastatin Decreases the Coenzyme Q10 Level in the Blood of Patients at Risk for Cardiovascular Disease and Stroke. Arch Neurol. 2004;61(6):889-892.
Richard Deichmann et al: Coenzyme Q10 and Statin-Induced Mitochondrial Dysfunction. The Ochsner Journal 10:16–21, 2010.
Caparrós-Martín JA, Lareu RR, Ramsay JP, Peplies J, Reen FJ, Headlam HA, et al. Statin therapy causes gut dysbiosis in mice through a PXR-dependent mechanism. Microbiome. 2017;5:95.
Copyright © MediGloPark's All Rights Reserved.
위염, 식도염약과 영양소
 위염 또는 식도염 치료제인 프로톤펌프억제제(Proton Pump Inhibitor, PPI)는 위산분비억제제이므로 장내 낮은 pH에서 흡수가 잘 되는
미량영양소들은 위산분비억제제로 인해 흡수가 저하되어 이들 영양소가 결핍될 수 있다.
위염 또는 식도염 치료제인 프로톤펌프억제제(Proton Pump Inhibitor, PPI)는 위산분비억제제이므로 장내 낮은 pH에서 흡수가 잘 되는
미량영양소들은 위산분비억제제로 인해 흡수가 저하되어 이들 영양소가 결핍될 수 있다.비타민 B12는 장내 흡수가 되기 위해서 음식 단백질로부터 분리가 되어야 하며 이때 위산이 필요하다. 단, 비타민 B12를 보충제로 복용하거나 비타민 B12를 강화한 식품을 섭취할 때는 단백결합상태의 비타민 B12를 분리하기 위한 위산이나 단백분해작용이 필요하지 않다. 사례대조군 및 전향코호트 연구에서 프로톤펌프억제제를 최소 12개월 이상 사용한 경우 비타민 B12 결핍의 위험성이 증가하는 것으로 보고되었으며, 프로톤펌프억제제에 의한 pH 증가를 더 심화시키고 위축성위염 발생 위험에 더 노출될 수 있는 흡연자, 또는 헤리코박터균 감염자의 경우 프로톤펌프억제제에 의한 비타민 B12 결핍에 더 취약한 것으로 알려져 있다.
▷ 위염, 식도염약과 고갈 영양소
| 분류 | 성분명 | 고갈 영양소 |
|---|---|---|
| 프로톤펌프억제제(Proton Pump inhibitors, PPI) | 오메프라졸(omeprazole), 에스오메프라졸(esomeprazole) 등. | 비타민 B12, 비타민 C, 철분(Fe), 칼슘, 마그네슘, 아연, 베타카로틴 |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
W.E. Kok et al: The association between polypharmacy and malnutrition(risk) in older people: A systematic review. Clinical Nutrition ESPEN 49 (2022) 163-171.
Copyright © MediGloPark's All Rights Reserved.
아스피린과 비타민 C
 아스피린을 단기간 비타민 C와 복용 시 백혈구내 비타민 C 흡수가 감소하는 것으로 나타났으나, 장기간 저용량의 아스피린을 복용한 경우
비타민 C 상태나 그 임상적 의미는 불분명한 것으로 알려져 있다.
아스피린을 단기간 비타민 C와 복용 시 백혈구내 비타민 C 흡수가 감소하는 것으로 나타났으나, 장기간 저용량의 아스피린을 복용한 경우
비타민 C 상태나 그 임상적 의미는 불분명한 것으로 알려져 있다. 최근 비타민 C 500mg과 아스피린 900mg으로 실시한 연구에서 혈액, 백혈구 및 소변의 비타민 C 농도를 측정하였는데, 비타민 C 보충으로 전체적으로 비타민 C 농도가 높게 나타났으나 아스피린을 같이 투여한 그룹에서는 비타민 C 보충에 의한 농도 증가가 현저하게 낮게 나타났다. 이러한 결과는 아스피린이 비타민 C의 장내 흡수를 방해하기 때문인 것으로 알려져 있다. 한편, 건강한 성인 남자를 대상으로 한 중재연구(intervention study)에서 600mg의 아스피린 투여로 2시간 경과 후 비타민 C 투여량(500-2000mg)에 관계없이 백혈구내 비타민 C 흡수가 완전하게 저해되는 것으로 나타난 반면에, 혈중 비타민 C는 아스피린의 영향을 받지 않는 것으로 나타났다. 연구자들은 아스피린이 비타민 C가 위장관에서 흡수되는 것을 저해하지는 않지만, 백혈구내 흡수를 저해하여 백혈구내 비타민 C 저장에 영향을 주는 것으로 결론을 내렸다. 흥미로운 것은 감기환자를 대상으로 한 실험에서는 건강한 사람을 대상으로 한 실험결과와 다르게 비타민 C 2000mg을 아스피린 600mg과 같이 또는 단독으로 투여 시 백혈구내 비타민 C 농도의 차이가 나타나지 않았는데, 이는 감기바이러스에 의해서 이들 상호작용이 변화되었기 때문으로 보인다고 보고되었다.
2400mg의 아스피린을 건강한 남녀에게 6일간 투여하는 전향적, 무작위, 이중맹검, 평행팔 연구(prospective, randomized, double-blind, parallel-arm study)에서는 소변, 혈장, 그리고 특히 위점막에서 비타민 C 농도가 감소하였다. 위점막의 비타민 C 감소는 아스피린으로 인한 장점막 흡수의 손상보다는 위점막손상에 대한 산화적 방어 작용이 증가하였기 때문으로 보인다.
비타민 C는 아스피린에 의한 위점막 병변을 막는데 도움이 되므로 아스피린 치료로 위점막 손상을 지니고 있는 환자들은 비타민 C 보충이 유익한 도움이 될 수 있는 것으로 보고되어 있다.
▷ 아스피린과 고갈 영양소
| 분류 | 성분명 | 고갈 영양소 |
|---|---|---|
| 비스테로이드성 소염진통제(NSAID) | 아스피린(Aspirin) | 비타민 C, 철분 |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
W.E. Kok et al: The association between polypharmacy and malnutrition(risk) in older people: A systematic review. Clinical Nutrition ESPEN 49 (2022) 163-171.
Copyright © MediGloPark's All Rights Reserved.
고혈압약(이뇨제)과 칼슘
 루프계 이뇨제는 칼슘의 배설을 촉진하여 체내 칼슘이 결핍상태로 되기 쉬우며, 치아자이드계 이뇨제는 반대로 칼슘 배설을 저해하여 체내 칼슘이 증가하는 상태로 될 수 있다.
동물실험에서 푸로세미드(furosemide)와 같은 루프계 이뇨제는 신장의 헨레고리에서 수동적 칼슘이송이 되도록 하는 내강쪽 상피통과 양전압을 저해하여
굵은 오름 헨레고리(the thick ascending loop of Henle)에서의 칼슘 재흡수를 억제한다.
루프계 이뇨제는 칼슘의 배설을 촉진하여 체내 칼슘이 결핍상태로 되기 쉬우며, 치아자이드계 이뇨제는 반대로 칼슘 배설을 저해하여 체내 칼슘이 증가하는 상태로 될 수 있다.
동물실험에서 푸로세미드(furosemide)와 같은 루프계 이뇨제는 신장의 헨레고리에서 수동적 칼슘이송이 되도록 하는 내강쪽 상피통과 양전압을 저해하여
굵은 오름 헨레고리(the thick ascending loop of Henle)에서의 칼슘 재흡수를 억제한다.건강한 성인에서 푸로세미드 80mg을 투여 시 칼슘의 배설과 혈장 부갑상선호르몬(parathyroid hormone, PTH)이 증가하는 것으로 나타났으며, 완경 이후 골감소증이 있는 여성을 대상으로한 임상연구에서는 루프계 이뇨제인 부메타니드(0.5-2.0mg/d bumetanide)의 뇨중 칼슘과 혈장 부갑상선호르몬에 대한 효과가 용량의존적인 것으로 나타났다. 이러한 결과는 루프계 이뇨제가 칼슘 항상성에 부정적 영향을 미치며, 이차적으로 부갑상선기능항진증을 초래할 수 있다는 것을 의미한다.
루프계 이뇨제에 의한 뇨중 칼슘 배출 증가는 장관내 칼슘 흡수 증가로 칼슘균형이 유지될 수 있지만, 노년층의 경우 장관내 칼슘 흡수가 효율적이지 않으므로 지속적인 루프계 이뇨제의 복용으로 인해 골밀도(Bone Mineral Density) 감소와 골절의 위험이 증가할 수 있다.
▷ 고혈압치료제(이뇨제)와 고갈 영양소
| 분류 | 성분명 | 고갈 영양소 |
|---|---|---|
| 고혈압치료제(루프계 이뇨제) | 푸로세미드(furosemide), 부메타니드(bumetanide) | 칼슘, 마그네슘, 칼륨 |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
W.E. Kok et al: The association between polypharmacy and malnutrition(risk) in older people: A systematic review. Clinical Nutrition ESPEN 49 (2022) 163-171.
Copyright © MediGloPark's All Rights Reserved.
고혈압약(이뇨제)과 마그네슘
 루프계 이뇨제, 또는 치아자이드계 이뇨제 사용 시 경미한 마그네슘 결핍은 비교적 일반적인 것으로 많은 연구에서 보고되고 있다. 루프계 이뇨제는 신장에서
마그네슘 재흡수를 직접적으로 저해하므로 단기간 및 장기간 치료 모두에서 마그네슘 결핍이 발생할 수 있다. 이와는 다르게 치아자이드계 이뇨제는
부갑상선 호르몬 억제를 포함한 여러 기전을 통하여 간접적으로 마그네슘 배출을 유도하므로 단기간 작용 보다는 장기간의 치아자이드 치료에 의해
마그네슘결핍이 발생하는 것으로 알려져 있다.
루프계 이뇨제, 또는 치아자이드계 이뇨제 사용 시 경미한 마그네슘 결핍은 비교적 일반적인 것으로 많은 연구에서 보고되고 있다. 루프계 이뇨제는 신장에서
마그네슘 재흡수를 직접적으로 저해하므로 단기간 및 장기간 치료 모두에서 마그네슘 결핍이 발생할 수 있다. 이와는 다르게 치아자이드계 이뇨제는
부갑상선 호르몬 억제를 포함한 여러 기전을 통하여 간접적으로 마그네슘 배출을 유도하므로 단기간 작용 보다는 장기간의 치아자이드 치료에 의해
마그네슘결핍이 발생하는 것으로 알려져 있다.마그네슘은 건강에 필수적인 미네랄이며 그 항상성은 장내 흡수와 신장 배설의 균형에 의해 조절된다. 마그네슘 섭취가 부족하거나 지속적인 알콜섭취, 마그네슘 결핍과 관련된 약의 장기복용, 또는 당뇨와 같은 기존 질병에 의해서도 저마그네슘혈증이 유발될 수 있다. 한편, 급성 또는 만성 신장질환, 갑상선기능저하증, 특히 부신피질기능부전 환자에서는 고마그네슘혈증이 유발되는 경우도 있다.
적절한 마그네슘의 섭취와 마그네슘 항상성을 유지하는 것은 근골격계의 유연성과 (근)섬유 재생력을 바르게 하여 근골격계의 건강을 유지하는데 필수적인 것으로 알려져 있다.
▷ 고혈압치료제(이뇨제)와 고갈 영양소
| 분류 | 성분명 | 고갈 영양소 |
|---|---|---|
| 고혈압치료제(루프계 이뇨제) | 푸로세미드(furosemide), 부메타니드(bumetanide) | 칼슘, 마그네슘, 칼륨 |
| 고혈압치료제(치아자이드계 이뇨제) | 하이드로클로로치아자이드(hydrochlorothiazide) | 마그네슘, 칼륨 |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
W.E. Kok et al: The association between polypharmacy and malnutrition(risk) in older people: A systematic review. Clinical Nutrition ESPEN 49 (2022) 163-171.
Monica Zocchi et al: Magnesium Influences Membrane Fusion during Myogenesis by Modulating Oxidative Stress in C2C12 Myoblasts. Nutrients 2021, 13, 1049.
Copyright © MediGloPark's All Rights Reserved.
고혈압약(이뇨제)과 비타민 B1
 루프계 이뇨제는 티아민(비타민 B1)의 뇨배설을 증가시키는 것으로 동물실험과 임상연구를 통하여 보고되었다. 이들 연구에서
티아민 배설율은 배뇨율과 관계가 있는 것으로 나타났는데, 이는 티아민 손실이 지속적이고 증가된 이뇨작용에 의한 것이며, 하나의 특정
이뇨제에 특이성이 있지는 않은 것으로 나타났다.
루프계 이뇨제는 티아민(비타민 B1)의 뇨배설을 증가시키는 것으로 동물실험과 임상연구를 통하여 보고되었다. 이들 연구에서
티아민 배설율은 배뇨율과 관계가 있는 것으로 나타났는데, 이는 티아민 손실이 지속적이고 증가된 이뇨작용에 의한 것이며, 하나의 특정
이뇨제에 특이성이 있지는 않은 것으로 나타났다. 또한 루프계 이뇨제인 푸로세미드(furosemide)를 복용중인 울혈성 심부전 환자의 티아민 상태를 조사한 연구에서 같은 연령대의 대조군에 비해 생화학적 티아민 결핍 유병율이 매우 우세하게 나타났으며, 그 생화학적 티아민 결핍 유병율은 푸로세미드의 용량증가에 따라 심화되는 것으로 나타났다.
이러한 티아민에 대한 이뇨제의 영향은 노년층에서 특히 문제가 되는데, 노인의 경우 티아민의 식이 섭취가 낮기 때문에 티아민 결핍의 위험성이 크다고 할 수 있다. 평균 70세의 입원한 노인환자들을 대상으로 한 연구에서 푸로세미드의 반복적인 투여로 인해 티아민 결핍상태가 발생하는 것으로 보고되었으며, 60세 이상의 외래 노인환자들을 대상으로한 이뇨제와 티아민 결핍을 조사한 연구에서도 이뇨제를 복용한 환자들은 복용하지 않는 그룹에 비해 상당한 결핍상태가 관찰되는 것으로 보고되었다.
한편, 티아민은 신경계 기능에 매우 중요하며 각종 효소의 보조효소에 이용되는데, 특히 뇌 에너지 대사에 필수적이다. 티아민 결핍으로 신경전달물질, 핵산, 스테로이드 및 지방산 합성 등이 저해될 수 있다.
▷ 고혈압치료제(이뇨제)와 고갈 영양소
| 분류 | 성분명 | 고갈 영양소 |
|---|---|---|
| 고혈압치료제(루프계 이뇨제) | 푸로세미드(furosemide), 부메타니드(bumetanide) | 칼슘, 마그네슘, 칼륨, 티아민(비타민 B1) |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
Monica Zocchi et al: Magnesium Influences Membrane Fusion during Myogenesis by Modulating Oxidative Stress in C2C12 Myoblasts. Nutrients 2021, 13, 1049.
Iva Bozic, Irena Lavrnja: Thiamine and benfotiamine: Focus on their therapeutic potential. Heliyon 9 (2023) e21839.
Copyright © MediGloPark's All Rights Reserved.
고혈압약(이뇨제)과 칼륨
 루프계 이뇨제와 치아자이드계 이뇨제 모두 장기복용에 따른 뇨중 칼륨 배설이 문제가 되지만, 치아자이드계 이뇨제의 경우 루프계 이뇨제보다 더
빈번하게 저칼륨혈증을 야기하므로 대부분의 연구가 치아자이드계 이뇨제에 주목하고 있다.
루프계 이뇨제와 치아자이드계 이뇨제 모두 장기복용에 따른 뇨중 칼륨 배설이 문제가 되지만, 치아자이드계 이뇨제의 경우 루프계 이뇨제보다 더
빈번하게 저칼륨혈증을 야기하므로 대부분의 연구가 치아자이드계 이뇨제에 주목하고 있다. 루프계 이뇨제가 헨레고리에서 칼륨의 재흡수를 직접 저해하는 것과는 다르게, 치아자이드계 이뇨제는 여러 기전으로 신장에서 칼륨의 배설을 촉진한다. 영국에서 951명의 환자를 대상으로 치아자이드 처방과 전해질 이상의 관련성을 조사한 연구에 따르면 전체의 8.5%에서 저칼륨혈증이 발생하였으며, 이 저칼륨혈증은 치아자이드계 이뇨제 복용에 따른 것으로 명확하게 나타났다. 또한, hydrochlorothiazide, chlorthalidone 및 bendroflumethiazide 사용과 혈중 칼륨의 용량-반응 관계를 조사한 메타분석에 따르면, bendroflumethazide가 가장 강력하게 칼륨 감소를 나타냈으며 hydrochlorothiazide가 가장 약한 것으로 나타났다.
치아자이드계 이뇨제에 의한 저칼륨혈증은 혈당증가와 심실성 부정맥과 관련이 있는 것으로 알려져 있다. 칼륨 보충은 루프계 이뇨제 또는 치아자이드계 이뇨제 사용에 기인한 저칼륨혈증의 증상을 나타내는 환자들에서 이루어질 수 있다. 그러나 칼륨 보충이 이뇨제 자체보다 더 혈압을 저하시켜 저혈압을 강하게 야기할 수 있으므로 주의하여야 한다. 대안으로는 칼륨 보존성 이뇨제를 사용하는 것으로서, 칼륨 보존성 이뇨제는 칼륨의 손실을 막는데 도움이 될 뿐만 아니라 루프계 이뇨제 및 치아자이드계 이뇨제에서 유사하게 손실될 수 있는 마그네슘과 같은 다른 이온들의 손실도 방지할 수 있다.
▷ 고혈압치료제(이뇨제)와 고갈 영양소
| 분류 | 성분명 | 고갈 영양소 |
|---|---|---|
| 고혈압치료제(루프계 이뇨제) | 푸로세미드(furosemide), 부메타니드(bumetanide) | 칼슘, 마그네슘, 칼륨, 티아민(비타민 B1) |
| 고혈압치료제(치아자이드계 이뇨제) | 하이드로클로로치아자이드(hydrochlorothiazide), 클로르탈리돈(chlorthalidone) | 마그네슘, 칼륨 |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
Monica Zocchi et al: Magnesium Influences Membrane Fusion during Myogenesis by Modulating Oxidative Stress in C2C12 Myoblasts. Nutrients 2021, 13, 1049.
Thu Kyaw M, Maung Z (March 07, 2022) Hypokalemia-Induced Arrhythmia: A Case Series and Literature Review. Cureus 14(3): e22940. DOI 10.7759/cureus.22940
Copyright © MediGloPark's All Rights Reserved.
고혈압약(안지오텐신 전환효소 저해제)과 아연
 안지오텐신 전환효소(Angiotensin-Converting Enzyme, ACE) 저해제를 장기 복용 시 미각감퇴증(味覺減退症, hypogeusia)이 발생될 수가 있는데 캅토프릴(captopril)이 대표적이다. 아연 결핍증상 중 하나가
미각상실이므로, 캅토프릴이 미각의 예민도와 아연상태에 미치는 영향에 대해 고혈압 환자들을 대상으로 조사가 이루어졌다. 6개월 이상 매일 캅토프릴을 고용량인
266mg씩 복용한 환자군에서 대조군에 비해 미각 판독 및 인지에 관한 역치가 더 높은 것으로 나타났으며, 아연의 혈장 수준도 더 낮게 나타났고, 뇨중 아연 배설도
더 높게 나타났다. 이러한 결과는 캅토프릴로 인한 미각상실이 아연상태의 감소와 관련이 있을 수 있다는 것을 의미한다. 한편, 매일 100mg의 캅토프릴을 복용하는
고혈압 환자들에서 5-6개월 후 혈청 아연상태를 조사한 결과에서는 변화가 관찰되지 않았는데, 이는 아연상태에 대한 캅토프릴의 영향이 용량 의존성이 있기
때문인 것으로 보인다. 그러나 매일 50mg의 낮은 용량의 캅토프릴을 복용하는 경우에도 신장질환자나 심부전 환자에서는 아연상태가 낮게 나타나는 것으로 밝혀졌다.
안지오텐신 전환효소(Angiotensin-Converting Enzyme, ACE) 저해제를 장기 복용 시 미각감퇴증(味覺減退症, hypogeusia)이 발생될 수가 있는데 캅토프릴(captopril)이 대표적이다. 아연 결핍증상 중 하나가
미각상실이므로, 캅토프릴이 미각의 예민도와 아연상태에 미치는 영향에 대해 고혈압 환자들을 대상으로 조사가 이루어졌다. 6개월 이상 매일 캅토프릴을 고용량인
266mg씩 복용한 환자군에서 대조군에 비해 미각 판독 및 인지에 관한 역치가 더 높은 것으로 나타났으며, 아연의 혈장 수준도 더 낮게 나타났고, 뇨중 아연 배설도
더 높게 나타났다. 이러한 결과는 캅토프릴로 인한 미각상실이 아연상태의 감소와 관련이 있을 수 있다는 것을 의미한다. 한편, 매일 100mg의 캅토프릴을 복용하는
고혈압 환자들에서 5-6개월 후 혈청 아연상태를 조사한 결과에서는 변화가 관찰되지 않았는데, 이는 아연상태에 대한 캅토프릴의 영향이 용량 의존성이 있기
때문인 것으로 보인다. 그러나 매일 50mg의 낮은 용량의 캅토프릴을 복용하는 경우에도 신장질환자나 심부전 환자에서는 아연상태가 낮게 나타나는 것으로 밝혀졌다.이들 연구들을 종합해보면, 캅토프릴이 아연상태를 낮출 수 있으며, 아연결핍의 위험성을 증가시킬 수 있지만, 고용량의 캅토프릴을 장기간 복용하는 경우나 고혈압과 다른 질병을 같이 앓고 있는 경우에 국한된다고 볼 수 있다.
캅토프릴과 에날라프릴(enalapril)이 아연상태에 미치는 영향을 비교한 연구에서, 안지오텐신 전환효소 억제제를 복용한 그룹은 치료하지않은 고혈압환자 그룹 또는 건강한 그룹에 비해 아연상태가 감소하는 것으로 나타났으며, 특히 캅토프릴을 장기간 복용한 경우 에날라프릴을 복용한 경우에 비해 아연상태에 더 큰 영향을 미치는 것으로 밝혀져다. 캅토프릴과 베나제프릴(benazepril)이 아연상태에 미치는 영향에 대한 연구에서도 4주 후 고혈압 환자에서 두 약물 모두 혈청 아연을 감소시켰으며 뇨중 아연 배설을 증가시키는 것으로 밝혀졌으며, 8주 후 캅토프릴 복용 환자 그룹에서 더욱 심각한 아연감소가 나타나는 것으로 보고되었다.
결론적으로, 안지오텐신 전환효소 억제제들은 아연결핍의 위험성을 증가시킬 수 있으며, 특히 이러한 영향은 캅토프릴에서 더욱 심각한 것으로 생각할 수 있다. 그 기전은 캅토프릴 구조의 치올-라디칼(thio-radical) 그룹이 혈청 아연을 킬레이트화하여 그 배설을 촉진하기 때문인 것으로 알려져 있다.
▷ 고혈압치료제(안지오텐신 전환효소 저해제)와 고갈 영양소
| 분류 | 성분명 | 고갈 영양소 |
|---|---|---|
| 고혈압치료제(안지오텐신전환효소 저해제) | 캅토프릴(captopril), 에날라프릴(enalapril) | 아연(Zn) |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
Daoud K. Abu-Hamdan, Hema Desai, James Sondheimer, James Felicetta, Sudesh Mahajan, and Franklin McDonald: Taste Acuity and Zinc Metabolism in Captopril-treated Hypertensive Male Patients. American Journal of Hypertension, Volume 1, Issue 3_Pt_3, July 1988, Pages 303S–308S.
Wenyue Zheng et al: Small molecule angiotensin converting enzyme inhibitors: A medicinal chemistry perspective. Front. Pharmacol., 01 November 2022.
Copyright © MediGloPark's All Rights Reserved.
고혈압약(안지오텐신 전환효소 저해제)과 칼륨
 안지오텐신 전환효소(Angiotensin-Converting Enzyme, ACE) 저해제는 알도스테론 분비를 억제하여 신장에서 칼륨 저류를 일으킬 수 있다.
안지오텐신 전환효소(Angiotensin-Converting Enzyme, ACE) 저해제는 알도스테론 분비를 억제하여 신장에서 칼륨 저류를 일으킬 수 있다.ACE 저해제와 관련된 고칼륨혈증의 발현율은 1-2%이지만, 고칼륨, 저염식을 하는 노인들의 경우는 ACE 저해제로 인해 고칼륨혈증의 위험성이 더욱 커지는 것으로 보고되고 있다. 또한, 만성 신부전환자와 당뇨환자에서도 ACE 저해제의 사용으로 고칼륨혈증의 위험성이 증가하는 것으로 알려져 있다. 이러한 고칼륨혈증의 위험성은 ACE 저해제를 복용하는 울혈성 심부전환자에서 더욱 커지며, 특히 칼륨보충제나 칼륨이 많은 식품을 섭취하는 경우 그 위험성이 증가하는 것으로 보고되어 있다. 한 연구에서는 40개월간 에날라프릴(enalapril)을 복용한 그룹이 위약대조군보다 고칼륨혈증의 위험성이 3배 이상인 것으로 나타났다.
결과적으로, 노령, 신장질환, 당뇨병, 울혈성 심부전, 칼륨보존성 이뇨제의 사용, 칼륨보충제 또는 칼륨이 많은 식품의 섭취 등은 ACE저해제를 복용중인 환자에서 고칼륨혈증의 위험성을 더욱 증가시키는 원인이 될 수 있다.
▷ 고혈압치료제(안지오텐신 전환효소 저해제)와 고칼륨혈증
| 분류 | 성분명 | 증가 영양소 | 주의사항 |
|---|---|---|---|
| 고혈압치료제(안지오텐신전환효소 저해제) | 에날라프릴(enalapril) 등. | 칼륨(K) | 고칼륨혈증 |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
Biff F. Palmer: Managing Hyperkalemia Caused by Inhibitors of the Renin–Angiotensin–Aldosterone System. N Engl J Med 2004;351:585-92.
Copyright © MediGloPark's All Rights Reserved.
고혈압약(칼슘채널차단제)과 엽산
 칼슘채널차단제(Calcium Channel Blockers, CCBs) 고혈압약을 복용 시 치은증식증(齒齦增殖症, gingival hyperplasia)이 나타나는 경우가 있는데 대부분 남자에서 나타나며
여자의 경우에도 나타날 수 있다. 대부분의 칼슘채널차단제에서 이러한 증상이 발생될 수 있지만 암로디핀과 니페디핀(nifedipine) 복용 시에 많이 나타나는 것으로 알려져 있으며,
네덜란드에서 시행된 연구를 보면 칼슘채널차단제에 의해 용량 의존적으로 치은증식증의 위험성이 두 배로 증가하는 것으로 나타났다.
칼슘채널차단제(Calcium Channel Blockers, CCBs) 고혈압약을 복용 시 치은증식증(齒齦增殖症, gingival hyperplasia)이 나타나는 경우가 있는데 대부분 남자에서 나타나며
여자의 경우에도 나타날 수 있다. 대부분의 칼슘채널차단제에서 이러한 증상이 발생될 수 있지만 암로디핀과 니페디핀(nifedipine) 복용 시에 많이 나타나는 것으로 알려져 있으며,
네덜란드에서 시행된 연구를 보면 칼슘채널차단제에 의해 용량 의존적으로 치은증식증의 위험성이 두 배로 증가하는 것으로 나타났다.칼슘채널차단제의 사용과 치은증식증의 연관성은 암로디핀(amlodipine)과 니페디핀을 복용하는 그룹과 대조군을 비교 조사한 여러 연구에서 확인되었다. 2017년 발표된 나이지리아에서의 연구에서는 칼슘채널차단제 복용군이 비복용군에 비해 거의 3배정도 치은증식의 위험성이 관찰되었으며, 니페디핀보다 암로디핀에서 2배 높게 나타나는 것으로 보고하였다. 이러한 치은증식증의 발현은 치태(齒垢, dental plaque)와 비위생적 구강상태에 의해서 발생할 수도 있지만, 치근 섬유아세포(gingival fibroblasts)로 엽산의 흡수가 저해되는 것이 주된 원인이다. 따라서 엽산보충을 통해 치은증식증의 발현과 정도를 감소시키고 그 개시를 늦추고자하는 연구가 있었지만, 이 연구들은 항경련약물로 인한 치은증식증에 한정된 것이어서 칼슘채널차단제로 인한 치은증식증에 대한 더 많은 연구가 필요하다. 한편, 칼슘채널차단제를 복용하는 환자들의 엽산섭취는 전문적인 상담과 권고에 따라야 할 것으로 보인다.
▷ 고혈압치료제(칼슘채널차단제)와 치은증식증
| 분류 | 치은증식증 유발 가능 성분명 | 영양소 |
|---|---|---|
| 고혈압치료제(칼슘채널차단제) | 암로디핀(amlodipine), 니페디핀(nifedipine) 등. | 엽산(Folate) |
- References
Emily S. Mohn et al: Evidence of Drug–Nutrient Interactions with Chronic Use of Commonly Prescribed Medications: An Update. Pharmaceutics 2018, 10, 36; doi:10.3390/pharmaceutics10010036.
Umeizudike KA, Olawuyi AB, Umeizudike TI, Olusegun-Joseph AD, Bello BT: Effect of calcium channel blockers on gingival tissues in hypertensive patients in Lagos, Nigeria: A pilot study. Contemp Clin Dent 2017;8:565-70.
Agnieszka Dro´zdzik, Marek Dro´zdzik: Drug-Induced Gingival Overgrowth—Molecular Aspects of Drug Actions. Int. J. Mol. Sci. 2023, 24, 5448.
Copyright © MediGloPark's All Rights Reserved.
한의학의 특징
한의학의 2가지 특징
1) 전체관(全體觀) 2) 변증시치(辨證施治)
I. 전체관
1) 인체 내부의 통일체관(統一體觀)
- 인체는 기(氣), 혈(血), 진액(津液), 정(精)을 기본으로 하여 구성되며 간(肝), 심(心), 비(脾), 폐(肺), 신(腎)의 오장(五臟)과 담(膽), 심포(心包), 위(胃), 대장(大場), 방광(膀胱), 삼초(三焦)의 6부(六胕)가 경락(經絡)을 통해 하나의 통일체가 되어 있다.
2) 인체와 자연환경 간의 통일체관
– 인체 내부의 기능(機能) 실조(失調)나 기능 저하(低下)로 인해 외계(外界) 환경의 변화에 적응하지 못할 때 질병(疾病)이 발생한다. 질병이 발생하는 근본 원인은 인체의 ‘내인(內因)’에 있으며 외계변동에 의한 ‘외인(外因)’은 단순한 발병조건에 지나지 않는다.
즉, ‘外因은 內因을 통해서 발현한다.’
발병 후에는 인체의 정기(精氣)( : 저항력(抵抗力))와 병사(病邪)( : 발병인자(發病因子))의 세력 관계에 의해서 경과(經過)가 결정되며 ‘정기(精氣)의 부조(扶助)와 병사(病邪)의 제거(除去)’라는 양면(兩面)을 고려한 치료를 행하는 것도 한의학의 큰 특징이다.
II. 변증시치(辨證施治) ( = 변증논치(辨證論治)) :
한의학의 진단과 치료의 전(全) 과정으로서 변증(辨證)과 시치(施治)의 2개 부분으로 구성되어 있다.
“변증(辨證)은 시치(施治)의 전제(前提)이며 시치(施治)는 변증(辨證)의 목적(目的)이다,’
변증시치의 기초는 전체관이다.
1. 변증(辨證)(=변증구인(辨證求因)) :
사진(四診) ( : ① 망진(望診), ② 문진(問診), ③ 문진(聞診), ④절진(切診))법에 의해서 질병의 원인(原因), 경과(經過), 예후(豫後)를 진단(診斷)함과 동시에 환자(患者)의 상태(狀態), 질병의 성질(性質)과 부위(部位), 정기(精氣)와 병사(病邪)의 세력 관계 등을 변별(辨別)하는 것을 말한다.
변증에는
① 팔강변증(八綱辨證) (八綱 : 표(表), 리(裏), 한(寒,) 열(熱), 허(虛), 실(實), 음(陰), 양(陽)),
② 기혈변증(氣血辨證) (=기혈진액변증(氣血津液辨證) : 기(氣), 혈(血), 진액(津液), 정(精)의 상황(狀況)을 변별(辨別)),
③ 장부변증(臟胕辨證),
④ 병사변증(病邪辨證)(=病因辨證 : 풍(風), 한(寒,) 서(暑), 습(濕), 조(燥), 화(火)(열(熱))의 외감육음(外感六淫)과 식적(食積), 담음(痰飮), 어혈(瘀血) 등의 병사(病邪)에 의한 질병(疾病)의 상황(狀況)을 변별(辨別)),
⑤ 외감열병변증(外感熱病辨證) ( : 한사(寒邪)에 의한 양기(陽氣) 손상(損傷)의 경과를 주로 분석한 상한론(傷寒論)의 ㉮ 육경변증(六經辨證)과 열사(熱邪)에 의한 음액(陰液) 소모(消耗) 의 경과(經過)를 주로 분석한 ㉯ 위기영혈변증(衛氣營血辨證)은 질병의 경과가 다르기 때문에 상위(相違)한 부분이 많으나 상호(相互) 교통(交通)되는 부분도 있다),
⑥ 경락변증(經絡辨證),
⑦ 사상인변증(四象人辨證) 등이 대표적이다.
2. 施治(=심인논치) :
施治의 3대 요소 – ① 치칙(治則) : 최적의 치료 수순, ② 치법(治法) : 치칙에 따른 구체적인 치료법, ③ 처방(處方) : 치법에 의해 결정되는 구체적인 수단
* 施治의 2대 요소 : ① 治則, ② 治法
* 이병동치(異病同治) : 다른 환자라도 같은 증(證)이면 같은 치법을 행한다.
* 동병이치(同病異治 ): 동일한 개체의 동일한 질환일지라도 경과나 시기의 상위로 인해 다른 치법을 행한다.
Copyright © MediGloPark's All Rights Reserved.